La ecografía pulmonar (EP) es una herramienta indispensable actualmente en las consultas de neumología. Tiene grandes ventajas tales como: reproducibilidad, bajo costo y ausencia de radiaciones ionizantes, pero también presenta 2limitaciones principales: la incompatibilidad con el aire y ser operador dependiente. Los hallazgos en la EP en un parénquima pulmonar sano ofrecen diferentes signos, como puede ser el signo del deslizamiento pleural y los artefactos denominados líneas A y B.
Concretamente, que aparezcan más de 3 líneas B por zona explorada puede traducir un engrosamiento de los septos interlobulillares y, si además se acompaña de la presencia de rugosidad, engrosamiento y desestructuración de la línea pleural, puede orientar a una enfermedad pulmonar intersticial (EPID)1-4.
En estos pacientes que presentan EPID, hasta la actualidad no ha existido ningún método ecográfico que cuantifique la gravedad de la afectación del parénquima pulmonar y que pudiera ser de utilidad en su seguimiento. Por ello, hoy en día sigue siendo necesaria la tomografía computarizada de alta resolución (TCAR) para la valoración de la gravedad y evolución de estos pacientes5-8.
Los métodos de ultrasonido más utilizados para evaluar la fibrosis (más concretamente, la fibrosis hepática) son las técnicas de elastografía por ultrasonido. Pero la ultrasonografía convencional, basada en el análisis morfológico en una escala de grises, podría contener más información que la administrada por la elastografía. El método de cuantificación de la estructura acústica (ASQ) es una herramienta no invasiva que se utiliza para caracterizar los tejidos a través de un análisis estadístico de las señales de ultrasonidos recibidas. Cuando el tejido es normal, el pulso de eco generado es menor que la longitud de onda del ultrasonido, siguiendo la distribución normal de Rayleigh (función de distribución continua). Cuando el tejido es fibrótico, los pulsos de eco se vuelven más grandes que la longitud de onda, y se desvían de la distribución de Rayleigh9-11.
En la actualidad se está utilizando ASQ para la caracterización de la fibrosis hepática. A diferencia de la técnica de elastografía, las imágenes ASQ se generan por la interferencia del ultrasonido generada por innumerables objetos reflexivos. Según esta teoría, la medición del patrón moteado del tejido explorado con el análisis de la función de probabilidad de densidad podría cuantificar la heterogeneidad tisular. A partir de estos principios, y dado que no existen estudios publicados previamente, este trabajo estudió el método ASQ para la evaluación de las EPID12-15.
Para ello, se ha realizado por primera vez un estudio prospectivo, observacional y aleatorizado de casos y controles con el que se valoró si la EP con método ASQ podría cuantificar la severidad en las EPID fibrosantes. Se recopilaron 2grupos de pacientes, tras la aprobación del CEIC y la firma del consentimiento informado. Los del grupo 1, pacientes con EPID y afectación demostrada en el TCAR. Y el grupo 2, formado por pacientes sanos sin enfermedad respiratoria, con ausencia de antecedente de hábito tabáquico, con auscultación pulmonar, espirometría y radiografía de tórax normales.
En un primer momento, en la consulta de neumología, se realizaba una evaluación ecográfica a los 2grupos de pacientes, y después con el método ASQ. Se utilizó una sonda convexa y se capturaron varias imágenes en modo B a través de un acceso intercostal. En los pacientes con EPID se buscaba el punto con mayor afectación intersticial visualizado previamente en el TCAR. Y en los pacientes sanos, el mejor plano axial de las bases pulmonares.
Las imágenes obtenidas se interpretaron bajo el análisis ASQ, dibujando 3ROI de manera aleatorizada, que incluyeran la musculatura intercostal, la línea pleural y el parénquima pulmonar. Se recogió la media y la desviación estándar en cada medición (datos que calculaba el mismo equipo ecográfico). Además, se obtuvo un mapa multiparamétrico basado en la distribución de la amplitud de los ecos, donde altos valores de Cm2 (parámetro estadístico derivado de la diferente distribución de la amplitud de los ecos) se representan en un gris más oscuro y los valores bajos en un gris más claro. Debido a que, en el caso de la fibrosis hepática, la dispersión se incrementa proporcionalmente con la distorsión de la arquitectura parenquimatosa y da lugar a un color rojo, hemos aplicado esta misma premisa en este trabajo, pero relacionándolo con la fibrosis pulmonar.
Los valores de heterogenicidad de los datos obtenidos en los ROI se recogieron como media y desviación estándar, y las comparaciones entre grupos se realizaron con la prueba de Mann-Whitney. Se consideraron significativos aquellos valores de probabilidad inferiores a 0,05.
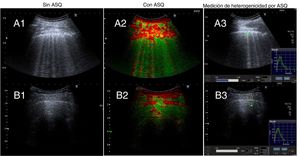
Se incluyó a un total de 20 pacientes (10 pacientes por cada grupo). En el grupo 1, la edad media fue de 74,7±8,8 años, con un 60% de hombres. Los patrones intersticiales pulmonares con componente fibrótico en el TCAR se distribuyeron de la siguiente manera: neumonía intersticial usual en 5 pacientes, neumonía intersticial no específica en 3 y neumonitis por hipersensibilidad crónica en 2. En la EP sin ASQ (fig. 1A) se observó rugosidad, engrosamiento y desestructuración de la línea pleural y múltiples líneas B (más de 3) por campo explorado. La EP con ASQ (fig. 1A2-A3), se representó con un mapa multiparamétrico, midiendo la heterogenicidad en el parénquima pulmonar (1,42±0,086), línea pleural (1,58±0,172) y extrapleural (1,16±0,138). En el grupo 2, la edad media era de 44,1±5,8 años, con un 30% de hombres. La EP sin ASQ (fig. 1B1) presentó una línea pleural fina y conservada, líneas B (menos de 3) y líneas A. La EP con ASQ (fig. 1B2-B3) mostró el mapa multiparamétrico y midió la relación de heterogenicidad en el parénquima pulmonar (1,05±0,118), línea pleural (1,43±0,178) y extrapleural (1,32±0,150).
Ecografía pulmonar sin ASQ y con ASQ.
Grupo 1. A1: sin método ASQ, existe rugosidad, engrosamiento y desestructuración de la línea pleural y múltiples líneas B. A2 y A3: método ASQ, representación multiparamétrica y medición de la heterogenicidad pulmonar, respectivamente.
Grupo 2. B1: sin método ASQ, existe línea pleural fina y conservada, líneas B (menos de 3) y líneas A. B2 y B3: método ASQ, representación multiparamétrica y medición de la heterogenicidad pulmonar, respectivamente.
Existieron diferencias estadísticamente significativas en la relación de la cuantificación de la heterogenicidad tisular entre ambos grupos, en el parénquima pulmonar (p <0,01) y extrapleural (p <0,05).
El trabajo actual tiene la limitación de presentar un tamaño muestral pequeño. Sin embargo, dados los hallazgos obtenidos en este primer estudio preliminar, concluimos que la EP con la aplicación ASQ podría llegar a cuantificar el grado de afectación intersticial y orientarnos en el manejo de estos pacientes. Aunque será necesario un estudio con un tamaño muestral mayor y con reproducción de las medidas obtenidas por ecografía.
FinanciaciónEl manuscrito actual no ha tenido fuente de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses relacionado directa o indirectamente con los contenidos del manuscrito.
A todas las personas que han colaborado en este trabajo.