La toracoscopia rígida y la semirrígida (TS) desempeñan un papel en el diagnóstico de los derrames pleurales malignos (DPM), especialmente los debidos a carcinomas de pulmón1–5. El toracoscopio semirrígido presenta ventajas derivadas de su flexibilidad y baja invasividad, pero también tiene algunas desventajas, como un canal de trabajo estrecho y, especialmente, un fórceps de biopsia débil y flexible, que obtiene muestras más pequeñas que las obtenidas con la toracoscopia rígida. No obstante, ha demostrado una alta sensibilidad y precisión diagnóstica6, siendo también un procedimiento seguro para el diagnóstico de derrames pleurales inexplicables. Además, al igual que en la toracoscopia rígida, la pleurodesis se puede lograr en el mismo procedimiento7–10.
La caracterización molecular del cáncer de pulmón no microcítico es cada vez más importante, ya que los tumores que albergan mutaciones somáticas en genes como el receptor del factor de crecimiento epidérmico (EGFR) o la quinasa anaplásica de linfoma (ALK) aumentan la capacidad de respuesta a los tratamientos dirigidos. Hay un aumento en los estudios que evalúan no solo la precisión diagnóstica de malignidad con diferentes técnicas diagnósticas, sino también la adecuación de las muestras obtenidas para la evaluación inmunohistoquímica y las determinaciones moleculares de la mutación EGFR y el estado de translocación ALK11. Sin embargo, hay muy pocos datos disponibles sobre la adecuación de la TS, centrándose la mayoría de los estudios en los ultrasonidos endobronquiales (EBUS-TBNA). Solo hay un estudio que evalúa la TS para analizar el estado de la mutación EGFR y ninguno que realice el análisis de translocación ALK en DPM por adenocarcinoma pulmonar, probablemente debido al tamaño de muestra limitado obtenido con este procedimiento12.
El objetivo de nuestro estudio es evaluar la idoneidad de las biopsias obtenidas mediante TS procesadas como muestras histopatológicas para determinaciones de EGFR y ALK.
Incluimos a todos los pacientes con DPM secundario a un cáncer de pulmón diagnosticado entre agosto de 2010 y julio de 2016 que se sometieron a una TS como un procedimiento diagnóstico y/o terapéutico. El DPM se definió como un derrame con células malignas identificadas mediante citología o biopsia pleural. El protocolo del estudio fue aprobado por el comité de ética local y todos los sujetos firmaron el consentimiento informado.
La técnica la realizó un neumólogo con un toracoscopio Olympus LTF-160, en la sala de endoscopias, con guía ecográfica y utilizando anestesia tópica (mepivacaína al 2%) y sedación consciente (midazolam y/o fentanilo). El líquido pleural se aspiró mientras se permitía la entrada de aire en el espacio pleural, que se inspeccionó minuciosamente, tomándose entre 6 y 10 biopsias en la pleura parietal y/o diafragmática, y realizando pleurodesis mediante la instilación de talco pulverizado a través del toracoscopio en los casos indicados. Registramos los hallazgos toracoscópicos, el rendimiento diagnóstico y el resultado del procedimiento. El estatus de la mutación EGFR se determinó mediante PCR y la translocación de ALK mediante FISH. Los resultados se expresaron como porcentajes y frecuencias absolutas para las variables cualitativas y como mediana e intervalo intercuartílico para las numéricas. Los datos se analizaron con SPSS 19.0 (Chicago, IL, EE. UU.)
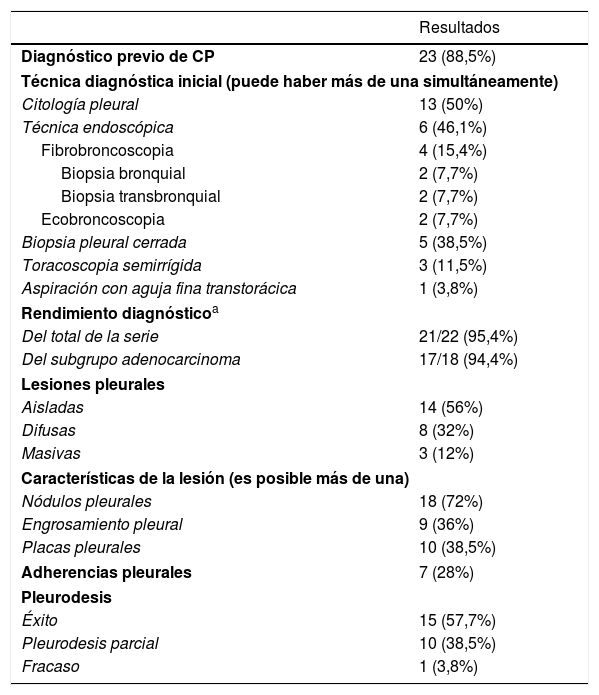
Incluimos nuestros primeros 26 pacientes, 69,2% hombres. La mediana de edad fue 66,5±22,5 años. Siete casos (26,9%) eran fumadores, 10 (38,5%) activos y 9 (34,6%) nunca fumadores. El tipo histológico más prevalente fue el adenocarcinoma, en 22 (84,7%) casos, seguido de 2 tumores indiferenciados (7,7%), un tumor escamoso (3,8%) y un tumor neuroendocrino (3,8%). La tabla 1 muestra otras características de los casos, el rendimiento diagnóstico de la TS y los hallazgos durante el procedimiento.
Características del paciente, tipo histológico, técnica diagnóstica inicial, rendimiento diagnóstico, hallazgos y complicaciones del procedimiento
| Resultados | |
|---|---|
| Diagnóstico previo de CP | 23 (88,5%) |
| Técnica diagnóstica inicial (puede haber más de una simultáneamente) | |
| Citología pleural | 13 (50%) |
| Técnica endoscópica | 6 (46,1%) |
| Fibrobroncoscopia | 4 (15,4%) |
| Biopsia bronquial | 2 (7,7%) |
| Biopsia transbronquial | 2 (7,7%) |
| Ecobroncoscopia | 2 (7,7%) |
| Biopsia pleural cerrada | 5 (38,5%) |
| Toracoscopia semirrígida | 3 (11,5%) |
| Aspiración con aguja fina transtorácica | 1 (3,8%) |
| Rendimiento diagnósticoa | |
| Del total de la serie | 21/22 (95,4%) |
| Del subgrupo adenocarcinoma | 17/18 (94,4%) |
| Lesiones pleurales | |
| Aisladas | 14 (56%) |
| Difusas | 8 (32%) |
| Masivas | 3 (12%) |
| Características de la lesión (es posible más de una) | |
| Nódulos pleurales | 18 (72%) |
| Engrosamiento pleural | 9 (36%) |
| Placas pleurales | 10 (38,5%) |
| Adherencias pleurales | 7 (28%) |
| Pleurodesis | |
| Éxito | 15 (57,7%) |
| Pleurodesis parcial | 10 (38,5%) |
| Fracaso | 1 (3,8%) |
CP: cáncer de pulmón.
No se tomaron biopsias en 4 casos debido a que por su situación funcional y previsible mala tolerancia al procedimiento se realizó una pleuroscopia exclusivamente terapéutica, dado que eran pacientes ya diagnosticados previamente. Una biopsia mostró pleura normal, cuando en realidad era un adenocarcinoma, de acuerdo con estudios previos (el objetivo de la toracoscopia semirrígida en este caso fue la determinación molecular).
Se realizaron pruebas moleculares en 14 adenocarcinomas (tras indicación de oncología), obteniéndose material suficiente y adecuado para determinar el estado de mutación de EGFR en el 100% de los casos y para la translocación de ALK en el 90% de casos (debido a que el material fue insuficiente para determinar la traslocación ALK). La mutación EGFR se encontró en 2 pacientes, mientras que no hubo casos con translocación ALK.
Este estudio muestra que la obtención de muestras con TS es un procedimiento muy útil para determinar la mutación de EGFR y el estado de translocación de ALK en el DPM secundario a cáncer de pulmón. A pesar del tamaño de las muestras nuestros resultados muestran que son suficientes para que un patólogo las interprete correctamente y pueda evaluar el estado de las mutaciones moleculares. Por lo tanto, se recomienda la TS cuando las pruebas anteriores no son diagnósticas, pero también cuando el material es insuficiente para la clasificación histológica o las pruebas moleculares11. Un estudio demuestra que el tamaño de las muestras obtenidas mediante TS es adecuado para la subtipificación patológica, siendo posible el análisis molecular del estado de la mutación EGFR en el 100% de las muestras analizadas, aunque las translocaciones de ALK no se incluyeron12. En nuestro estudio la detección de la mutación EGFR fue posible en todos los casos y el análisis de translocación ALK en todos menos uno. La frecuencia de ambas mutaciones en nuestra muestra se correlaciona con la prevalencia de ambas mutaciones en pacientes con cáncer de pulmón, que es del 5% al 20% para la mutación EGFR e inferior al 5% para la translocación de ALK13.
Una limitación de la TS es la que el fórceps flexible no permite realizar muestras en profundidad que incluyan tejido graso de la pared12. Esto es especialmente importante en el caso de sospecha de mesotelioma pleural. En nuestro estudio la mayor parte de los hallazgos fueron nódulos o masas pleurales, lo que podría aumentar la rentabilidad diagnóstica y minimizar la posibilidad de obtener una biopsia falsamente negativa.
Aunque existe una clara distinción entre la toracoscopia médica y los procedimientos quirúrgicos, considerados una buena opción para establecer el diagnóstico de DPM14 y la toracoscopia rígida con anestesia local y sedación profunda ofrece los mismos resultados siendo una técnica mínimamente invasiva3. Sin embargo, aunque las muestras de biopsia tomadas durante la TS son más pequeñas que las biopsias tomadas con pinzas rígidas, existen estudios que afirman que las biopsias de fórceps pleurales flexibles tienen el mismo potencial diagnóstico que las biopsias obtenidas con pinzas rígidas, resultados similares a los obtenidos en nuestro trabajo15.
Nuestro estudio tiene ciertas limitaciones: el reducido tamaño muestral, que se realizó en un solo centro y que la mayoría de los pacientes se había sometido a procedimientos diagnósticos previos. Esto se explica porque el objetivo en pacientes con cáncer de pulmón es establecer el diagnóstico, la estadificación y el estado molecular con la técnica menos invasiva disponible11.
Dada la importancia creciente de la determinación de mutaciones tales como la del protooncogén ROS1 y la detección de la pareja receptor-ligando PD1-PDL1 inducida, así como la aparición de nuevas determinaciones en un futuro, es necesario desarrollar nuevos estudios encaminados a establecer mejor el papel de la TS como técnica mínimamente invasiva y adecuada para su correcta determinación.
ConclusionesNuestro estudio demuestra que la TS tiene un alto rendimiento diagnóstico, permitiendo, mediante una técnica mínimamente invasiva, muestras adecuadas para detectar mutaciones del EGFR en el 100% de los casos y del ALK en el 90%. También permite realizar pleurodesis cuando se considera necesario.