Un equipo multidisciplinario ha realizado una actualización de recomendaciones en la profilaxis de la enfermedad tromboembólica venosa basándose en las evidencias disponibles actualmente. Se ha abordado la problemática tanto del paciente médico como quirúrgico. Hay que puntualizar que esta Normativa está planteada para su utilización en el ámbito de España y, por lo tanto, debe aplicarse con los fármacos autorizados y las prácticas terapéuticas más aceptadas en este país.
The recommendations on venous thromboprophylaxis have been updated on the basis of current evidence reviewed by a multidisciplinary team. The problem has been approached with regard to its relevance in both surgical and nonsurgical patients. It should be noted that these recommendations were drawn up for use in Spain and, therefore, should be implemented with the drugs and therapeutic practices authorized and generally accepted in this country.
American College of Chest Physicians
Anticoagulantes orales
Artroplastia de cadera
Artroplastia de rodilla
Accidente vascular cerebral agudo
Compresión neumática intermitente
Ensayo clínico aleatorizado
Enfermedad pulmonar obstructiva crónica
Enfermedad tromboembólica venosa
Heparina de bajo peso molecular
Heparina no fraccionada en dosis bajas
Cociente internacional normalizado
Medias de compresión gradual
Miembros inferiores
National Institute for Health and Clinical Excelence
New York Heart Association
Sociedad Española de Neumología y Cirugía Torácica
Tromboembolia pulmonar
Trombosis venosa profunda
La enfermedad tromboembólica venosa (ETV), tanto en su expresión de trombosis venosa profunda como en su complicación más temida, la tromboembolia pulmonar (TEP), constituye un problema sanitario de dimensiones considerables por su impacto en términos de morbimortalidad, coste y consumo de recursos. La mortalidad de la TEP sin tratamiento oscila entre el 13 y el 17%. Datos proporcionados por el Ministerio de Sanidad y Consumo1 desde 1999 hasta 2002 demuestran un aumento paulatino y constante del número de casos diagnosticados de ETV. El porcentaje de ingresos por ETV en los hospitales españoles se acerca al 1% y la tasa de mortalidad intrahospitalaria de esta enfermedad supera el 7%. El aumento de su incidencia condiciona un incremento constante de los costes sanitarios. Se estima que en el año 2002 el coste anual por ingresos hospitalarios relacionados con esta enfermedad fue de 50.484.193 €.
En los grupos de pacientes con factores de riesgo (tabla I), la prevención de la ETV, ya sea mediante medidas farmacológicas o físicas (tabla II), es la mejor estrategia. La profilaxis de ETV se aplica cuando los beneficios superan a los riesgos. Las decisiones de prescripción de profilaxis se toman combinando los conocimientos aportados por la bibliografía, el conocimiento específico de los factores de riesgo de ETV en cada paciente, la posibilidad de consecuencias adversas de la profilaxis y la disponibilidad de las opciones en cada centro sanitario.
Factores de riesgo para la enfermedad tromboembólica venosa
| Cirugía mayor recienteFracturas o inmovilizaciones recientes con escayola de extremidades inferioresInmovilización reciente por enfermedades médicas: insuficiencia cardíaca de grado funcional III-IV de la New York Heart Association, exacerbaciones de EPOC, sepsis, accidente vascular cerebral agudoTrombofilia congénita: déficit de antitrombina, proteína C o proteína S, mutación homocigota o heterocigota del factor V Leiden, déficits combinados, mutación heterocigota del factor II G20210A, hiperhomocisteinemia, aumento de la concentración plasmática de factor VIII, otrasEnfermedad tromboembólica venosa previa, especialmente en las idiopáticasCáncer, especialmente con metástasisSíndrome antifosfolipídicoEdad avanzadaEmbarazo, puerperioObesidadTrombosis venosa superficial, varicesAnticonceptivos orales, tratamiento hormonal sustitutivo, tamoxifenoMiscelánea: policitemia vera, trombocitosis, hemoglobinuria paroxística nocturna, síndrome nefrótico, enfermedad inflamatoria intestinal, síndrome de Behçet, lupus eritematoso, antipsicóticos |
Métodos profilácticos disponibles de la enfermedad tromboembólica venosa
| Métodos farmacológicosHeparinas de bajo peso molecular: bemiparina, dalteparina, enoxaparina, nadroparina, tinzaparinaHeparina no fraccionadaAntivitaminas K: acenocumarol, warfarinaInhibidores indirectos del factor Xa (fondaparinux)Métodos no farmacológicos o físicosCompresión neumática intermitenteMedias de compresión gradualBomba pedia venosa |
Nuestro objetivo es actualizar las mejores evidencias científicas en el uso de medidas preventivas para la ETV, tanto en pacientes médicos como quirúrgicos, y resumir esas evidencias en un documento que sirva de instrumento en la práctica clínica a neumólogos, cirujanos torácicos y cualquier médico especialista o generalista. En el anexo I se resume el método empleado2-5.
Metodología
Se constituyó un grupo de trabajo multidisciplinario, en el que participaron 3 neumólogos, uno de los cuales actuó como coordinador, 2 internistas, un hematólogo, un cirujano de tórax y un experto en metodología de investigación en Ciencias de la Salud.
- 1.
Partimos de 2 documentos básicos: la última guía del American College Chest Physicians (ACCP), basada en la Séptima Conferencia de Consenso sobre tratamiento antitrombótico y trombolítico2, y, en el tema de la profilaxis en pacientes médicos, la guía PRETEMED 20033. Se siguieron los esquemas de clasificación de enfermedades quirúrgicas y situaciones médicas de riesgo recogidas en dichos documentos.
- 2.
Para actualizar las recomendaciones, se realizó una revisión sistemática de la bibliografía publicada desde octubre de 2003 hasta septiembre de 2006. Las preguntas de investigación que se plantearon en la búsqueda bibliográfica estuvieron centradas en el riesgo de enfermedad tromboembólica venosa asociado a cada enfermedad o circunstancia clínica, y en la efectividad de la intervención profiláctica para disminuir el riesgo sin producir efectos adversos mayores. El resultado de la búsqueda fue analizado por pares entre el equipo de trabajo, evaluándose la calidad de la evidencia que aportaban los artículos seleccionados.
Tuvimos que homogeneizar la gradación de la fuerza de las recomendaciones de las 2 guías de práctica clínica que se usaron como documentos de partida y la que generó la síntesis de las evidencias aportadas por la revisión bibliográfica realizada por el grupo de trabajo. Elegimos el criterio seguido por los autores de la guía PRETEMED 2003 y adaptamos a éste las recomendaciones de la guía ACCP para pacientes quirúrgicos y las nuevas evidencias encontradas.
- 3.
Por último, dada la concurrencia de factores de riesgo que particularmente se presentan en el paciente médico, nos pareció interesante añadir la herramienta desarrollada en la guía PRETEMED 2003 sobre la valoración individualizada del paciente.
Redactamos un primer borrador del documento, que fue consensuado por un panel multidisciplinario de revisores externos (anexo II). No se recabó la opinión de pacientes para la elaboración de las recomendaciones recogidas en esta Normativa.
Anexo II.Panel de revisores externos
Dr. Juan Ignacio Arcelus Martínez (Cirugía General. Hospital Universitario Virgen de las Nieves. Granada)Dr. Manuel Arenas Gordillo (Neumología. Hospital de Jerez. Jerez de la Frontera)Dra. Raquel Barba Martín (Medicina Interna. Fundación Hospital de Alcorcón. Madrid)Dra. Ana Blanco Orozco (Cirugía Torácica. Hospital Universitario Virgen del Rocío. Sevilla)Dr. José Blanquer Oliva (Cuidados Intensivos. Hospital Clínico. Valencia)Dr. Miguel Ángel Cabezudo Hernández (Neumología. Hospital Central de Asturias. Oviedo)Dr. Francisco Conget López (Neumología. Hospital Clínico Universitario Lozano Blesa. Zaragoza)Dra. Teresa Elías Hernández (Neumología. Hospital Universitario Virgen del Rocío. Sevilla)Dra. Gemma Iruín Irulegui (Hematología y Hemoterapia. Hospital de Cruces. Barakaldo. Vizcaya)Dr. José Luis Lobo Beristain (Neumología. Hospital de Txagorritxu. Vitoria. Álava)Dr. Juan Vicente Llau Pitarch (Anestesia. Hospital Clínico. Valencia)Dr. Manuel Monreal Bosch (Medicina Interna. Hospital Germans Trias i Pujol. Badalona)Dr. Mikel Oribe Ibáñez (Neumología. Hospital de Galdakao. Vizcaya)Dra. Consolación Rodríguez Matute (Neumología. Hospital San Juan de Dios. Bormujos. Sevilla)Dr. José Antonio Rodríguez Portal (Neumología. Hospital Universitario Virgen del Rocío. Sevilla)Dr. Javier Trujillo Santos (Medicina Interna. Hospital General Santa María del Rosell. Cartagena)Dra. Silvia Vidal Serrano (Agencia de Evaluación de Tecnologías Sanitarias de Andalucía)
La búsqueda bibliográfica se realizó mediante una estrategia específica, utilizando palabras clave para cada enfermedad, en MEDLINE, Embase y Librería Cochrane desde octubre de 2003 hasta septiembre de 2006. También se efectuó una búsqueda manual a partir de los estudios y las guías de práctica clínica encontrados. Los estudios recuperados se analizaron y seleccionaron en función de su capacidad para responder a las preguntas iniciales de investigación (riesgo de enfermedad tromboembólica venosa, efectividad de la intervención y complicaciones de las medidas profilácticas adoptadas).
Calidad metodológicaLa calidad de cada artículo se analizó mediante la lista de comparación propuesta por el National Institute for Health and Clinical Excellence (NICE) para la valoración y lectura crítica de los artículos científicos4, y un método cuantitativo basado en la escala de Jadad5 para publicaciones sobre riesgo e intervenciones. Las escalas permiten puntuar la calidad de la evidencia suministrada por cada artículo de 0 a 7, según la siguiente estratificación: 0-2, baja calidad de evidencia; 3-4, intermedia; 5-6, alta; 7, excelente. La evaluación crítica de los artículos incluidos corrió a cargo de 2 investigadores independientes pertenecientes al equipo de trabajo, y las discrepancias se resolvieron por consenso. Los instrumentos mencionados permiten determinar la validez de un artículo (criterios de extracción de la muestra, recogida prospectiva de datos y verificación del efecto a medir) y determinar su aplicabilidad a cada paciente.
Grado de recomendaciónLa gradación de las recomendaciones de actuación para cada enfermedad se realizó teniendo en cuenta la calidad de la evidencia y el efecto de la intervención en términos de riesgo/beneficio3. De esta forma, cada recomendación puede ubicarse en alguna de las celdas de la siguiente tabla:
| Calidad de la evidencia | Efecto esperado de la intervención (riesgo/beneficio) | |||
| Sustancial | Grande | Pequeño | Nulo | |
| BuenaRegularMalaDesconocida | ABCSin evidencia | ABCSin evidencia | BCDSin evidencia | DDDSin evidencia |
Elaboración y gradación de la fuerza de las recomendaciones: guía PRETEMED 20033.
Se adaptaron las recomendaciones recogidas en la guía ACCP para pacientes quirúrgicos2 a las arriba citadas en función de la calidad de la evidencia y de la información que proporciona la guía. El objeto de esta medida fue homogeneizar el sistema de clasificación de las recomendaciones propuestas. En el anexo III se explican las equivalencias de cada uno de los sistemas de recomendaciones.
Equivalencias entre 2 escalas de grados de recomendación
| Escala ACCP | Relación riesgo-beneficio | Calidad metodológica de los estudios | Implicaciones | Escala de esta normativa |
| 1A | Evidente | ECA sin limitaciones importantes | Recomendación fuerte: puede aplicarse a la mayoría de los pacientes en la mayoría de las circunstancias sin reservas | A |
| 1C+ | Evidente | No hay ECA, pero los resultados de los ECA realizados en otras poblaciones pueden extrapolarse de manera inequívoca o la evidencia de estudios observacionales es aplastante | Recomendación fuerte: puede aplicarse a la mayoría de los pacientes en la mayoría de las circunstancias | A |
| 1B | Evidente | ECA con limitaciones importantes (resultados inconsistentes o defectos metodológicos) | Recomendación fuerte: probablemente pueda aplicarse a la mayoría de los pacientes | B |
| 1C | Evidente | Estudios observacionales | Recomendación de fuerza intermedia | B |
| 2A | No evidente | ECA sin limitaciones importantes | Recomendación de fuerza intermedia | B |
| 2C+ | No evidente | No hay ECA, pero los resultados de otros ECA pueden extrapolarse | Recomendación débil | C |
| 2B | No evidente | ECA con limitaciones importantes | Recomendación débil | C |
| 2C | No evidente | Estudios observacionales | Recomendación muy débil; otras opciones pueden ser igualmente razonables | D |
ACCP: American College of Chest Physicians; ECA: ensayo clínico aleatorizado.
Para la cuantificación del riesgo global en cada paciente médico y la valoración de la indicación de medidas profilácticas en la guía PRETEMED, se desarrolló una escala de riesgo basada en las incidencias o riesgos absolutos de enfermedad tromboembólica venosa para cada factor. La escala de pesos se ajustó tras la validación de las indicaciones de profilaxis realizada por un consenso de expertos3. En el anexo IV se recoge la escala sobre el riesgo de enfermedad tromboembólica venosa en los procesos médicos y las recomendaciones de profilaxis.
| Riesgo de enfermedad tromboembólica venosa (ETV) en procesos médicos y recomendaciones de profilaxis | ||||
| 1 | 2 | 3 | 4 | |
| Procesos médicos | Embarazo/puerperio Paresia grave de MMIIViaje > 6 h | NeoplasiaInsfuciencia cardíaca congestivaInsuficiencia renal crónica, síndrome nefróticoInfección aguda graveTrombofiliaa | EPOC descompensadaAVCA con paresia de MMII | Infarto agudo de miocardio |
| Fármacos | TamoxifenoRaloxifenoTratamiento hormonal sustitutivoAnticonceptivos orales | Quimioterapia | ||
| Procesos locales | Catéter venoso central | TVP-ETV previa Férula/vendaje MMII | ||
| Otros | Edad > 60 añosObesidad (IMC > 28 kg/m2)bTabaquismo > 35 cigarrillos/díabInstitucionalizaciónb | Encamamiento > 4 días | ||
| Cálculo del riesgo | Recomendaciones de profilaxis de la ETV |
| Recomendación | |
| 1-34> 4 | Considerar el uso de medidas físicasMedidas físicas o HBPM (dosis de riesgo moderado) si la puntuación se alcanza con procesos médicos más otras circunstanciasHBPM (dosis de alto riesgo) si la puntuación se alcanza sólo con procesos médicosProfilaxis con HBPM (dosis de alto riesgo)HBPM: heparinas de bajo peso molecular. |
Tomada de Alonso Ortiz del Río et al3.
AVCA: accidente vascular cerebral agudo; IMC: índice de masa corporal; MMII: miembros inferiores; TVP: trombosis venosa profunda.
La mayoría de los ensayos clínicos aleatorizados en pacientes quirúrgicos se ha realizado iniciando la profilaxis preoperatoria 12 h antes de la intervención, que en Europa es la práctica más habitual. No obstante, hay también un número considerable de trabajos realizados con pautas postoperatorias, 12 h después de la intervención, que es la modalidad más aceptada en Norteamérica2. En la actualidad está emergiendo un tercer régimen de profilaxis basado en la proximidad a la cirugía, 2 h antes o 6 h después de la intervención, pues se considera que su administración 12 h antes o después es demasiado distante. Cualquiera de estas opciones puede ser aceptable, aunque antes de instaurar un régimen de profilaxis con un fármaco en concreto hay que basarse en los ensayos clínicos realizados con el medicamento en particular y en la descripción del uso antes o después de la cirugía que se exprese en su ficha técnica.
2.1Riesgos asociados a la anestesia o analgesia neuroaxialAunque el hematoma perirraquídeo es muy poco frecuente tras el bloqueo anestésico/analgésico neuroaxial, su incidencia puede aumentar con el uso de fármacos antitrombóticos, y los efectos de esta complicación pueden ser muy graves6. La Food and Drug Administration (Public Health Advisory, 1997)7 dispone que, para establecer los tiempos óptimos de realización de punciones epidurales, debe considerarse el perfil farmacocinético de cada fármaco. El Ministerio de Sanidad y Consumo de España, en su circular 20607-10/2001 de 11 de octubre, trata sobre el manejo del catéter y el uso de heparina de bajo peso molecular (HBPM). La Sociedad Española de Anestesiología, Reanimación y Terapéutica del Dolor establece los tiempos de seguridad para la realización de una anestesia neuraxial en los pacientes a quienes se administra un fármaco (HBPM o fondaparinux) como profilaxis8. Las recomendaciones básicas son:
- 1.
En pacientes que reciben una HBPM en el preoperatorio el tiempo de seguridad mínimo entre la última dosis de HBPM y la punción neuroaxial, la colocación o la retirada de un catéter se establece en 12 h. Desde cualquiera de estas maniobras hasta la siguiente dosis de HBPM deben transcurrir al menos 6 h.
- 2.
En pacientes que reciben fondaparinux no hay que tomar ninguna precaución especial si se aplica anestesia general o subaracnoidea de punción única. En los casos de colocación de catéter para analgesia postoperatoria, se recomienda un intervalo de 36 h entre la última dosis de fondaparinux y la retirada del catéter (saltando, por tanto, una dosis del fármaco), y esperar 12 h hasta la administración de la siguiente dosis.
- –
Se recomienda la utilización de medidas físicas de profilaxis en pacientes con alto riesgo de hemorragia (A) o como complemento de la profilaxis farmacológica en pacientes de alto riesgo trombótico (B). Se aconseja prestar atención al buen uso y cumplimiento de los dispositivos mecánicos (A).
- –
Se desaconseja el uso de ácido acetilsalicílico como único método de profilaxis (A).
- –
Se debe considerar la insuficiencia renal en la dosificación de la HBPM, fondaparinux, inhibidores directos de la trombina y otros fármacos antitrombóticos, en particular en pacientes ancianos y con riesgo elevado de hemorragia (A).
- –
Se recomienda extremar la precaución al utilizar profilaxis anticoagulante en los pacientes que reciban anestesia o analgesia neuroaxial (A).
- –
En pacientes de cirugía general de bajo riesgo a quienes se realiza un procedimiento menor, que tienen menos de 40 años y carecen de otros factores de riesgo (tabla III), se desaconseja el uso de una profilaxis específica que no sea la movilización precoz y persistente (A).
Tabla III.Niveles de riesgo de enfermedad tromboembólica venosa (ETV) en pacientes quirúrgicos sin profilaxis
Niveles de riesgo Procedimientos Incidencia sin profilaxis (%) TVP distal TVP proximal ETV clínica TEP mortal Bajo Cirugía menor en < 40 años sin factores de riesgo 2 0,4 0,2 0,002 Moderado Cirugía menor más factores de riesgo 10-20 2-4 1-2 0,1-0,4 Cirugía menor en 40-60 años Cirugía mayor en < 40 años sin factores de riesgo Alto Cirugía menor en > 60 años 20-40 4-8 2-4 0,4-1,0 Cirugía mayor en < 40 años Cirugía mayor más factores de riesgo Muy alto Cirugía mayor en > 40 años y ETV previa, neoplasias, hipercoagulabilidad, prótesis o fracturas de cadera o rodilla, traumatismos graves, lesión de médula espinal 40-80 10-20 4-10 0,2-0,5 TEP: tromboembolia pulmonar; TVP: trombosis venosa profunda.
Modificada de: Gallus AS, Salzman EW, Hirsh J. Prevention of VTE. En: Colman RW, Hirsh J, Marder VJ, editors. Haemostasis and thrombosis: basic principles and clinical practice. 3rd ed. Philadelphia: JB Lippincott; 1994. p. 1331-45; Nicolaides AN, Berqvist D, Hull R. Prevention of VTE: international consensus statement. Int Angiol. 1997;16:3-38; Geerts WH, Heit JA, Claset GP. Prevention of venous thromboembolism, Chest. 2001;119 Suppl:132-75.
- –
Los pacientes de riesgo moderado son aquellos que presentan un factor de riesgo para la ETV, tienen entre 40 y 60 años o se someten a un procedimiento menor, o pacientes de menos de 40 años sin factores de riesgo a quienes se realizan intervenciones mayores. Se recomienda profilaxis con HBPM a dosis de alto riesgo (tabla IV) (A). Otra opción es la heparina no fraccionada en dosis bajas (HNFDB), 5.000 U 2 veces al día (A).
Tabla IV.Dosificación de las heparinas de bajo peso molecular según la estratificación de riesgo
Dosis (U/día) Riesgo bajo/moderado Riesgo alto o muy alto Dalteparina: Boxol®, Fragmin® 2.500 5.000 Nadroparina: Fraxiparina® 2.500 < 70 kg: 3.000 > 70 kg: 4.000 Bemiparina: Hibor® 2.500 3.500 Enoxaparina: Clexane®, Decipar® 2.000 4.000 Tinzaparina: Innohep® 3.500 4.500 Modificada de: Navarro JL, García Avelló A, César JM. Heparinas de bajo peso molecular en la profilaxis de la enfermedad tromboembólica en pacientes quirúrgicos y médicos. En: Rocha E, Díaz S, Alegría A, editores. Heparinas de bajo peso molecular. Barcelona: Acción Médica; 2002.
- –
Son pacientes de riesgo alto aquellos a los que se realizan intervenciones menores y tienen más de 60 años, o pacientes que se someten a cirugía mayor con más de 40 años u otros factores de riesgo. Se recomienda profilaxis con HBPM a dosis de alto riesgo (tabla IV) (A). Otra opción es la HNFDB, 5.000 U 3 veces al día (A).
- –
En pacientes de cirugía general de alto riesgo con múltiples factores de riesgo, se recomienda combinar los métodos farmacológicos con el uso de métodos físicos, como medias de compresión gradual (MCG) o compresión neumática intermitente (CNI) (A).
- –
En pacientes de cirugía general con alto riesgo de hemorragia se recomienda el uso de profilaxis mecánica con MCG o CNI al menos hasta que disminuya el riesgo de hemorragia (A).
- –
En pacientes de cirugía general de alto riesgo, como pacientes neoplásicos a quienes se realiza cirugía oncológica, se propone profilaxis después del alta hospitalaria durante 2-3 semanas (B).
- –
En pacientes a quienes se realiza cirugía vascular y que no presentan otros factores de riesgo tromboembólico se propone no utilizar sistemáticamente medidas profilácticas (A).
- –
En pacientes a quienes se realiza cirugía vascular mayor y que presentan otros factores de riesgo tromboembólico se recomienda profilaxis con HBPM o HNFDB (A).
- –
En pacientes a quienes ha de realizarse cirugía ginecológica con procedimientos breves (< 30 min) por una enfermedad benigna, se desaconseja el uso de una profilaxis específica distinta de la movilización precoz y persistente (A).
- –
En pacientes sometidas a procedimientos laparoscópicos que presentan otros factores de riesgo de ETV, se recomienda la profilaxis con una o más de las modalidades siguientes: HBPM, HNFDB, CNI o MCG (A).
- –
Se recomienda tromboprofilaxis para todas las pacientes de cirugía ginecológica mayor (A).
- –
En pacientes con cirugía ginecológica mayor por enfermedad benigna sin factores de riesgo se recomiendan HBPM a dosis de riesgo moderado (tabla IV) (A), o HNFDB, 5.000 U 2 veces al día (A), o CNI iniciada justo antes de la intervención quirúrgica y utilizada continuamente mientras la paciente no camine (B).
- –
En pacientes con cirugía extensa por neoplasia maligna y en aquéllas con otros factores de riesgo, se recomienda profilaxis sistemática con HBPM a dosis de alto riesgo (tabla IV) (A). Opciones alternativas son: HNFDB, 5.000 U 3 veces al día (A); CNI sola hasta el alta hospitalaria (A), o combinación de HBPM o HNFDB más profilaxis mecánica con MCG o CNI (B).
- –
En pacientes a quienes se practican procedimientos transuretrales u otros procedimientos urológicos de bajo riesgo, se desaconseja el uso de profilaxis específica distinta de la movilización precoz y persistente (A).
- –
En pacientes con procedimientos urológicos abiertos mayores, se recomienda la profilaxis sistemática con HBPM (A). Otras opciones son: HNFDB 2 o 3 veces al día (A), CNI o MCG (B). En pacientes con cirugía urológica que tienen hemorragia activa o un riesgo muy elevado de presentarla, se recomienda el uso de profilaxis mecánica con MCG o CNI, al menos hasta que disminuya el riesgo de hemorragia (A).
- –
En los pacientes con múltiples factores de riesgo se recomienda la combinación de MCG o CNI con HBPM o HNFDB (A).
- –
En estos pacientes se desaconseja una profilaxis sistemática distinta de la movilización intensiva (A).
- –
En pacientes con factores de riesgo para ETV se recomienda el uso de profilaxis con una o más de las modalidades siguientes: HBPM, HNFDB, CNI o MCG (A).
- –
La utilización de anticoagulantes orales (ACO), warfarina o acenocumarol en la profilaxis antitrombótica en cirugía ortopédica está muy extendida en EE.UU., pero en Europa, y concretamente en España, es excepcional. No se utilizan porque su inicio de acción es tardío y la respuesta varía dependiendo de múltiples factores como la medicación concomitante, por lo que se requiere seguimiento frecuente. Además, en ningún ensayo clínico aleatorizado se ha demostrado la superioridad de los ACO respecto a otros fármacos anticoagulantes. Todo lo anterior, junto con la falta de formación, de experiencia clínica y de guías sobre su utilización en España, hace que desaconsejemos su empleo de forma sistemática. Por lo tanto, no se realizarán recomendaciones sobre su utilización en esta Normativa. No obstante, los ACO con un cociente internacional normalizado (INR) de 2-3 pueden emplearse en casos especiales de contraindicación a los otros fármacos anticoagulantes disponibles.
- –
Los inhibidores directos de la trombina (ximelagatrán-melagatrán) han demostrado ser eficaces en la profilaxis antitrombótica. Sin embargo, su utilización no está aprobada en España. Por lo tanto, no se realizarán recomendaciones sobre su empleo en esta Normativa.
La cirugía ortopédica comprende la artroplastia de cadera (ATC), artroplastia de rodilla (ATR) y cirugía por fractura de cadera. La incidencia de trombosis venosa profunda sin profilaxis oscila entre el 40 y el 60%, y el 10-30% corresponde a trombosis venosa profunda proximal. Respecto a la incidencia de TEP, se ha descrito que el 3-28% de los pacientes presenta TEP en las gammagrafías practicadas en las 2 semanas siguientes de la cirugía9,10. Por ello la profilaxis en este tipo de cirugía está sistemáticamente establecida.
2.1.1.6.2Recomendaciones- –
En pacientes con ATC se recomienda alguna de las pautas siguientes: a) HBPM en dosis de alto riesgo, iniciada 12 h antes de la intervención o 12-24 h después de ésta, o bien 4-6 h después de la cirugía a la mitad de la dosis de alto riesgo, para aumentarla a dosis plena al día siguiente (A), o b) fondaparinux a dosis de 2,5 mg/día, iniciado 6-8 h después de la intervención (A).
- –
Se desaconseja el uso de dextrano, HNFDB, MCG, CNI o bomba pedia venosa como único método de profilaxis en pacientes con ATC (A).
- –
En pacientes con ATR se recomienda profilaxis con HBPM a dosis de alto riesgo o fondaparinux (A).
- –
El uso óptimo de la CNI constituye una opción alternativa a la profilaxis anticoagulante (B) en pacientes con ATR.
- –
En pacientes con ATR se desaconseja el uso de cualquiera de las modalidades siguientes como único método de profilaxis: HNFDB (A) y bomba pedia venosa (B).
- –
En pacientes con cirugía por fractura de cadera se recomienda el uso sistemático de fondaparinux (A), HBPM a dosis de alto riesgo (A) o HNFDB (B).
- –
Se recomienda la profilaxis mecánica si la profilaxis anticoagulante está contraindicada por un riesgo elevado de hemorragia (A).
- –
En los procedimientos quirúrgicos ortopédicos se recomienda basar la decisión del comienzo de la profilaxis farmacológica en la relación entre eficacia y riesgo hemorrágico de cada fármaco (A). En el caso de la HBPM el comienzo antes o después de la intervención son opciones igualmente admisibles (A).
- –
La profilaxis debe prolongarse al menos 10 días en pacientes con ATC, ATR o cirugía por fractura de cadera empleando HBPM a dosis de alto riesgo o fondaparinux a dosis de 2,5 mg/día (A).
- –
Se recomienda que se mantenga hasta 28-35 días tras la intervención ortopédica mayor con HBPM (A) y hasta 21 días con fondaparinux (B).
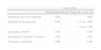
Riesgo absoluto de trombosis venosa profunda (TVP) en pacientes hospitalizados*
| Grupos de pacientes | Prevalencia de TVP (%) |
| Pacientes médicos | 10-20 |
| Cirugía general | 15-40 |
| Cirugía mayor ginecológica | 15-40 |
| Cirugía mayor urológica | 15-40 |
| Neurocirugía | 15-40 |
| Accidente vascular cerebral | 20-50 |
| Cirugía ortopédica | 40-60 |
| Traumatismo grave | 40-80 |
| Lesión medular aguda | 60-80 |
| Pacientes críticos | 10-80 |
Modificada de: Geerts WH, Pineo GF, Heit JA, Bergqvist D, Lassen MR, Colwell CW, et al. Prevention of venous thromboembolism. The Seventh ACCP Conference on Antithrombotic and Thrombolytic Therapy. Chest. 2004;126:338S-400S.
- –
En la artroscopia de rodilla se propone que no se utilice otro método profiláctico que no sea la movilización precoz (C).
- –
En la artroscopia de rodilla se propone, cuando coexisten factores de riesgo o después de un procedimiento prolongado, profilaxis con HBPM (C).
- –
En pacientes intervenidos de columna vertebral sin factores de riesgo se desestima el uso de otro método profiláctico que no sea la movilización precoz y persistente (B).
- –
Se recomienda utilizar alguna forma de profilaxis ante factores de riesgo (B). Las opciones son: HNFDB postoperatoria sola (A); HBPM postoperatoria sola (B), o bien CNI perioperatoria sola (B), MCG perioperatoria sola (C) o CNI perioperatoria combinada con MCG (D). En pacientes con múltiples factores de riesgo se recomienda la combinación de HBPM o HNFDB con MCG o CNI (A).
- –
Se propone que no se use de forma sistemática profilaxis en los pacientes con lesiones aisladas en extremidades inferiores (B).
- –
Se recomienda profilaxis con HBPM si hay otros factores de riesgo añadidos (consenso).
- –
Todos los pacientes con traumatismo y al menos un factor de riesgo deben recibir profilaxis (A).
- –
En ausencia de contraindicaciones, la administración de HBPM debe comenzarse lo antes posible (B).
- –
Si la HBPM está contraindicada por hemorragia activa o alto riesgo de hemorragia, se recomienda el uso de CNI o MCG (B).
- –
Se recomienda el mantenimiento de la profilaxis hasta el alta hospitalaria (A). Después de ésta se recomienda mantener la profilaxis con HBPM o, alternativamente, ACO con INR entre 2 y 3 en los pacientes con dificultad para administrar HBPM (D).
- –
Se recomienda administrar profilaxis a todos los pacientes con lesión medular aguda (A).
- –
Se desaconseja el uso de HNFDB, MCG o CNI como modalidades profilácticas aisladas (A).
- –
Se recomienda la profilaxis con HBPM (B). Alternativas: CNI y HNFDB (C).
- –
Durante la fase de rehabilitación, tras una lesión aguda medular, se recomienda continuar la profilaxis con HBPM o pasar a ACO con un INR de 2-3 (B).
- –
Se recomienda que los pacientes quemados que presenten otros factores de riesgo reciban profilaxis (A).
- –
Si no hay contraindicaciones, se recomienda el uso de HBPM o HNFDB (A).
- –
Se recomienda utilizar sistemáticamente profilaxis en pacientes con neurocirugía mayor (A).
- –
Se recomienda el uso de CNI con o sin MCG en pacientes con neurocirugía intracraneal (A). Alternativas: HBPM (B) o HNFDB (C) postoperatoria.
- –
Se propone la combinación de métodos mecánicos y farmacológicos en los pacientes de alto riesgo (C).
Actualmente del 50 al 70% de los eventos trombóticos sintomáticos11 y del 70 al 80% de TEP mortales12 aparecen en pacientes con enfermedad médica. Además, los eventos tromboembólicos en pacientes médicos están asociados a más complicaciones, en términos de recurrencias, muertes debidas a TEP y complicaciones hemorrágicas, que en los pacientes con enfermedad quirúrgica13.
La mayoría de los trabajos que han investigado los factores de riesgo en pacientes con enfermedad médica se han realizado en pacientes hospitalizados14. Los principales factores de riesgo identificados fueron: insuficiencia cardíaca de grados funcionales III-IV de la New York Heart Association (NYHA), exacerbaciones de enfermedad pulmonar obstructiva crónica (EPOC), sepsis, edad avanzada, historia previa de ETV, cáncer, accidente vascular cerebral agudo (AVCA) con paresia en extremidades inferiores y encamamiento15,16.
Varios ensayos clínicos aleatorizados han demostrado la eficacia de la profilaxis, bien con HBPM o con HNFDB17,18, frente a placebo. Las dosis de HBPM profilácticas en pacientes médicos son las equivalentes a las de pacientes quirúrgicos de riesgo moderado-alto14. Las HBPM, cuando se han comparado con la HNFDB, han sido igual de eficaces y más seguras19. El fondaparinux a dosis de 2,5 mg/día ha demostrado su eficacia en la profilaxis de pacientes médicos frente a placebo20.
Se desconoce cuál es la duración óptima de la profilaxis en estos pacientes. Probablemente los resultados del ensayo clínico EXCLAIM podrán aclarar algunos aspectos de esta cuestión21.
3.2Recomendaciones- –
En pacientes con enfermedad médica ingresados en un hospital con insuficiencia cardíaca congestiva, enfermedad respiratoria grave y encamados con otros factores de riesgo, como cáncer, historia previa de ETV, sepsis, enfermedad neurológica aguda o enfermedad inflamatoria intestinal, se recomienda el uso de profilaxis con HBPM a dosis de alto riesgo (tabla IV) (A). Otra opción es la HNFDB.
- –
En pacientes médicos con riesgo elevado de ETV y en los que esté contraindicado el uso de anticoagulantes, se recomienda aplicar medidas físicas de profilaxis, MCG o CNI (A).
- –
Se recomienda profilaxis en pacientes con cáncer hospitalizados que estén encamados con una enfermedad médica aguda (A).
- –
Los pacientes con neoplasias que deban ser intervenidos quirúrgicamente tendrán que recibir profilaxis según su valoración de riesgo como pacientes quirúrgicos (A).
- –
No se recomienda la profilaxis con HBPM a dosis bajas (A).
- –
No está justificada sistemáticamente la profilaxis de ETV en pacientes neoplásicos no hospitalizados (B).
- –
No se recomienda profilaxis ni con HBPM ni con warfarina en pacientes neoplásicos con catéter venoso central, para evitar la trombosis del catéter (C).
- –
Se recomienda profilaxis con HBPM en pacientes neoplásicos sin quimioterapia si hay encamamiento o una combinación de enfermedades o factores de riesgo (consenso).
Incurriríamos en una incoherencia si recomendáramos el uso profiláctico con HBPM en la fase aguda del infarto agudo de miocardio, cuando el manejo actual del infarto agudo de miocardio comprende trombolíticos y HBPM a dosis de anticoagulación.
3.2.3Insuficiencia cardíaca- –
Se recomienda profilaxis con HBPM a dosis altas (tabla IV) en pacientes hospitalizados por insuficiencia cardíaca congestiva mientras persista el encamamiento (A). Otras opciones: fondaparinux a dosis de 2,5 mg/día.
- –
No se recomienda profilaxis con HBPM a dosis bajas (A).
- –
No está justificada la profilaxis sistemática en pacientes con insuficiencia cardíaca congestiva (B).
- –
Si el paciente no está encamado, se recomienda HBPM en mayores de 60 años con algún otro factor de riesgo asociado, y en menores de 60 años si coexiste alguna circunstancia patológica (consenso).
- –
Se recomienda profilaxis con HBPM en pacientes con EPOC hospitalizados mientras estén encamados (A). Otras opciones: fondaparinux a dosis de 2,5 mg/día.
- –
No se recomienda la profilaxis con HBPM a dosis bajas (A).
- –
En pacientes en los que esté contraindicada la anticoagulación, se recomienda el uso de medidas físicas como MCG o CNI (A).
- –
Se recomienda la profilaxis con HBPM a dosis altas en pacientes hospitalizados por infección aguda mientras persista el encamamiento (A). Otras opciones: fondaparinux a dosis de 2,5 mg/día.
- –
No se recomienda profilaxis con HBPM a dosis bajas (A).
- –
Si el paciente no está encamado, se recomienda HBPM en mayores de 60 años con algún otro factor de riesgo asociado, y en menores de 60 años si coexiste alguna circunstancia patológica (consenso).
- –
Está recomendado el uso de HBPM durante 2 semanas en la fase aguda del AVCA en pacientes con bajo riesgo de hemorragia intracraneal (A).
- –
Se recomienda profilaxis con HBPM en todos los pacientes con AVCA durante el período de hospitalización (consenso).
- –
Se recomienda profilaxis con HBPM cuando hay paresia de extremidades inferiores como secuela de un AVCA, siempre que se asocie con otro factor de riesgo (consenso).
- –
Se recomienda la profilaxis con HBPM a dosis altas (tabla IV) en embarazadas con riesgo elevado de ETV (B).
- –
Se recomienda profilaxis con HBPM en embarazadas si están encamadas y coexiste otro factor de riesgo, cuando haya 2 circunstancias patológicas o una sola circunstancia patológica se asocie a un factor de riesgo de ETV (consenso).
- –
Se recomienda HBPM o medidas físicas si están encamadas y son obesas, sin otros factores de riesgo, o embarazadas no obesas con una circunstancia menor (consenso).
- –
En embarazadas con trombofilia sin ETV previa se recomienda la consulta con un especialista para evaluar el riesgo, dada la heterogeneidad de las distintas trombofilias (consenso).
A pesar de la controversia suscitada en torno al riesgo de una mayor incidencia de ETV en viajes de larga distancia en avión, las cifras son de una TEP por 700.000 pasajeros que viajen más de 6 h y de una por 100 millones que viajen durante menos de 6 h22. La mayoría de las personas que tuvieron episodios de ETV presentaban también uno o más factores de riesgo, por lo que la relación causal o el papel aditivo del viaje no están claros. Habría que delimitar otras circunstancias que concurren en el propio viaje: la inmovilidad, la compresión venosa, la deshidratación o los cambios de presión en la cabina del avión. Estudios realizados para hallar eventos trombóticos asintomáticos encontraron una incidencia del 1-2,2%23,24.
Se han realizado 6 ensayos clínicos2 con MCG, 2 con enoxaparina a dosis de 40 mg/día y uno con 400 mg de ácido acetilsalicílico. Con respecto a los estudios que utilizaron las MCG, a pesar de las limitaciones metodológicas, la suma de eventos trombóticos entre los pasajeros que no las usaron representó el 3,7%, y entre los que las usaron, el 0,2%. La toma de enoxaparina de 2 a 4 h antes del viaje eliminó la incidencia de eventos trombóticos en 184 pasajeros; sin embargo, la utilización de aspirina25 12 h antes del viaje y durante 3 días después de éste no fue protectora.
- –
Se recomienda a los viajeros de larga distancia (> 6 h) que eviten llevar ropas ajustadas alrededor de las extremidades y la cintura, prevengan la deshidratación y realicen estiramientos frecuentes de la pantorrilla (B).
- –
Si el viajero presenta factores de riesgo adicionales, se recomiendan MCG con presión en la rodilla de 15-30 mmHg o una dosis única de HBPM a dosis altas inyectada antes de la salida (tabla IV) (C).
- –
No se recomienda el uso de ácido acetilsalicílico para la prevención de la ETV asociada a los viajes (B).
Los autores son un grupo de trabajo nombrado por la coordinadora, nombrada a su vez por la Sociedad Española de Neumología y Cirugía Torácica (SEPAR). Los Dres. Medrano, Calderón, Uresandi y Otero participaron en la elaboración bien como autores o como miembros del panel externo de la guía PRETEMED 2003, patrocinada por Aventis, SA. Ninguno de los autores tuvo conflictos de interés ni relación comercial o dependencia por este patrocinio. La presente Normativa tuvo el apoyo técnico de SEPAR y no ha contado con el patrocinio de industrias farmacéuticas.
- Home
- All contents
- Publish your article
- About the journal
- Metrics