Introducción
Desde la década de los cincuenta se conocen descripciones bibliográficas de la asociación entre enfermedades pulmonares y enfermedades inflamatorias intestinales (EII), en particular, la colitis ulcerosa (CU) y la enfermedad de Crohn (EC)1. Fue en 1976 cuando Kraft et al2 describieron en 6 pacientes la presencia de supuraciones bronquiales crónicas que habían aparecido entre 3 y 13 años después del inicio de la EII. A partir de entonces quedaron definidas como manifestaciones pulmonares de las EII todas aquellas afecciones respiratorias que no pudieran explicarse por otra causa.
Las manifestaciones extraintestinales de la EII se han descrito en casi todos los órganos de la economía. Su incidencia, que oscila entre el 21 y el 41%, aumentan con la duración de la enfermedad intestinal y son más frecuentes en la EC que en la CU3. La coincidencia de más de una manifestación extraintestinal en un mismo individuo con EII es mayor que lo esperado debido al azar, lo que ha llevado a plantear que podrían tener mecanismos patogénicos comunes4. Greenstein et al5 distinguen 3 grupos de manifestaciones extraintestinales: a) las que se asocian al proceso inflamatorio de la EII y pueden responder al tratamiento de ésta; b) las que persisten aunque la EII no esté presente, y c) las que responden a mecanismos inespecíficos (menos frecuentes).
En España la incidencia de la EII ha ido aumentando en los últimos 30 años con los cambios en el nivel de vida. Hoy día se considera una enfermedad de los países industrializados. Se calcula que actualmente 65.000 españoles presentan esta enfermedad, pero esta cifra podría triplicarse en 10 años. En 1990 Hinojosa et al6 comunicaron una incidencia y una prevalencia globales de 9,07/100.000 y 28,87/100.000, respectivamente. En 1992, el grupo catalán de EII7 publicó una revisión realizada entre 1978 y 1987 con una prevalencia de 19/100.000 en Barcelona y 18/100.000 en Gerona.
En los últimos 10 años se han producido muchos avances en el conocimiento de la contribución genética a la EII. El predominio étnico (judíos askenazíes), la mayor frecuencia entre miembros de una misma familia y la mayor concordancia entre gemelos monocigóticos son 3 pruebas evidentes del papel central de los factores genéticos en la patogenia de la enfermedad. Recientemente el mapeo detallado del cromosoma 16 ha permitido el hallazgo de un gen que codifica para una proteína citoplásmica designada como NOD2, también conocida como CARD15. Esta proteína, que se expresa en los macrófagos, constituye un descubrimiento muy importante para el conocimiento de la enfermedad8.
Manifestaciones pulmonares
La afectación pulmonar constituye la manifestación extraintestinal menos frecuente de la EII, pero es probable que su prevalencia real sea desconocida. Por otro lado, el deterioro pulmonar, al contrario de lo que sucede con el resto de las manifestaciones extraintestinales, se asocia más a la CU que a la EC.
Storch et al9 revisaron 400 casos, de los que 150 ha-bían tenido enfermedad pulmonar activa y un número mayor sólo había presentado manifestaciones subclínicas. Esta revisión, además de realizar una descripción y clasificación por patrones de las enfermedades encontradas, contiene una lista muy completa de estudios que comprenden todos los diagnósticos diferenciales (tabla I). Entre las enfermedades que se pueden confundir, la sarcoidosis y la enfermedad de Wegener, ambas granulomatosas, pueden coincidir con la EII. Se ha postulado que la infección por micobacterias atípicas pudiera contribuir a la formación de granulomas en la EC y sarcoidosis. Estas micobacterias se han detectado en tejidos de pacientes con ambas enfermedades. También la reacción de Kveim puede ser positiva o negativa en ambas, mientras que la enzima de conversión de la angiotensina puede ser elevada en la sarcoidosis pero no en la EC. Los anticuerpos anticitoplásmicos de los neutrófilos y aquellos con un patrón perinuclear específico inducen a pensar en mecanismos autoinmunitarios comunes con la enfermedad de Wegener.
Mahadeva et al10 estudiaron la relación entre los acontecimientos clínicos, los fisiológicos y los hallazgos en la tomografía axial computarizada de alta resolución (TACAR) torácica en 17 pacientes con EII (14 con CU y 3 con EC) que presentaron manifestaciones pulmonares sin causa que lo justificase. En 7 de ellos se había realizado colectomía por enfermedad grave. La disnea fue el síntoma predominante, independientemente del tipo de enfermedad. También la hipersecreción bronquial se presentaba en algunos pacientes. La función pulmonar fue normal en 6, a pesar de que presentaban signos de atrapamiento aéreo en el estudio radiológico. Trece tenían bronquiectasias evidentes en la TACAR torácica, 9 mostraban signos de atrapamiento aéreo, 5 tenían imagen de "árbol en brote" y 2 presentaban cambios indicativos de fibrosis. Un solo paciente no mostraba alteraciones, aunque refería haber sido diagnosticado de una alveolitis comprobada histológicamente 14 años antes, tratada con buena respuesta a los corticoides. En este trabajo la TACAR junto con el estudio de la función pulmonar permitió detectar tempranamente la afección respiratoria.
Es probable que la dificultad en el diagnóstico de las enfermedades pulmonares asociadas a la EII se deba fundamentalmente a 2 razones: por un lado, las manifestaciones extraintestinales pueden presentarse sin coincidir con el comienzo de la enfermedad intestinal, por lo cual el médico no las relaciona con la enfermedad de base. Por otra parte, pueden ser hallazgos subclínicos, por lo que el paciente no los nota, no refiere síntomas y, por lo tanto, el médico no las investiga. Esta situación sólo puede modificarse si el médico tiene presente esta posible asociación y, como consecuencia, orienta la búsqueda diagnóstica.
Los medicamentos utilizados en el tratamiento de la EII (sulfasalacina, mesalamina, infliximab y metotrexato) pueden inducir enfermedades pulmonares como efectos secundarios. Pueden ser muy graves y/o semejantes a algunas de las enfermedades pulmonares asociadas a la EII. Es necesario diagnosticarlas tempranamente, ya que mejoran con la suspensión del fármaco implicado y pueden responder al tratamiento con corticoides9.
Manifestaciones pulmonares en la enfermedad inflamatoria intestinal (tabla II)
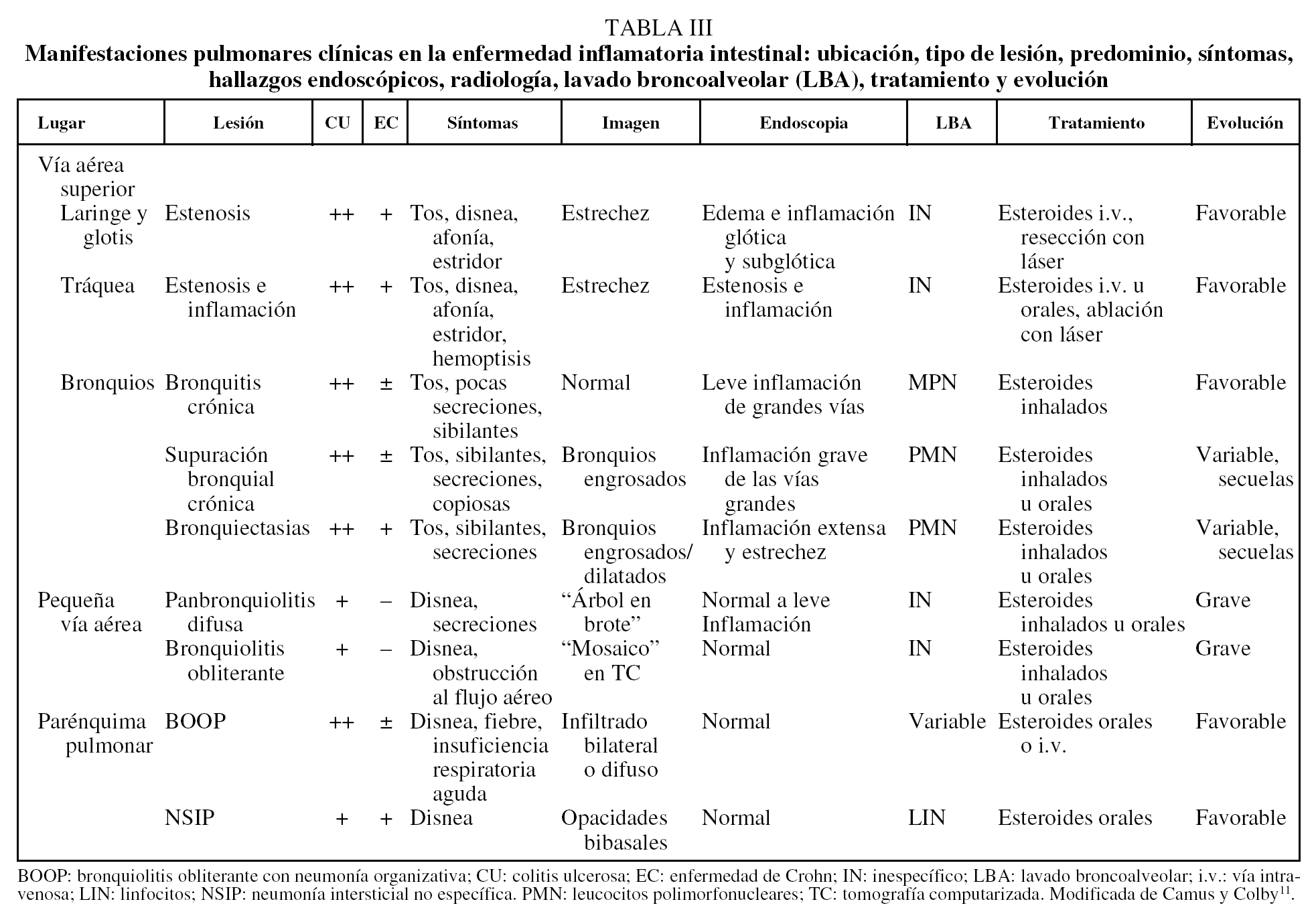
Clínicas. Camus y Colby11 describieron exhaustivamente todas las manifestaciones pulmonares (tabla III). En general, los síntomas más destacados son la tos, la expectoración y la disnea, a las que se puede agregar disfonía o estridor si la lesión se encuentra en las vías altas, o bien neumotórax, neumomediastino u obstrucción importante si se halla en la pequeña vía aérea. En muy pocas situaciones se ha descrito también hemoptisis. Curiosamente, si bien se trata de un mecanismo inflamatorio, la respuesta bronquial a la metacolina por lo general es normal, y la prueba broncodilatadora con agonistas betamiméticos inhalados no es significativa. La radiología puede ser normal o mostrar estrechez de la tráquea, cuando ésta es la afectada, o bien engrosamientos bronquiales como en las supuraciones bronquiales crónicas. Con relativa frecuencia, mediante la TACAR torácica se pueden diagnosticar bronquiectasias no visibles en la radiología convencional. El lavado broncoalveolar ofrece resultados variables, con presencia de leucocitos polimorfonucleares, linfocitos o inespecífico.
Se comentan a continuación las afecciones:
Enfermedades de las vías aéreas superiores. Se han descrito estenosis glótica y subglótica de la laringe12, así como estenosis de la tráquea13, en las cuales se observaba la presencia de un tejido friable y hemorrágico que obstruía la vía aérea, durante la valoración endoscópica. El análisis histológico de estas zonas confirmó que se trataba de un proceso inflamatorio con presencia de células plasmáticas, linfocitos y neutrófilos. Los pacientes presentaban estridor y disnea como síntomas principales. En algunos casos el proceso respiratorio se asociaba a hipoderma gangrenoso, episcleritis y úlceras bucales. Los pacientes respondieron al tratamiento con glucocorticoides y en algún caso la obstrucción requirió tratamiento con láser13-15.
Enfermedades de las vías aéreas inferiores. Para Storch et al9 las bronquiectasias constituyen la entidad más frecuentemente comunicada en asociación a EII. Mahadeva et al10 encontraron bronquiectasias en 13 de 17 pacientes estudiados. Por su parte, Camus et al13 describieron bronquiectasias en 6 de 15 pacientes con compromiso de las vías aéreas superiores, siendo, junto con las bronquitis crónicas, las más frecuentes. Las manifestaciones pulmonares se habían iniciado en un 85% después de haberse realizado el diagnóstico de EII. En un 79% de los casos la enfermedad pulmonar se presentó cuando la EII estaba en fase inactiva como respuesta al tratamiento médico o quirúrgico (colectomía). En un 5% de los casos ambas enfermedades, la pulmonar y la digestiva, se presentaron de forma concomitante. La broncoscopia mostraba tejido de aspecto inflamatorio, y la biopsia realizada en 12 de los 13 confirmó igualmente la presencia de linfocitos y células plasmáticas en la submucosa, con metaplasia escamosa a veces infiltrada por neutrófilos en la mucosa. Los autores comentan que estos hallazgos endoscópicos e histológicos son inusuales y que hay una semejanza histológica entre las vías aéreas y el colon, especialmente en relación con el infiltrado neutrofílico, la ulceración mucosa y la inflamación crónica subyacente con células plasmáticas. El cultivo de esputo no aportaba datos de valor significativo. Se trataba de pacientes no fumadores y sin antecedentes patológicos respiratorios previos, que presentaban tos y expectoración mucopurulenta en cantidades abundantes16 y que no respondían a los antibióticos, pero sí a los corticoides inhalados o sistémicos13,17-20.
Como ya se ha comentado, la bronquitis crónica es la segunda entidad en frecuencia asociada a la EII. Se diferencia de las supuraciones pulmonares en la cantidad de esputo purulento producido, y de las bronquiectasias en que, además de la tos y la cantidad de secreciones, las últimas se visualizan con dilataciones bronquiales en la TACAR torácica13.
Camus et al13 comentan que, al igual que en las bronquiectasias, no había antecedentes de tabaquismo en estos pacientes, y tampoco exacerbaciones paralelas de síntomas bronquiales e intestinales; los hallazgos histológicos y la respuesta a corticoides les inducen a pensar que existe una relación entre la inflamación bronquial y la EII.
Enfermedad de la pequeña vía aérea. La evolución natural de estas lesiones puede causar daños irreversibles7. En algunos casos se producen patrones de panbronquiolitis difusa, cuadro específico que se describió originalmente en asiáticos21-23. Estas enfermedades, al igual que casi todas las respiratorias asociadas, responden a los corticoides enterales, parenterales o inhalados.
La panbronquiolitis, la bronquiolitis necrosante y la bronquiolitis granulomatosa se han descrito en algunos pocos casos. Son enfermedades de la pequeña vía aérea, que se han comprobado por biopsias en algunos casos, pero también se han descrito alteraciones funcionales compatibles con enfermedad de esta pequeña vía, sin hallazgo definitivo en la histología.
Enfermedades del parénquima pulmonar. En estos casos el síntoma predominante es la disnea. El cuadro más común es la bronquiolitis obliterante con neumonía organizativa15,24, que se suele presentar con fiebre, compromiso del estado general y en ocasiones dolor torácico. Se acompaña de opacidades radiológicas únicas o múltiples. En algunas ocasiones está indicada la biopsia para llegar al diagnóstico.
Otras formas de enfermedades intersticiales son poco frecuentes. Se ha descrito la formación de nódulos necrobióticos estériles13 y de infiltrados periféricos con eosinofilia13. Fármacos como la sulfasalacina o la mesalamina pueden ocasionar cuadros similares.
Subclínicas. La aparición de técnicas de mayor complejidad ha permitido el hallazgo de indicadores subclínicos de enfermedad respiratoria en pacientes aún asintomáticos:
Esputo inducido. Fireman et al25 estudiaron el compromiso pulmonar a través del esputo inducido en 24 pacientes con EC y 9 controles sanos. Los primeros tenían diferentes grados de actividad de la enfermedad, carecían de síntomas respiratorios y las pruebas de función pulmonar eran normales. La población celular en el esputo inducido del grupo con EC mostró un porcentaje de linfocitos más elevado que en el grupo control. En cambio, no había diferencias en el recuento de eosinófilos. Dos tercios de los pacientes tenían una acumulación de células CD4+ (7,7 ± 2,5 de CD4/CD8). Los resultados de este estudio fueron similares a los obtenidos por Bonniere et al26, quienes utilizaron el lavado broncoalveolar en 22 pacientes con EC, sin síntomas respiratorios, y observaron que un 54% tenía una relación anormal en las subpoblaciones CD4/CD8.
Óxido nítrico. El óxido nítrico es un mediador de la inflamación en varios procesos patológicos. Se encuentra elevado en el aire exhalado (NOe) de pacientes asmáticos en relación con voluntarios sanos y también en el gas colónico aspirado de pacientes con EC. Con estos antecedentes, Koek et al27 realizaron un estudio en 31 pacientes con EC y 24 con CU, con el objetivo de evaluar si el NOe estaba elevado en pacientes con EII activa. Además investigaron si existía correlación entre: a) los valores de NOe y la actividad de la EII, y b) entre la espirometría y actividad de la EII en un subgrupo. Los autores encontraron que el NOe estaba elevado en la EII activa y, además, observaron una correlación negativa entre los valores espirométricos y la actividad de la enfermedad en pacientes con EC.
Hiperreactividad bronquial. Ceyhan et al28 estudiaron a 30 pacientes con EII (19 con CU y 11 con EC) y 16 controles, en los cuales investigaron el estado atópico por pruebas cutáneas, la existencia de hiperreactividad bronquial a través de broncoprovocación con metacolina y la prevalencia de pruebas funcionales respiratorias anormales. Los resultados mostraron que los síntomas de alergia, las pruebas cutáneas positivas y las pruebas funcionales anormales fueron significativamente más prevalentes en los pacientes con EII. En cambio, la hiperreactividad bronquial no fue más prevalente en un grupo que en otro.
Por su parte, Herrlinger et al29 investigaron a 66 pacientes con EII (31 con CU y 35 con EC) y 30 controles, a los que efectuaron las siguientes pruebas de función pulmonar: volumen espiratorio forzado en el primer segundo, capacidad vital inspiratoria, índice volumen espiratorio forzado en el primer segundo/capacidad vital inspiratoria y capacidad de transferencia de monóxido de carbono. A su vez evaluaron el grado de actividad de la EII. Los resultados mostraron que tanto en la CU como en la EC las pruebas de función pulmonar estaban significativamente disminuidas en relación con el grupo control. No se observaron diferencias significativas entre ambas entidades. La incapacidad era más pronunciada cuando había actividad de la EII que cuando no la había.
Patogenia
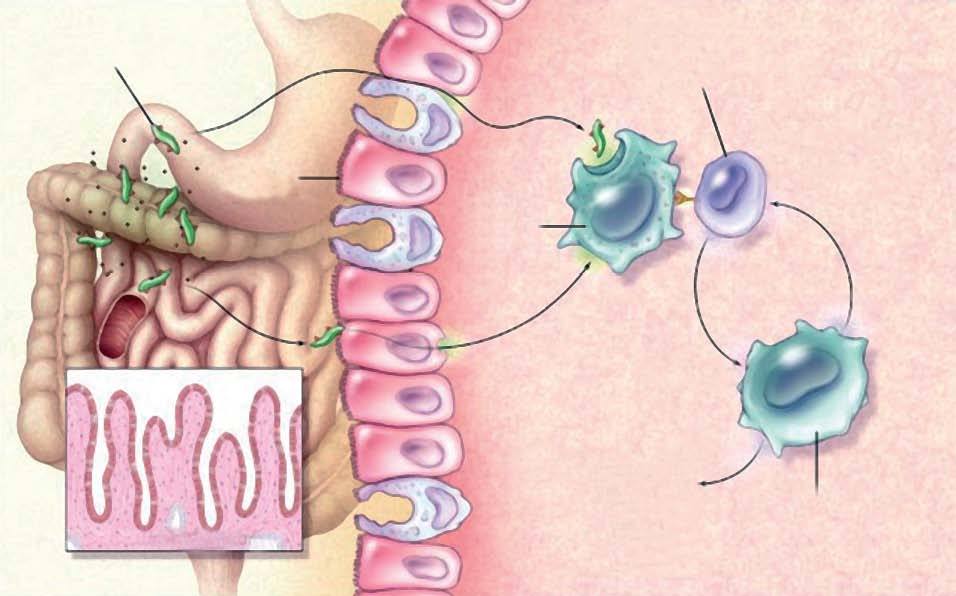
La patogenia de la EII sólo se conoce parcialmente. Se piensa que es el resultado de la activación inadecuada y recurrente del sistema inmunitario de la mucosa, activado por la presencia de la flora luminal normal30. Como ya se ha comentado previamente, sin duda los factores genéticos contribuyen a la susceptibilidad de la EII. Sin embargo, estudios en gemelos idénticos, en los cuales sólo el 45% de los pares de locus genéticos eran concordantes con EC, llevaron a pensar que el desarrollo de la enfermedad dependía de otros factores. Entre ellos se menciona el tabaquismo, que parece proteger contra la CU pero aumenta el riesgo de EC31,32. También se ha considerado el papel de los antiinflamatorios no esteroideos, ya que pueden provocar brotes de la enfermedad, y también se ha especulado con el papel que puede tener la apendicectomía temprana, la cual se ha asociado a una reducción de la incidencia de la CU33,34. La flora luminal es tal vez el factor más importante en el desarrollo de la enfermedad. Estudios en modelos animales muestran que la enfermedad no se produce en animales mantenidos en medios libres de gérmenes35,36. Otros autores proponen que los antígenos presentes en la dieta también pueden contribuir. La estimulación puede ocurrir como resultado de la penetración de productos bacterianos a través de la mucosa para actuar con las células dendríticas y las poblaciones linfocitarias, lo que promovería la clásica respuesta inmunitaria. El epitelio puede así producir quimiocinas y citocinas que reclutarán y activarán a las células inmunitarias de la mucosa. De un modo u otro, se producirá la diferenciación de linfocitos T helper 1 en pacientes con EC y T helper 2 en pacientes con CU (fig. 1). En la EC, la acción mediada por los linfocitos T helper 1 se caracteriza por la producción de interferón gamma e interleucina 2, mientras que la mucosa de la CU, mediada por los linfocitos T helper 2 atípicos, produce factor transformador del crecimiento beta e interleucina 537. La activación del proceso inflamatorio va acompañada de la producción de una amplia variedad de mediadores inespecíficos de la inflamación. Éstos pueden ser otras citocinas, quimiocinas, factores de crecimiento, metabolitos del ácido araquidónico (prostaglandinas y leucotrienos) y óxido nítrico38,39.
Fig. 1. Patogenia de la enfermedad inflamatoria intestinal. Th: T helper. (Adaptada de Podolsky30.)
Hasta la fecha se ha intentado explicar la asociación de afecciones pulmonares con la EII, sin llegar a conclusiones claras. Las vías aéreas y el intestino tienen un origen común en el intestino primitivo, ambos presentan un epitelio columnar con células caliciformes y glándulas submucosas, ambos experimentan cambios inflamatorios no específicos por debajo del epitelio bronquial, y por debajo del epitelio colónico en el caso la CU40,41. Se han propuesto distintas hipótesis de mecanismos patogénicos comunes. Una hipótesis interesante postula que irritantes comunes (antígenos), tanto inhalados como ingeridos, sensibilizarían el tejido linfoide del pulmón y del intestino y desencadenarían la respuesta alérgica inflamatoria en ambos42.
Conclusiones
La incidencia y prevalencia de la EII y, con ella, de todas sus manifestaciones extraintestinales van en aumento en los países desarrollados. Además se ha observado que las manifestaciones pulmonares de la enfermedad se comunican cada vez más en la bibliografía. Sin embargo, todavía se desconoce su magnitud real dadas las dificultades diagnósticas. No cabe duda de que se ha avanzado en el conocimiento de los mecanismos patogénicos de la EII, pero sin llegar a conclusiones definitivas. Desde luego, los procesos patogénicos comunes a ambas enfermedades se presuponen, pero tampoco se conocen con certeza. La búsqueda de posibles orígenes de estas enfermedades inflamatorias pulmonares como respuesta a sustancias procedentes del tubo digestivo es una vía de investigación poco explorada, por lo que constituye un reto para los investigadores interesados en conocer los mecanismos implicados en este tipo de enfermedades pulmonares. La introducción reciente de métodos no invasivos para estudiar las respuestas inflamatorias del pulmón tales como el estudio de aire exhalado (óxido nítrico, monóxido de carbono, marcadores de estrés oxidativo), el estudio de aire exhalado condensado (metabolitos del ácido araquidónico, citocinas, etc.) y esputo inducido (estudio citológico) pueden permitir hacer un estudio más profundo y sin riesgos en una muestra numerosa de pacientes con EII, lo que facilitaría profundizar en los mecanismos responsables de la enfermedad respiratoria asociada a la EII.