La amiloidosis es una enfermedad sistémica producida por el depósito anómalo de material amiloide; tiene la peculiaridad de detectarse con la tinción rojo Congo y es de difícil diagnóstico. La afectación del árbol traqueobronquial es muy poco frecuente y constituye un reto para el neumólogo debido al amplio diagnóstico diferencial de esta enfermedad. Se presentan 2 casos en los que se ha objetivado la afectación traqueobronquial: en uno de ellos como enfermedad primaria y en otro como afectación secundaria. El uso de técnicas broncoscópicas es primordial para el diagnóstico de la afectación traqueobronquial. En ausencia de un tratamiento médico eficaz, el manejo local de esta enfermedad con técnicas endoscópicas de repermeabilización bronquial consigue una mejoría clínica y amplía las opciones terapéuticas y pronósticas en esta enfermedad.
Amyloidosis is a systemic disease caused by abnormal deposition of amyloid material that is detected with Congo red staining and is difficult to diagnose. Involvement of the tracheobronchial tree is rare and is a challenge for pulmonologists because of the wide differential diagnosis of this disease. We present two cases where tracheobronchial affectation has been observed: in one of them as a primary disease, and in another as secondary affectation. The use of bronchoscopic techniques is essential for the diagnosis of tracheobronchial involvement. In the absence of an effective drug therapy, local management of this disease with endoscopic techniques for bronchial repermeabilization is able to provide clinical improvement and expand the treatment options and prognosis in this disease.
La amiloidosis es una enfermedad sistémica de origen desconocido que se caracteriza por depósito extracelular de proteínas con una conformación estructural característica que les confiere la peculiaridad de presentar una birrefringencia verde-manzana al teñirse con rojo Congo. Se depositan principalmente en el corazón, los riñones y el hígado. Las enfermedades producidas por depósito anómalo de amiloide se pueden clasificar en primarias o secundarias, o, basándose en su distribución, en localizadas o sistémicas. Por tanto, la afectación pulmonar por amiloidosis puede ser tanto secundaria como primaria, sistémica o localizada. Se estima una incidencia entre 5 y 10 personas por millón de habitantes/año; sin embargo, la afectación primaria pulmonar es mucho más infrecuente1 y supone un reto para el neumólogo, ya que el uso de técnicas broncoscópicas es imprescindible para llegar al diagnóstico y para ofrecer un tratamiento óptimo.
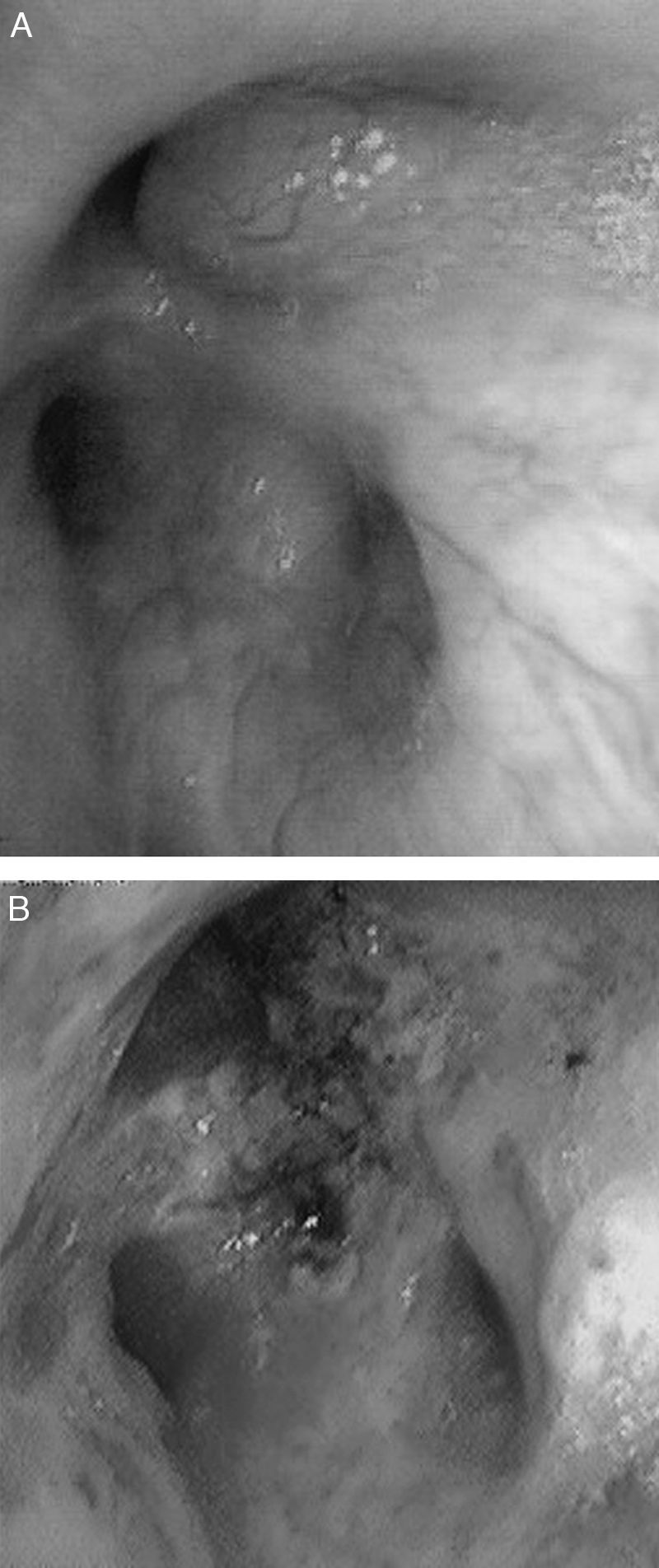
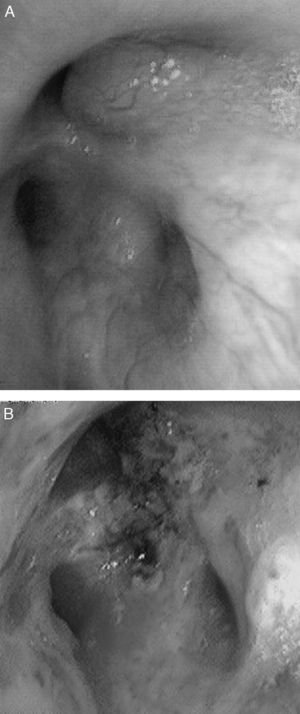
CasosCaso 1Varón de 46 años que consultó por tos no productiva, disnea de moderados esfuerzos de nueva aparición y fiebre de 38°C. Como único antecedente, fumador de 45 paquetes/año sin criterios clínicos de bronquitis crónica. En la exploración física destacaba saturación basal de oxígeno medida por pulsioximetría (SpO2) de 93% respirando aire ambiente, y en la auscultación pulmonar roncus en ambos hemitórax. La radiografía de tórax mostró una condensación alveolar en la base derecha e incipiente en el ápex izquierdo, y una imagen nodular en el segmento apical del lóbulo inferior izquierdo. En la analítica sanguínea presentaba leucocitosis de 17,6×109/l con neutrofilia del 86% y una proteína C reactiva de 19mg/dl. Ante la sospecha de neoplasia pulmonar, se realizó una tomografía computarizada (TC) de tórax que mostró imágenes en vidrio deslustrado en el lóbulo superior izquierdo y en segmentos posterobasales de ambos lóbulos inferiores, así como múltiples imágenes nodulares (centroacinares) y de árbol en brote, localizadas en el segmento apical del lóbulo inferior izquierdo y en segmentos posterobasales con tendencia a conglomerarse, sin formaciones adenopáticas. Se realizó fibrobroncoscopia, que evidenció una obstrucción >80% de la luz de los bronquios B1-B6D por infiltración de la submucosa y lesiones nodulares (fig. 1A), así como una estenosis irregular de los bronquios basales derechos. Además presentaba un ensanchamiento carineal y estenosis traqueal en el tercio superior. La biopsia mostró epitelio respiratorio con depósitos de material amiloide que, tras la realización de técnicas inmunohistoquímicas con rojo Congo, se confirmó como amiloidosis. Se realizó estudio de extensión, descartándose enfermedad sistémica, por lo que se estableció el diagnóstico de amiloidosis primaria traqueobronquial localizada.
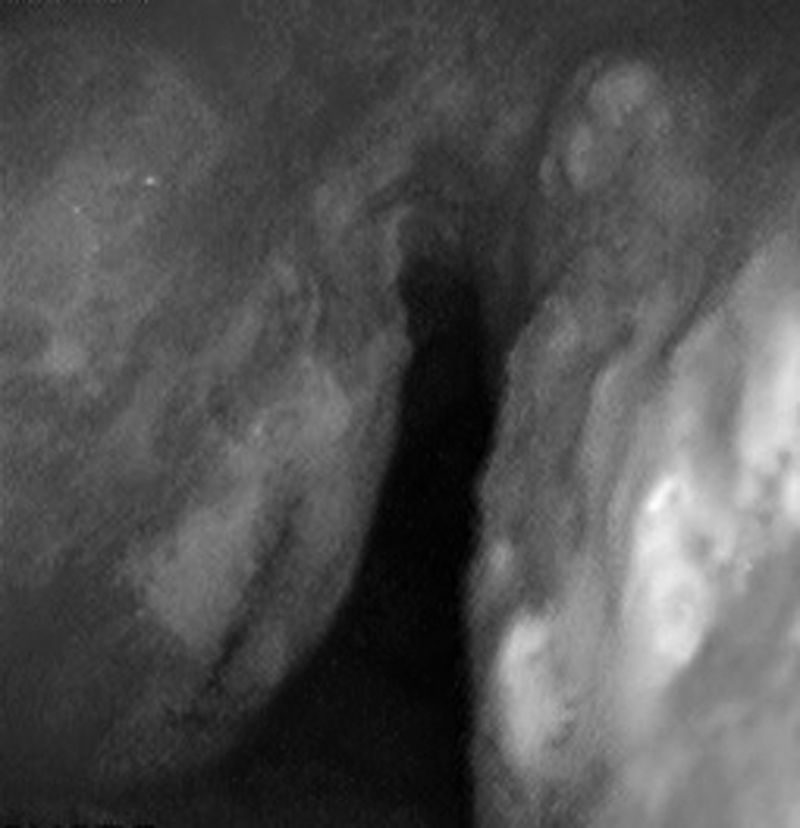
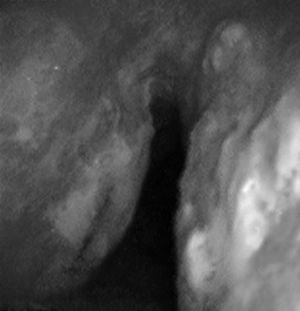
Caso 2Mujer de 57 años con episodios repetidos de expectoración hemoptoica sin otra sintomatología acompañante. Tenía antecedentes de hipertensión arterial en tratamiento con valsartán, obstrucción nasal crónica y sin hábitos tóxicos. La exploración física fue normal, así como las pruebas complementarias realizadas: analítica y radiografía torácica. Se realizó broncoscopia, detectándose múltiples nódulos en las caras anterior y posterior de la tráquea friables y sangrantes, uno de ellos ulcerado (fig. 2). El estudio anatomopatológico demostró la presencia de material amorfo eosinófilo que presentaba birrefringencia con luz polarizada correspondiente a material amiloide. Se realizó estudio de extensión de la enfermedad, detectándose también material amiloide en la grasa subcutánea y en la biopsia de médula ósea, quedando diagnosticada de una amiloidosis primaria sistémica con afectación pulmonar y de médula ósea.
DiscusiónLa amiloidosis es una enfermedad poco frecuente de etiología incierta caracterizada por un depósito extracelular anómalo de proteínas fibrilares que patognomónicamente presentan birrefringencia verde manzana bajo luz polarizada tras la tinción con rojo Congo. La afectación es variable, y puede existir una enfermedad primaria, secundaria o senil. La enfermedad puede ser sistémica o bien localizada en un órgano o tejido2. La afectación pulmonar por amiloide es excepcional, tanto si forma parte de una enfermedad sistémica como si es localizada. Se han descrito 5 formas de amiloidosis primaria pulmonar: traqueobronquial, nodular (solitaria o múltiple), pulmonar senil, mediastínica-hiliar e intersticial difusa3. La amiloidosis traqueobronquial es la presentación más frecuente3 y se caracteriza por depósitos de amiloide exclusivamente en el árbol traqueobronquial.
La amiloidosis afecta mayoritariamente al sexo masculino (2:1) y en edades medias de la vida (50-60 años). La presentación clínica, en el caso de una enfermedad sistémica, varía en función de los órganos involucrados. En el caso de afectación pulmonar es más frecuente la presencia de tos (74%), sibilancias audibles (70%), disnea (60%), hemoptisis (50%) y estridor (30%)4. Más de la mitad de los casos pueden comenzar como neumonía obstructiva, bronquiectasias o atelectasias4, por lo que plantea un importante reto identificarla aun formando parte de los diagnósticos diferenciales de diversas entidades como son asma, neumonías de repetición y neoplasias.
Se han empleado diferentes técnicas de imagen para el diagnóstico de la enfermedad. Principalmente útil es la TC de alta resolución, que permite distinguir la forma de afectación pulmonar5. Novedoso es el uso del PET-TC, que presenta una intensa captación de la 18-fluorodesoxiglucosa (18-FDG) por parte del material amiloide, utilizado con el fin de valorar la actividad, siendo de utilidad en el seguimiento de los pacientes6.
El diagnóstico de certeza se establece mediante un estudio anatomopatológico de la zona afectada, lo que hace fundamental la realización de técnicas endoscópicas bronquiales cuando se afecta la vía aérea. Se han descrito varios patrones sugestivos broncoscópicos: nodular, seudotumoral, polipoideo o submucoso7, y junto con la ultrasonografía endobronquial (EBUS) —para descartar afectación mediastínica— se consigue una valoración integral de la enfermedad por parte del broncoscopista. La afectación sistémica puede valorarse mediante una ecocardiografía y la medición de la proteinuria, que evalúan la afectación cardíaca y renal, respectivamente, ya que son los 2 órganos que más frecuentemente se afectan.
No se ha descrito un tratamiento médico eficaz para la amiloidosis pulmonar; sin embargo, hay técnicas broncoscópicas terapéuticas efectivas para el manejo de esta enfermedad con el fin primario de repermeabilizar la vía aérea. Para ello se ha utilizado el láser Nd:YAG para tratar obstrucciones bronquiales debidas a depósitos de amiloide8, consiguiendo una mejoría sintomática a medio plazo también con el uso de crioterapia9. El broncoscopio rígido permite tanto la resección endoscópica de una obstrucción amiloidea como la posterior colocación de una prótesis endobronquial de Dumon para mantener así permeable la vía aérea por más tiempo10. La radioterapia local externa (EBRT) consigue una importante mejoría clínica11-13, precisando una individualización del tratamiento dadas las posibles complicaciones debidas a la radiación11.
Si la afectación es sistémica, clásicamente se ha utilizado el tratamiento con colchicina. Posteriormente se ha demostrado una mayor supervivencia con dexametasona en monoterapia14 y, sobre todo, con la combinación de prednisona y melfalán15. En los casos en los que es posible, se realiza trasplante de células madre autólogo2. Cuando la afectación se localiza en el árbol traqueobronquial o en el parénquima pulmonar no está indicado el tratamiento con fármacos sistémicos2.
En cuanto al seguimiento de estos pacientes, el grupo de trabajo de Amiloidosis de la Universidad de Boston, con gran experiencia, sugiere la realización de pruebas de función respiratoria y TC seriadas como la mejor forma de valorar el estado de la vía aérea y la progresión de la enfermedad16.
El pronóstico se relaciona con la afectación sistémica, con mayor mortalidad en los que presentan afectación cardiaca; la principal causa de fallecimiento es la muerte súbita17. En el caso de una afectación localizada pulmonar el pronóstico mejora, y las principales causas de muerte son la insuficiencia respiratoria y la hemoptisis masiva.
El paciente del caso 1 fue tratado en 2 ocasiones con láser Nd:YAG para la repermeabilización de la vía aérea (fig. 1B), debido a la estenosis que presentaba por infiltración amiloide, con lo que se consiguió una mejoría clínica y funcional del paciente. En cuanto a la paciente del caso 2, recibió tratamiento con una combinación de prednisona y melfalán, con buena respuesta y resolución parcial de las lesiones traqueales sin afectación funcional ni sintomática.
FinanciaciónNinguna.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.