El nódulo pulmonar solitario (NPS) es un reto clínico importante para todo médico implicado en su estudio. El objetivo se cifra siempre en impedir que una lesión maligna pase inadvertida, pero también en evitar que se realicen pruebas diagnósticas innecesarias. Si en el futuro inmediato se generaliza todavía más, como parecen indicar las investigaciones más recientes, el uso de la tomografía computarizada de tórax como método de detección precoz del cáncer de pulmón, es probable que se produzca un notable aumento del número de NPS diagnosticados. En tal caso se haría imprescindible desarrollar técnicas que permitan abordar este problema con una óptima relación riesgo-beneficio. En este trabajo se revisan los fundamentos y los avances que se han producido en el uso de la tomografía por emisión de positrones como técnica de estudio del NPS. Se discuten, asimismo, las causas que explican los posibles falsos positivos y negativos de la prueba, así como las estrategias dirigidas a incrementar la rentabilidad diagnóstica de este procedimiento.
Solitary pulmonary nodules are a major clinical challenge for all doctors involved in their study. The aim is always to avoid missing malignant lesions but also to avoid performing unnecessary diagnostic tests. The most recent research suggests that in the near future chest computed tomography will become even more widely used for the early detection of lung cancer. If this occurs, there is likely to be a marked increase in the number of solitary pulmonary nodules detected, making it essential to develop techniques that enable us to manage this problem with an optimal risk-benefit ratio. We review the underlying principles of positron emission tomography and the advances that have been made in its use for the study of solitary pulmonary nodules. In addition, we discuss the possible causes of false positives and negatives in this technique and the strategies aimed at increasing diagnostic yield.
El nódulo pulmonar solitario (NPS) se define como una imagen radiológica única, de aspecto nodular, localizada en el pulmón y rodeada de parénquima sano, de un tamaño inferior a 3cm, que no se acompaña de adenopatías significativas. Puede aparecer hasta en un 0,2% de las radiografías de tórax realizadas por cualquier motivo1. Su estudio supone un gran reto para cualquier clínico en su práctica diaria. Por un lado, entre el 20 y el 40% de los NPS son lesiones malignas, lo que debe obligar a resecarlos lo antes posible2. Por otra parte, entre el 20 y el 40% de los NPS operados se comprueba luego que son benignos, por lo que quizá no hubiera tenido que realizarse intervención quirúrgica alguna2. Lo ideal sería pues que antes de la cirugía pudieran clasificarse como malignos o benignos todos los NPS, al objeto de impedir que una lesión maligna siga creciendo y empeore el pronóstico del paciente, pero también para evitar que, en el caso de las lesiones benignas, se lleven a cabo extirpaciones innecesarias, que se asocian con cierto peligro para el paciente.
El diagnóstico del NPS se establece en la actualidad mediante una radiografía simple o una tomografía computarizada (TC) de tórax, con independencia del motivo que haya podido llevar a la realización de estas exploraciones. La valoración de la naturaleza del nódulo se hace normalmente atendiendo al cálculo del riesgo de que la lesión sea maligna, análisis que casi siempre se basa en criterios clínicos y radiológicos. Entre ellos, los que han demostrado su importancia como factores independientes y su relación con una alta probabilidad de que la imagen sea maligna son la edad, el antecedente de un tabaquismo significativo, la historia previa de cáncer (> 5 años atrás) y las características propias del nódulo (tamaño > 3cm, existencia de espículas en sus bordes y localización en los lóbulos superiores)3. Otros hallazgos radiológicos posibles, como la presencia de calcificaciones o la estabilidad de la lesión durante más de 2 años, se considera que apuntan a la benignidad del hallazgo1. No obstante, no hay duda de que para confirmar si finalmente la imagen es maligna o benigna, en los casos en que las técnicas antes mencionadas no permiten llegar a una conclusión definitiva (NPS indeterminado), se hace imprescindible la biopsia del nódulo. Ésta puede efectuarse mediante una broncoscopia, con una punción aspirativa transtorácica con aguja fina o merced a un abordaje quirúrgico. Ninguno de estos 3 procedimientos está exento de riesgo1.
Conviene señalar que en un estudio multicéntrico reciente parece demostrarse que la realización de una TC torácica anual a los individuos con un riesgo mayor que la población general de presentar un cáncer de pulmón consigue que dicho tumor, de existir, se detecte en estadios menos avanzados. De esta forma, en los pacientes a los que por este motivo se practica la obligada resección quirúrgica se observa que la supervivencia a los 5 años es muy alta4. A la vista de estos resultados cabe suponer que en los próximos años podrá asistirse, si se generaliza el uso de la TC torácica como un método rentable en la prevención secundaria del cáncer de pulmón, a un notable aumento del número de NPS diagnosticados. Clasificar estos nódulos como benignos o malignos será una parte muy importante del trabajo diario de los neumólogos y, en general, de los médicos que atienden a los pacientes con enfermedades respiratorias. Por tanto, es muy conveniente que aparezcan nuevas vías de acercamiento al diagnóstico diferencial del NPS, vías que idealmente han de obviar la necesidad de realizar pruebas cruentas y que, al mismo tiempo, deben reducir a cero la probabilidad de que una lesión maligna deje de reconocerse.
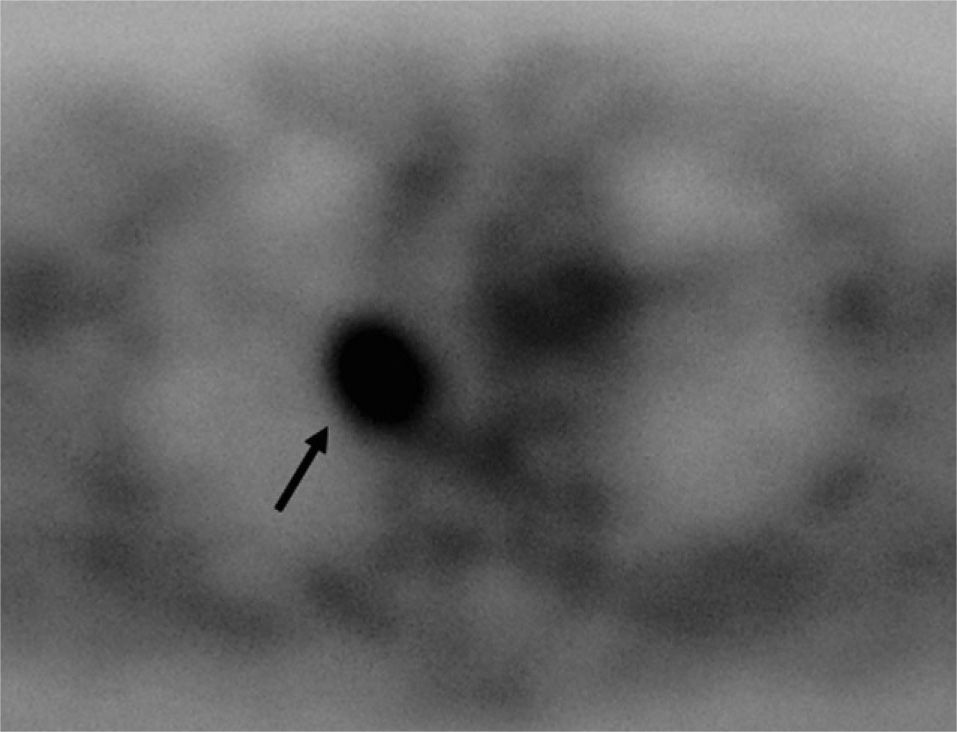
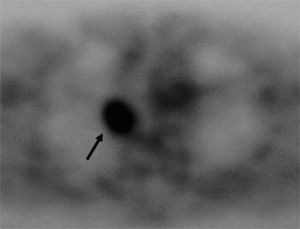
Los tumores malignos, entre ellos el cáncer de pulmón, tienen una gran capacidad para captar y metabolizar la glucosa5. La 18F-fluorodesoxiglucosa (FDG) puede emplearse como un análogo de la glucosa que, captada por las células, en mayor proporción por las malignas, se acumula en ellas, para luego emitir la correspondiente radiación en forma de positrones. Estos elementos pueden analizarse después con aparatos especiales y traducirse en imágenes tomográficas, lo que constituye la base de la denominada tomografía por emisión de positrones (PET)6. De este modo puede decirse, simplificando, que si en un NPS se acumula la glucosa marcada, en comparación con la que se deposita en el resto de los tejidos, es muy probable que la lesión sea maligna (fig. 1). Por el contrario, si su captación es igual o inferior a la de las estructuras circundantes, es probable que sea benigna.
En atención a lo señalado, una de las principales indicaciones de la PET es el estudio del NPS cuya naturaleza benigna o maligna no ha podido aclararse mediante una valoración radiológica convencional (NPS indeterminado)1. Sin embargo, la PET no está exenta de resultados falsamente positivos (lesiones benignas que captan la FDG, tales como los granulomas o los tuberculomas) y falsamente negativos (lesiones malignas que no captan la FDG). Cuando se producen, estos errores se traducen, en el primer caso, en la realización de pruebas innecesarias y, en el segundo, en la falta de tratamiento de una tumoración pulmonar potencialmente curable, lo que es aún mucho peor. Por ello, los esfuerzos de muchos investigadores se han encaminado a establecer las variables que determinan la sensibilidad y la especificidad de la PET, así como a intentar que aumente la precisión de la técnica. A continuación se discute el papel que la PET puede tener en el diagnóstico diferencial del NPS, analizando para ello sus ventajas, sus inconvenientes y los métodos que permiten mejorar la rentabilidad del procedimiento.
Rentabilidad de la tomografía por emisión de positronesRentabilidad diagnósticaLa validación de la rentabilidad de cualquier prueba diagnóstica se establece al comparar la nueva técnica con otra de referencia, lo que permite determinar, entre otras cosas, su sensibilidad (porcentaje de positivos verdaderos detectados como tales) y especificidad (porcentaje de negativos verdaderos detectados como tales). En el caso del NPS, la técnica estándar es el estudio anatomopatológico de la biopsia obtenida mediante una fibrobroncoscopia, una punción aspirativa transtorácica con aguja fina o un procedimiento quirúrgico. No obstante, en la mayoría de los estudios al respecto también se acepta la posibilidad de un seguimiento radiológico que supere los 18 o 24 meses, de tal forma que el crecimiento del nódulo se interpreta como un signo de malignidad y la estabilidad radiológica, como un dato de benignidad7-9.
Según las series que se consulten, la sensibilidad y la especificidad de la PET en la valoración del NPS varían apreciablemente, en gran parte como consecuencia de los diferentes diseños metodológicos utilizados en cada estudio. Por ello son importantes los resultados proporcionados por un metaanálisis publicado en 2001, en el que se incluyeron 40 trabajos que reunían, en conjunto, más de 1.400 lesiones pulmonares y en el que se establecieron unos valores para la sensibilidad y la especificidad del 96,8 y el 77,8%, respectivamente. Con ellos el área bajo la curva de eficacia diagnóstica era máxima10. De este metaanálisis puede colegirse, por tanto, que la PET ofrece una alta sensibilidad, aunque también tiene una probabilidad nada desdeñable de encontrar casos falsamente negativos. Por otra parte, su especificidad es intermedia, por lo que puede mostrar resultados falsamente positivos con relativa frecuencia.
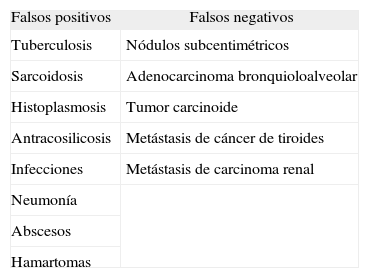
Falsos positivos. Casi todos los estudios que evalúan la rentabilidad de la PET en el diagnóstico del NPS encuentran algún falso positivo. Esta circunstancia se explica porque el aumento de la captación de la FDG no es específico de los tumores. Diversos procesos infecciosos o inflamatorios crónicos, como los granulomas11, la histoplasmosis12, la tuberculosis o la antracosilicosis,2, al igual que algunos tumores benignos como los hamartomas,9, por citar algunos ejemplos, pueden dar imágenes falsamente positivas, que pueden llevar a engaño y a poner en marcha exploraciones cruentas que no están exentas de riesgo (tabla I).
Causas de falsos positivos y negativos cuando se emplea la tomografía por emisión de positrones en el estudio del nódulo pulmonar solitario
| Falsos positivos | Falsos negativos |
| Tuberculosis | Nódulos subcentimétricos |
| Sarcoidosis | Adenocarcinoma bronquioloalveolar |
| Histoplasmosis | Tumor carcinoide |
| Antracosilicosis | Metástasis de cáncer de tiroides |
| Infecciones | Metástasis de carcinoma renal |
| Neumonía | |
| Abscesos | |
| Hamartomas |
Falsos negativos. Un resultado falsamente negativo es, en el caso del NPS, un problema de mayor envergadura que uno falsamente positivo, ya que puede inducir a dejar sin tratamiento un tumor maligno que podría encontrarse en un estadio potencialmente curable. Conviene recordar que hay 3 causas principales de resultados falsamente negativos:
- 1.
Tumores de un tamaño tan pequeño que supere la capacidad de resolución espacial de la PET. En la TC torácica pueden verse y medirse imágenes subcentimétricas con relativa facilidad. Sin embargo, la resolución máxima de los equipos de PET actuales6 está en torno a los 6-8mm, por lo que es muy difícil que estos nódulos, aun captando la glucosa marcada, puedan aparecer como imágenes detectables. En un intento de solventar este problema, en algunos trabajos se ha establecido la estrategia de corregir el efecto de volumen parcial que ofrece la TC torácica para modificar posteriormente los niveles de captación de la PET13. Sin embargo, este procedimiento es bastante complejo y pocas veces útil en la práctica clínica. En realidad, la valoración de los nódulos pequeños es uno de los más importantes retos que actualmente tiene la PET.
- 2.
Competición en la captación de la FDG ocasionada por la existencia de hiperglucemia concomitante14. En los pacientes con hiperglucemia se observa una mayor proporción de falsos negativos. Curiosamente, los incrementos bruscos de la glucosa sérica son responsables de este fenómeno con mayor frecuencia que la hiperglucemia mantenida14. Por este motivo suele recomendarse a los pacientes que se mantengan en ayunas durante al menos las 4h previas a la realización de la PET. Es ésta una precaución importante, ya que se han descrito casos en que un nódulo que al principio aparecía como negativo pasaba a ser claramente positivo tras llevar a cabo un ayuno controlado14.
- 3.
Tumores malignos con escasa capacidad para captar la glucosa, como ocurre con el adenocarcinoma bronquioloalveolar o el tumor carcinoide. Muchas de las series más importantes describen, entre sus falsos negativos, neoplasias de este tipo6,13,15.
El adenocarcinoma bronquioloalveolar, subtipo de carcinoma pulmonar poco frecuente, tiene una importante variabilidad histológica, lo que se traduce en una cierta capacidad para variar sus manifestaciones radiológicas y en que no siempre es fácil su identificación anatomopatológica. Su forma de expresión más frecuente es el NPS16 y su crecimiento suele ser lento, con una tendencia relativamente baja a producir metástasis a distancia17. Su estudio mediante una PET puede dar lugar a resultados falsamente negativos hasta en un 57% de los casos. Además, se ha señalado que su capacidad para captar la glucosa marcada es inversamente proporcional al grado de diferenciación histológica del tumor18, lo que se ha querido explicar por el hecho de que las células malignas de este tumor expresan, en comparación con las de otras neoplasias pulmonares primarias, una menor cantidad de la molécula transportadora de la glucosa denominada Glut-117.
Los carcinoides pulmonares, por su parte, son tumores neuroendocrinos que derivan de células que pueden captar y descarboxilar precursores amínicos (sistema APUD)19. Su grado de diferenciación es alto, lo que hace que capten menos glucosa marcada que otros tumores malignos y, por ello, que a veces sea difícil detectarlos con una PET20. Para obviar este inconveniente, algunos trabajos recientes han planteado la posibilidad de utilizar, en vez de glucosa marcada, algún metabolito específico de los tumores neuroendocrinos, como el 11-C-5-hidroxitriptófano, que, al ser captado selectivamente por las células del sistema APUD, aumentaría la rentabilidad diagnóstica de la PET19. No obstante, es claro que se requieren más estudios para evaluar el rendimiento de esta posibilidad en estos casos.
Rentabilidad pronósticaAdemás de un valor diagnóstico, la PET tiene utilidad pronóstica, sobre todo en los pacientes ya diagnosticados de cáncer de pulmón. En efecto, es útil en la estadificación1 y en el estudio de la recidiva tumoral, tanto en el cáncer de pulmón como en otras neoplasias6,21.
Además, el grado de captación de la FDG es un buen marcador de la agresividad de la neoplasia22. Se ha observado asimismo que determinados tumores quimiorresistentes captan menos la glucosa marcada, captación que es inversamente proporcional a la expresión de la glucoproteína P, uno de los factores de quimiorresistencia mejor estudiados23. Conviene señalar, sin embargo, que las posibilidades de la PET en el establecimiento del pronóstico de una lesión maligna no se conocen aún suficientemente, por lo que debe esperarse hasta que aparezcan nuevos trabajos al respecto.
Valoración de la captación en la tomografía por emisión de positronesHay dos formas de valorar la captación de la FDG en una PET. Una es subjetivo-cualitativa (capta o no capta, con los grados intermedios que se quiera) y la otra es objetivo-semicuantitativa. Esta última forma se basa en la aplicación del denominado “valor estándar de captación” (SUV, de standardized uptake value), que expresa una normalización de la captación de la FDG por la lesión teniendo en cuenta la dosis administrada y la masa corporal del individuo. El SUV proporciona la posibilidad de una “escala de grises”, cuya oscilación se encuentra entre el 0 y un valor máximo indefinido. Se acepta que el punto de corte para la malignidad se sitúa en la cifra de 2,56.
En una primera aproximación puede pensarse que los valores objetivos son más fiables que los subjetivos. Sin embargo, diversos trabajos han coincidido en indicar que las diferencias que se encuentran en cuanto a la sensibilidad y la especificidad de la técnica según se emplee una u otra forma de valoración no son significativas10,24. Es más, se ha llegado a señalar que la probabilidad de malignidad en los nódulos que tienen un SUV entre 0 y 2,5 puede llegar a ser hasta de un 24%15. En realidad, conocidos los múltiples factores que pueden afectar a la captación de la glucosa marcada y, por tanto, al SUV, no es fácil establecer unos valores fijos que sirvan para separar la malignidad de la benignidad de un NPS13.
Estrategias para mejorar la rentabilidad de la tomografía por emisión de positronesLa rentabilidad diagnóstica de la PET puede incrementarse si se calcula la probabilidad pretest de malignidad que tiene un paciente con un NPS. Si se considera el modelo de Swensen et al3, que recoge 3 factores clínicos y 3 radiológicos (véase más arriba), el área bajo la curva de eficacia diagnóstica de la PET aumenta de forma significativa24. Dewan et al25, por el contrario, no han observado que la aplicación de la probabilidad pretest de que exista un tumor maligno mejore el rendimiento diagnóstico de esta técnica. Esta discrepancia pudiera explicarse si se tiene en cuenta que en el último trabajo citado el número de pacientes estudiados era inferior, y que para el cálculo de la probabilidad pretest se emplearon métodos bayesianos, no de regresión logística.
En los últimos años se han desarrollado nuevas estrategias en un intento de mejorar la rentabilidad de la PET. Una de ellas se basa en tomar las imágenes tomográficas en 2 ocasiones sucesivas separadas por un tiempo determinado, que suele oscilar entre los 45 y los 60min. Así, por ejemplo, Zhuang et al26, que estudiaron distintas líneas celulares tumorales y lesiones inflamatorias inducidas en el animal de experimentación, así como nódulos pulmonares reales cuyo carácter benigno o maligno era conocido, pudieron demostrar que los tumores malignos tienen una captación que aumenta con el paso del tiempo, cosa que no sucede con las lesiones benignas. El interés de estos resultados radica en que añaden un matiz nuevo a la captación de la glucosa marcada que es propia de las células tumorales y que no se aprecia en los nódulos benignos. La explotación de esta diferencia podría servir para disminuir la tasa de falsos positivos que se observa en la PET. Futuros trabajos habrán de confirmar la veracidad de esta posibilidad.
También para corregir la infravaloración del SUV que produce la hiperglucemia se han investigado algunas fórmulas, como la de ajustar el valor de este parámetro en atención a la cifra de glucosa sérica del paciente. Con este método algunos autores han conseguido aumentar ligeramente la reproducibilidad de la técnica27.
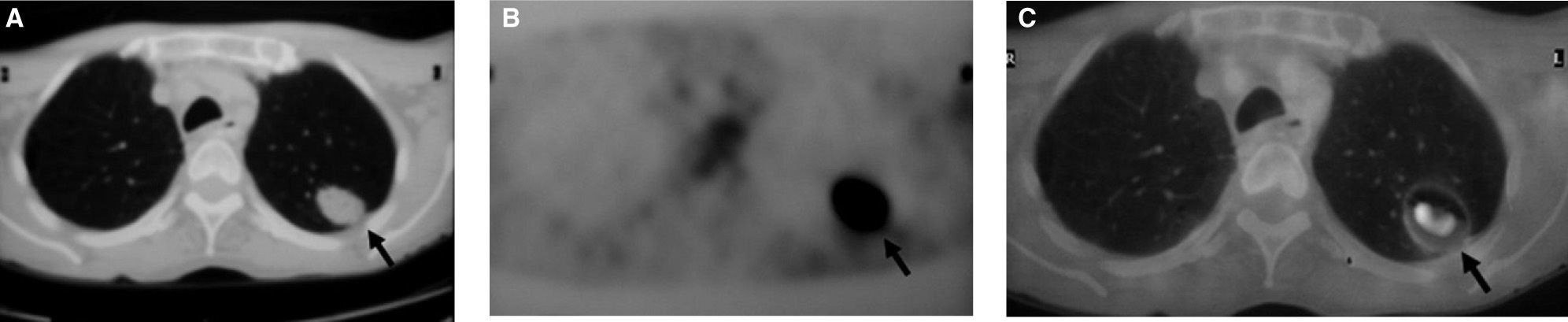
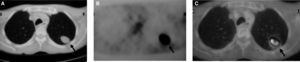
Otra estrategia que se ha empleado para aumentar la rentabilidad diagnóstica de la PET es la de combinarla con las imágenes que proporciona la TC torácica (PETTC torácica)28. En tal sentido, en los últimos 2 o 3 años han aparecido aparatos que permiten llevar a cabo ambas técnicas simultáneamente, con lo que se obtienen proyecciones que logran una superposición real (no virtual) de las imágenes que se han captado mediante la PET y con la TC torácica (fig. 2). En un reciente trabajo retrospectivo en que se compararon la sensibilidad y la especificidad de la TC, la PET y la PET-TC, como técnicas útiles en el estudio diagnóstico del NPS, se demostró que con el sistema integrado PET-TC se obtenían valores significativamente más altos que con cualquiera de las otras 2 técnicas por separado29. Conviene señalar, sin embargo, que este trabajo tiene al menos 2 limitaciones importantes: su carácter retrospectivo y el pequeño tamaño de la muestra recogida. Por ello, podría ser interesante realizar nuevos estudios basados en un diseño prospectivo y con un número mayor de pacientes.
Nódulo pulmonar solitario de naturaleza maligna, que presenta un contraste positivo en el estudio realizado de forma simultánea con tomografía por emisión de positrones y tomografía computarizada torácica (PET-TC torácica), y que luego se identificó como un adenocarcinoma pulmonar. Obsérvese el nódulo en la TC torácica (A), en la PET (B) y en la PET-TC torácica (C). Las flechas marcan la localización del nódulo maligno.
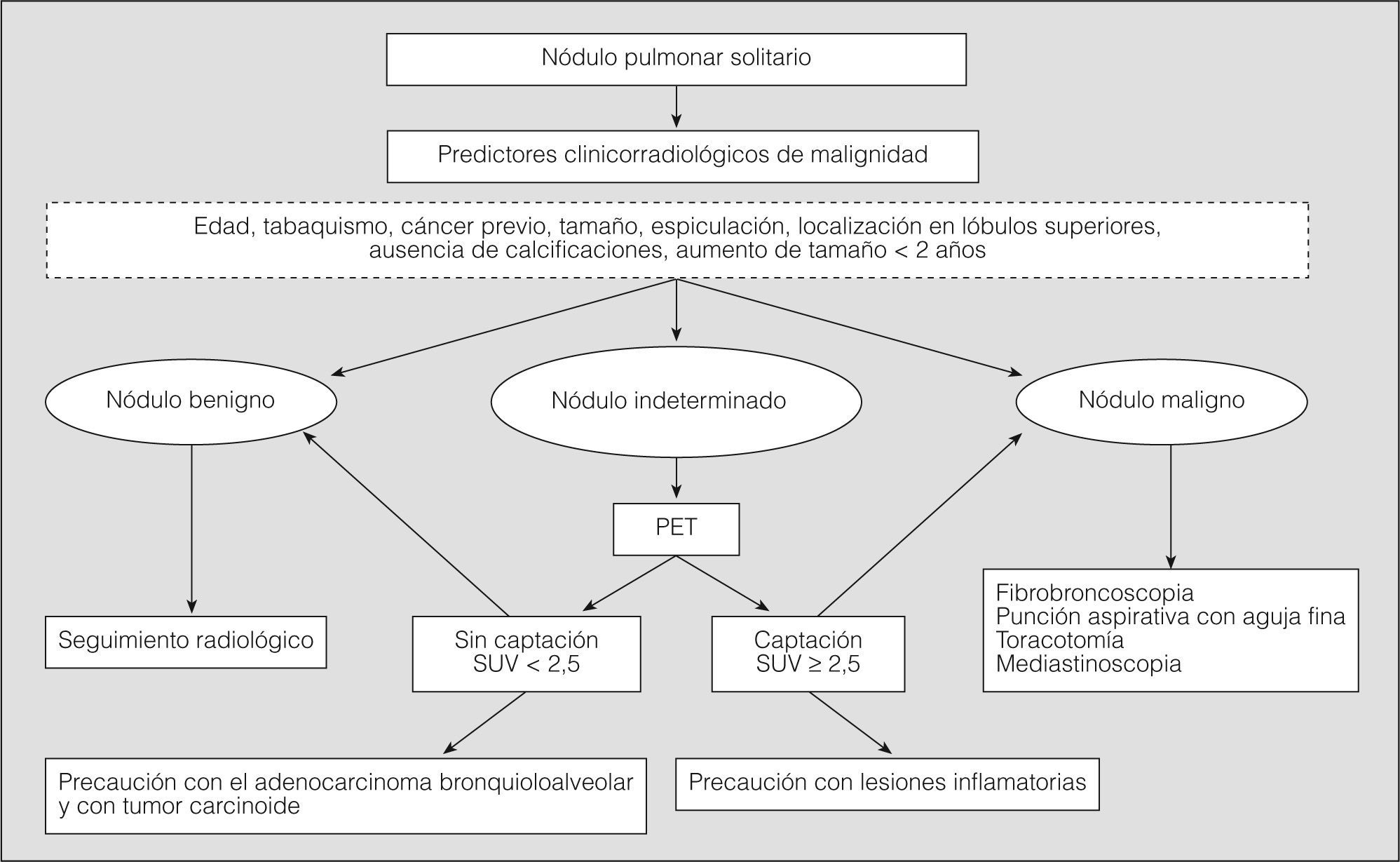
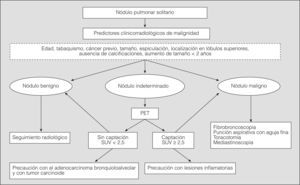
En la figura 3 se muestra un algoritmo sencillo en el que se incluyen las situaciones en que, de acuerdo con la literatura médica actual, la PET puede ayudar en el diagnóstico diferencial entre benignidad y malignidad en el estudio de un NPS. Como resumen, puede señalarse que la PET ayuda en la valoración de los nódulos que no están claramente filiados como benignos o malignos desde un punto de vista radiológico. En todo caso, no conviene olvidar la posibilidad de que también con esta técnica aparezcan falsos positivos o, lo que es aún peor, falsos negativos.
ConclusiónEl NPS sigue siendo un importante reto para todo médico implicado en su estudio. La necesidad de que no quede sin diagnosticar lesión maligna alguna hace que, en muchas ocasiones, se lleven a cabo exploraciones cruentas que nunca están exentas de riesgo y que pueden originar complicaciones graves. Por el contrario, también es posible que nódulos benignos se sometan a una resección quirúrgica que quizá no era necesaria. Este dilema, lejos de solucionarse, es probable que cada vez se plantee con más frecuencia en la práctica diaria, sobre todo si se consolida la utilización de la TC torácica como método de detección precoz del cáncer de pulmón en la población de riesgo.
La PET puede ayudar en la toma de decisiones respecto al mejor procedimiento a seguir en el diagnóstico diferencial de un NPS de características indeterminadas. Sin embargo, hay que tener en cuenta que esta técnica tiene algunas limitaciones, sobre todo en los nódulos de pequeño tamaño y en determinadas neoplasias, como es el caso del adenocarcinoma bronquioloalveolar y los tumores carcinoides. El objetivo actual se cifra en mejorar la propia técnica, evaluar la rentabilidad de nuevos metabolitos específicos para tumores poco captadores de la glucosa (como los 2 citados), valorar la posibilidad de emplear la PET de forma secuencial (en 2 tiempos) o combinada (superpuesta) con la TC torácica (PET-TC torácica) y validar los modelos que integran simultáneamente la probabilidad pretest y la PET a fin de mejorar en un futuro la rentabilidad de esta técnica diagnóstica.