La afectación pleural en la sarcoidosis es baja y se puede manifestar de diversas formas. Con el objetivo de documentar la frecuencia y las características del derrame pleural en los pacientes con sarcoidosis, revisamos los casos diagnosticados en nuestro centro entre enero de 2001 y diciembre de 2012. De los 195pacientes con sarcoidosis identificados, 3 (2hombres y una mujer) tenían un derrame pleural unilateral (1,5%): uno derecho y 2 izquierdo; 2 en estadioii y uno en estadioiv. El derrame de los 2 que se puncionaron era un exudado de predominio linfocítico. Uno de ellos correspondía a un quilotórax y el otro presentaba valores elevados de CA-125. Estos derrames suelen ser exudados serosos (a veces quilotórax), paucicelulares, de predominio linfocítico, con unas proteínas proporcionalmente más elevadas que la LDH. Pueden evolucionar favorablemente de forma espontánea, si bien en la mayoría de los casos se tratan con corticoides.
Pleural involvement in sarcoidosis is uncommon and appears in several forms. To document the incidence and characteristics of pleural effusion in sarcoidosis patients, a review of the cases diagnosed in our centre between January 2001 and December 2012 was carried out. One hundred and ninety-five patients with sarcoidosis were identified; three (two men and one woman) presented with unilateral pleural effusion (1.5%): one in the right side and two in the left. Two were in stageii and one was in stageiv. The pleural fluid of the two patients who underwent thoracocentesis was predominantly lymphocytic. One of these patients presented chylothorax and the other had high CA-125levels. In general, these effusions are lymphocyte-rich, paucicellular, serous exudates (sometimes chylothorax) and contain proportionally higher levels of protein than LDH. Most cases are treated with corticosteroids, although it may resolve spontaneously.
La sarcoidosis es una enfermedad granulomatosa sistémica de etiología desconocida de presentación y curso clínico variables. Aunque el 90% de los pacientes tienen afectación torácica, cualquier órgano puede estar afectado1. La afectación de la pleura oscila entre el 0,7 y el 10% de los casos2, pudiendo manifestarse como engrosamiento o nódulo pleural, neumotórax o derrame pleural (DP)3. Existen varios mecanismos implicados en la aparición de un DP en la sarcoidosis, lo que puede originar que el líquido pleural (LP) tenga distintas características bioquímicas3. Para documentar la frecuencia y las características del DP en los pacientes con sarcoidosis en nuestro medio, realizamos un estudio retrospectivo de los pacientes diagnosticados de sarcoidosis en nuestro hospital a partir de los datos del registro de Anatomía Patológica entre enero de 2001 y diciembre de 2012. Se incluyeron los pacientes mayores de 18años con sarcoidosis probada mediante biopsia y se excluyeron aquellos con una causa alternativa de enfermedad granulomatosa. Se revisaron sus historiales clínicos y radiológicos para determinar la presencia de DP y se registraron la edad, el sexo, el estadio radiológico, el resultado de la prueba de la tuberculina y los órganos biopsiados que aportaron el diagnóstico.
Observaciones clínicasSe diagnosticaron de sarcoidosis 195pacientes, de los cuales 3 tenían un DP unilateral. En la tabla 1 se muestran sus datos demográficos y en la tabla 2, las características del LP.
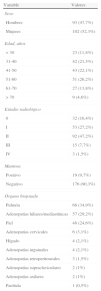
Datos demográficos, estadio radiológico y hallazgos clínicos de los pacientes con sarcoidosis (n=195)
| Variable | Valores |
| Sexo | |
| Hombres | 93 (47,7%) |
| Mujeres | 102 (52,3%) |
| Edad, años | |
| < 30 | 23 (11,8%) |
| 31-40 | 42 (21,5%) |
| 41-50 | 43 (22,1%) |
| 51-60 | 51 (26,2%) |
| 61-70 | 27 (13,8%) |
| > 70 | 9 (4,6%) |
| Estadio radiológico | |
| 0 | 32 (16,4%) |
| I | 53 (27,2%) |
| II | 92 (47,2%) |
| III | 15 (7,7%) |
| IV | 3 (1,5%) |
| Mantoux | |
| Positivo | 19 (9,7%) |
| Negativo | 176 (90,3%) |
| Órgano biopsiado | |
| Pulmón | 68 (34,9%) |
| Adenopatías hiliares/mediastínicas | 57 (29,2%) |
| Piel | 48 (24,6%) |
| Adenopatías cervicales | 6 (3,1%) |
| Hígado | 4 (2,1%) |
| Adenopatías inguinales | 4 (2,1%) |
| Adenopatías retroperitoneales | 3 (1,5%) |
| Adenopatías supraclaviculares | 2 (1%) |
| Adenopatías axilares | 2 (1%) |
| Parótida | 1 (0,5%) |
Características del líquido pleural en los pacientes con sarcoidosis
| Variable | Caso 1 | Caso 2 |
| Aspecto | Lechoso | Seroso |
| Células nucleadas (×106/l) | 1.360 | 7.000 |
| Recuento diferencial (%) | 70% linfocitos; 24% macrófagos | 62% linfocitos; 27% macrófagos |
| pH | 7,40 | 7,46 |
| Proteínas totales (g/dl) | 4,2 | 5,9 |
| Cociente proteínas LP/S | 0,63 | 0,9 |
| LDH (U/l) | 244 | 303 |
| LDH LP/S | 1 | 0,92 |
| Glucosa (mg/dl) | 116 | 101 |
| ADA (U/l) | 36 | 45 |
| Colesterol (mg/dl) | 98 | 78 |
| Triglicéridos (mg/dl) | 251 | |
| CA-125 (U/l) | 1.343 | |
| Quilomicrones | Sí | |
| Cultivos | Negativos | Negativos |
ADA: adenosina desaminasa; CA-125: antígeno carbohidrato 125; LDH: lactado deshidrogenasa; LP: líquido pleural; S: suero.
Varón de 45años que consultó por dolor torácico derecho y disnea con semiología de DP en la exploración. La TC de tórax demostró adenopatías hiliares bilaterales, DP derecho, enfermedad micronodular y probable fibrosis masiva derecha. La enzima conversora de la angiotensina (ECA) fue de 76U/l y el Mantoux, negativo. El DP fue un quilotórax. La biopsia de las adenopatías paratraqueales derechas demostró granulomas epitelioides no necrosantes. La tinción de Ziehl-Nielsen fue negativa. Se inició tratamiento con octreótido y corticoides con desaparición del DP, que reaparece al bajar o suspender la dosis de corticoides (por debajo de 10mg/día de prednisona).
Caso 2Mujer de 83años que consultó por dolor pleurítico izquierdo y disnea con semiología de DP en la exploración física. En la TC de tórax se observaban múltiples adenopatías hiliares bilaterales y mediastínicas paratraqueales (2R, 4R, 4L), moderado DP izquierdo y dudosa enfermedad micronodular. La ECA fue de 57U/l y el Mantoux, negativo. El DP fue seroso, con un CA-125 elevado. En la biopsia pleural se observaron cambios inflamatorios inespecíficos y la biopsia transbronquial demostró granulomas no necrosantes. Tras tratamiento con corticoides la evolución clínica fue favorable, desapareciendo el DP.
Caso 3Varón de 39años que consultó por síndrome general, tos, disnea progresiva y disfonía. En la exploración física destacaba la auscultación de crepitantes bibasales. La analítica de sangre era normal salvo una ECA de 170U/l, y en la TC de tórax se observaban crecimientos adenopáticos hiliares bilaterales, pequeño DP izquierdo y enfermedad intersticial bilateral. El Mantoux fue negativo y la biopsia transbronquial demostró inflamación granulomatosa no necrosante. El DP no se puncionó, y desapareció tras tratamiento con corticoides.
DiscusiónLa prevalencia de DP en nuestra serie (1,5%) está en el rango de lo habitual2, si bien se ha descrito hasta en el 8,2%4. Los mecanismos implicados en la aparición del DP son el aumento de la permeabilidad capilar por una afectación directa de la pleura (exudado), o una obstrucción del conducto torácico (quilotórax), como sucedió en nuestros casos. Con menor frecuencia, el DP puede ser hemático (compresión de los vasos por los granulomas), o un trasudado (obstrucción de la cava superior, atelectasia por estenosis bronquial, o pulmón atrapado).
El DP en la sarcoidosis afecta a ambos sexos y se manifiesta en cualquier grupo de edad y estadio radiológico. Suele ser de pequeño-moderado tamaño y afecta con más frecuencia al lado derecho. Puede estar presente en el momento del diagnóstico, o bien en una fase posterior coincidiendo con una exacerbación de la enfermedad3. En esta línea, nuestros pacientes eran de distinto género y pertenecían a diferentes grupos de edad, estadios radiológicos y lateralidades.
El DP suele ser un exudado paucicelular de predominio linfocítico (con cociente CD4/CD8 elevado), aunque puede ser eosinofílico o de predominio neutrófilo. Las proteínas están proporcionalmente más elevadas que la LDH2, la ADA suele ser baja y es posible encontrar niveles elevados de CA-125, como sucede en nuestro caso2, en mujeres con evidencia de sarcoidosis peritoneal. Sus valores disminuyen tras tratamiento con corticoides5. La prueba de la tuberculina es negativa y las biopsias, tanto pulmonar como pleural, aportan el diagnóstico al demostrar granulomas no caseificantes. Esta última puede inducir al diagnóstico de un DP tuberculoso. Pueden evolucionar favorablemente de forma espontánea, si bien en la mayoría de los casos se tratan con corticoides.
Contribución de los autoresFerreiro L. Redactora y autora. Concepción y diseño. Análisis e interpretación de los datos. Aprobación final del manuscrito.
San José E. Coautora. Análisis e interpretación de los datos. Aprobación final del manuscrito.
González-Barcala FJ. Coautor. Adquisición de los datos. Revisión del artículo. Aprobación final del manuscrito.
Suárez-Antelo J. Coautor. Adquisición de los datos. Revisión del artículo. Aprobación final del manuscrito.
Toubes ME. Coautor. Adquisición de los datos. Revisión del artículo. Aprobación final del manuscrito.
Valdés L. Redactor y autor. Concepción y diseño. Análisis e interpretación de los datos. Aprobación final del manuscrito.