La tuberculosis (TB) resistente a fármacos es un problema de salud pública mundial1. Muchos estudios se han centrado en la TB multirresistente (isoniacida y rifampicina), presentando poca atención a la TB resistente a isoniacida y sensible a rifampicina (HRRS)2. La HRRS es la forma más frecuente de resistencia (el 8,5% de los casos1,3,4) y es un factor de riesgo para presentar mala evolución clínica si el tratamiento no es adecuado5. La resistencia a H en España se estima en el 5% de los adultos y el 9,6% de los niños6. Existen pocos estudios, generalmente retrospectivos, de niños con TB HRRS debido a la dificultad de conseguir el aislamiento del germen7,8.
Durante el periodo 2014-2016 se diagnosticaron 17 niños con TB en nuestro centro, de los cuales 7 (41,2%) fueron considerados HRRS (tabla 1). El estudio fue prospectivo, utilizando la base de datos on-line REDCAP del grupo de trabajo pTBred y los niños fueron tratados por un único pediatra. Se recogieron muestras clínicas antes de iniciar el tratamiento, realizando el estudio de sensibilidad en el laboratorio local y de referencia nacional.
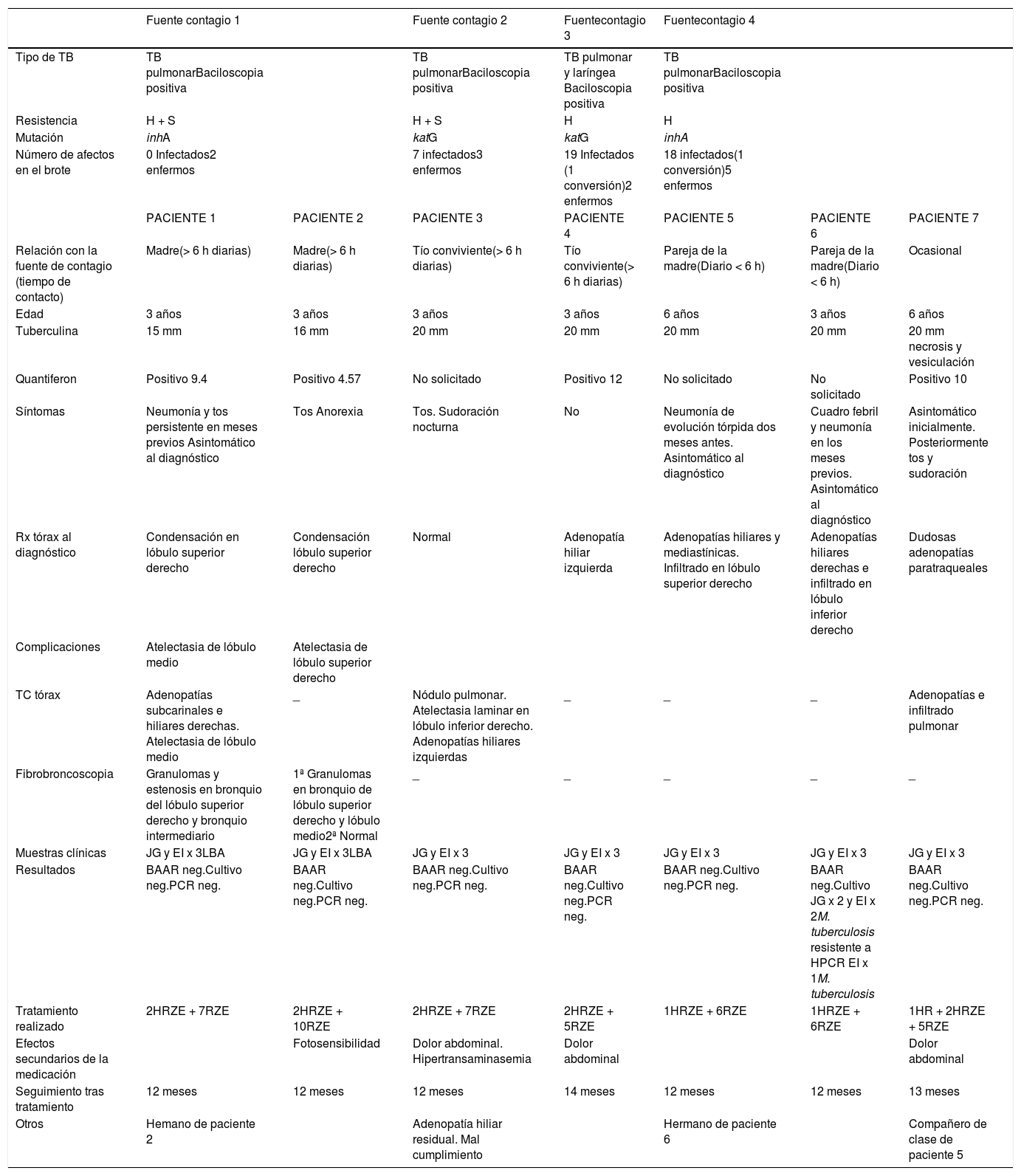
Características de los pacientes y de sus fuentes de contagio
| Fuente contagio 1 | Fuente contagio 2 | Fuentecontagio 3 | Fuentecontagio 4 | ||||
|---|---|---|---|---|---|---|---|
| Tipo de TB | TB pulmonarBaciloscopia positiva | TB pulmonarBaciloscopia positiva | TB pulmonar y laríngea Baciloscopia positiva | TB pulmonarBaciloscopia positiva | |||
| Resistencia | H + S | H + S | H | H | |||
| Mutación | inhA | katG | katG | inhA | |||
| Número de afectos en el brote | 0 Infectados2 enfermos | 7 infectados3 enfermos | 19 Infectados (1 conversión)2 enfermos | 18 infectados(1 conversión)5 enfermos | |||
| PACIENTE 1 | PACIENTE 2 | PACIENTE 3 | PACIENTE 4 | PACIENTE 5 | PACIENTE 6 | PACIENTE 7 | |
| Relación con la fuente de contagio (tiempo de contacto) | Madre(> 6 h diarias) | Madre(> 6 h diarias) | Tío conviviente(> 6 h diarias) | Tío conviviente(> 6 h diarias) | Pareja de la madre(Diario < 6 h) | Pareja de la madre(Diario < 6 h) | Ocasional |
| Edad | 3 años | 3 años | 3 años | 3 años | 6 años | 3 años | 6 años |
| Tuberculina | 15 mm | 16 mm | 20 mm | 20 mm | 20 mm | 20 mm | 20 mm necrosis y vesiculación |
| Quantiferon | Positivo 9.4 | Positivo 4.57 | No solicitado | Positivo 12 | No solicitado | No solicitado | Positivo 10 |
| Síntomas | Neumonía y tos persistente en meses previos Asintomático al diagnóstico | Tos Anorexia | Tos. Sudoración nocturna | No | Neumonía de evolución tórpida dos meses antes. Asintomático al diagnóstico | Cuadro febril y neumonía en los meses previos. Asintomático al diagnóstico | Asintomático inicialmente. Posteriormente tos y sudoración |
| Rx tórax al diagnóstico | Condensación en lóbulo superior derecho | Condensación lóbulo superior derecho | Normal | Adenopatía hiliar izquierda | Adenopatías hiliares y mediastínicas. Infiltrado en lóbulo superior derecho | Adenopatías hiliares derechas e infiltrado en lóbulo inferior derecho | Dudosas adenopatías paratraqueales |
| Complicaciones | Atelectasia de lóbulo medio | Atelectasia de lóbulo superior derecho | |||||
| TC tórax | Adenopatías subcarinales e hiliares derechas. Atelectasia de lóbulo medio | _ | Nódulo pulmonar. Atelectasia laminar en lóbulo inferior derecho. Adenopatías hiliares izquierdas | _ | _ | _ | Adenopatías e infiltrado pulmonar |
| Fibrobroncoscopia | Granulomas y estenosis en bronquio del lóbulo superior derecho y bronquio intermediario | 1ª Granulomas en bronquio de lóbulo superior derecho y lóbulo medio2ª Normal | _ | _ | _ | _ | _ |
| Muestras clínicas | JG y EI x 3LBA | JG y EI x 3LBA | JG y EI x 3 | JG y EI x 3 | JG y EI x 3 | JG y EI x 3 | JG y EI x 3 |
| Resultados | BAAR neg.Cultivo neg.PCR neg. | BAAR neg.Cultivo neg.PCR neg. | BAAR neg.Cultivo neg.PCR neg. | BAAR neg.Cultivo neg.PCR neg. | BAAR neg.Cultivo neg.PCR neg. | BAAR neg.Cultivo JG x 2 y EI x 2M. tuberculosis resistente a HPCR EI x 1M. tuberculosis | BAAR neg.Cultivo neg.PCR neg. |
| Tratamiento realizado | 2HRZE + 7RZE | 2HRZE + 10RZE | 2HRZE + 7RZE | 2HRZE + 5RZE | 1HRZE + 6RZE | 1HRZE + 6RZE | 1HR + 2HRZE + 5RZE |
| Efectos secundarios de la medicación | Fotosensibilidad | Dolor abdominal. Hipertransaminasemia | Dolor abdominal | Dolor abdominal | |||
| Seguimiento tras tratamiento | 12 meses | 12 meses | 12 meses | 14 meses | 12 meses | 12 meses | 13 meses |
| Otros | Hemano de paciente 2 | Adenopatía hiliar residual. Mal cumplimiento | Hermano de paciente 6 | Compañero de clase de paciente 5 |
BAAR: tinción directa de bacilos ácido-alcohol resistentes; E: etambutol; EI: esputo inducido; H: isoniacida; JG: jugo gástrico; LBA: lavado broncoalveolar; PCR: reacción en cadena de la polimerasa; R: rifampicina; Rx: radiografía; S: estreptomicina; TB: tuberculosis; TC: tomografía computarizada; Z: pirazinamida.
Los 7 niños con probable TB HRRS tenían entre 3 y 6 años, eran de nacionalidad española y no vacunados con BCG. Todos fueron estudiados a raíz del diagnóstico y estudio de contacto de 4 adultos con TB activa en los que posteriormente se diagnosticó la resistencia a H: 2 eran monorresistentes a H y 2 tenían además resistencia a estreptomicina, y el estudio de mutaciones detectó 2 casos en el inhA y 2 en el katG (tabla 1). Solo en un niño se aisló el germen, corroborándose el patrón de resistencia de la fuente de contagio. En los restantes 6 niños el diagnóstico de HRRS se realizó por la resistencia en la fuente de contagio y la ausencia en el estudio de contactos de un patrón de sensibilidad distinto. Cuatro de estos 6 niños tenían contacto diario de más de 6h con el adulto resistente y uno era hermano del niño con cultivo positivo.
La radiografía de tórax estaba alterada en 5 niños en el momento del diagnóstico. El paciente 7, con radiografía normal, comenzó el tratamiento de la infección tuberculosa latente presentando al mes tos persistente, con radiografía dudosa y TC patológica. Otros 2 casos se realizaron TC torácica: uno tenía síntomas clínicos y radiografía normal, siendo la TC patológica, y otro, por empeoramiento radiológico durante el tratamiento. En este y en otro paciente se realizó fibrobroncoscopia, comprobando afectación endobronquial y recibiendo corticoides.
Todos los pacientes iniciaron tratamiento con HRZE hasta que1-2 meses después, tras conocerse la resistencia siguieron con RZE hasta completar 7-12 meses. Los niños que recibieron más tiempo de tratamiento fue por incumplimiento o por TB endobronquial de lenta resolución.
El seguimiento oftalmológico por la toma de etambutol fue normal y 4 presentaron efectos secundarios leves, que no obligaron a suspender la medicación. Tras finalizar el tratamiento se realizó un seguimiento durante al menos 12 meses, presentando al alta 6 casos una radiografía normal y uno, una pequeña adenopatía residual.
Generalmente se habla de TB monorresistente, polirresistente, multirresistente o extremadamente resistente9, aunque la denominación de TB HRRS es importante por ser la más frecuente y precisar un tratamiento apropiado5,8. En nuestro estudio, la demora diagnóstica de la HRRS mediante cultivo fue de 1-2 meses al realizarse solo el diagnóstico rápido de resistencia a rifampicina (GeneXpert®). Sería recomendable incorporar un test de diagnóstico rápido como el MTBDRplus® (Hain Lifescience, Nehren, Alemania), que identifica la mayor parte de los casos resistentes a R y/o a H10. Sin embargo, los niños tuvieron un tratamiento adecuado al haber iniciado 4 fármacos por no conocerse inicialmente la sensibilidad de la fuente de contagio y tener España una tasa de resistencia a H mayor del 4%11,12. Además, en nuestra área hospitalaria hay una prevalencia inusualmente alta de tuberculosis HRRS debido mayoritariamente a cepas con patrón único indicativas de reactivaciones de TB antiguas. Tras el diagnóstico de HRRS se continuó con RZE hasta completar 7-12 meses11,13 con buena tolerancia y comprobando la curación sin secuelas ni reactivación en el seguimiento prolongado.
Las pautas recomendadas para el tratamiento inicial (2HRZE+4HR) y el retratamiento (2SHRZE+1HRZE+5HRZ) pueden llevar en los casos de HRRS a fallos de tratamiento, recaídas y resistencias adquiridas, y la asociación 6-9RZE tiene mayor hepatotoxicidad en adultos5. Un metaanálisis comparando diferentes tratamientos para la TB HRRS concluyó que la adición de una fluoroquinolona mejoraba el éxito del tratamiento, aunque solo incluyeron 37 niños2,14. Un estudio retrospectivo en niños con TB HRRS, mayoritariamente con enfermedad severa y con uso de fluoroquinolonas en el 75% de los casos, encontró solo un 4% de fallo de tratamiento8. En nuestro estudio, los pacientes no tenían enfermedad avanzada y la pauta 6-12RZE fue efectiva y sin efectos secundarios.
Podría argumentarse que alguno de los 6 niños sin confirmación bacteriológica podría no ser HRRS. La definición de probable enfermedad resistente en el niño se ha recomendado cuando la fuente de contagio es resistente9. Este estudio fue prospectivo y todos los niños se diagnosticaron a raíz del estudio de contactos de un adulto que provocó un brote de TB con muchos casos secundarios infectados y enfermos (con igual cepa y patrón de sensibilidad) y en la que 6 de los niños tenían una alta probabilidad de contagio (proximidad, frecuencia de exposición e infectividad)15. Además, los niños eran pequeños, con poca exposición a otros enfermos de TB fuera de su ambiente familiar. En cualquier caso, la baja tasa de aislamientos en la infancia condiciona que el diagnóstico de resistencia se realice con frecuencia a partir del estudio de sensibilidad de su fuente de contagio, lo cual es una barrera a la hora de publicar estudios de TB resistente en niños y poder comprobar la efectividad de las distintas pautas de tratamiento.
Concluimos la importancia de considerar la resistencia a H realizando un estudio rápido de sensibilidad a este fármaco en el niño y en su fuente de contagio y la evolución favorable de nuestros pacientes con 7-12RZE sin efectos secundarios, secuelas ni recaídas.