La gran afectación pulmonar producida por la infección del COVID-19 hace necesaria una herramienta diagnóstica rápida que complemente el test diagnóstico mediante PCR y que además sea útil en la evaluación de la progresión de las lesiones pulmonares. Ya que la mayoría de estas son periféricas, en este documento de consenso proponemos el uso de la ecografía torácica para el diagnóstico precoz y la evaluación diaria de la progresión de lesiones pulmonares por un solo explorador sin necesidad de utilizar la TC de tórax.
En este consenso se propone la realización de una exploración sistemática ecográfica del tórax dividiéndolo por cuadrantes e identificando los signos ecográficos que se relacionen con el tipo de afectación parenquimatosa o pleural que tiene el paciente: líneas A, líneas B, condensación parenquimatosa, línea pleural y derrame pleural. Estos hallazgos nos facilitarán la toma de decisiones respecto al manejo del paciente, tanto en la decisión del lugar de ingreso del paciente como en el tipo de tratamiento que debemos pautar.
The great pulmonary affectation produced by the COVID-19 infection, requires a fast diagnostic tool that complements the diagnostic test by PCR and which is also useful in evaluating the progression of lung lesions. Since most of these are peripheral, in this consensus document we propose the use of thoracic ultrasound for early diagnosis and for the daily evaluation of the progression of lung lesions by a single explorer without the need to use the chest CT. In this consensus, it is proposed to carry out a systematic ultrasound examination of the thorax dividing it by quadrants and therefore identifying the ultrasound signs that are related to the type of parenchymal or pleural affectation that the patient has: A lines, B lines, parenchymal condensation, pleural line and pleural effusion. These findings will facilitate the decision making regarding the patient management, both when deciding the place of admission of the patient and the type of treatment to be prescribed
La rápida progresión de la pandemia ocasionada por la infección de COVID-19 debido a su alta tasa de contagio, así como su rápida evolución a neumonías graves hacen necesario tanto un diagnóstico precoz de la enfermedad como una rápida detección de avance de su proceso neumónico.
Actualmente la tomografía computarizada de tórax (TC de tórax) se considera la herramienta más útil tanto para el diagnóstico precoz como para vigilar la evolución de la enfermedad (ya que la PCR tiene una alta tasa de falsos negativos en los primeros días). Los hallazgos más frecuentes son el vidrio deslustrado (88%) y la consolidación (31%), que con frecuencia aparecen en la periferia pulmonar y habitualmente combinado. En un mínimo porcentaje de casos se aprecian además engrosamiento del septo interlobular, bronquiectasias y engrosamiento pleural1,2. Sin embargo, la TC de tórax tiene el inconveniente del desplazamiento del paciente a otras zonas del hospital, lo que supone un riesgo de transmisión a otros pacientes y los propios sanitarios del hospital (en China e Italia el 3-10% de los infectados son personal sanitario)3. La ecografía torácica permite la realización de una prueba de imagen en la propia habitación del paciente, lo que evita estos inconvenientes.
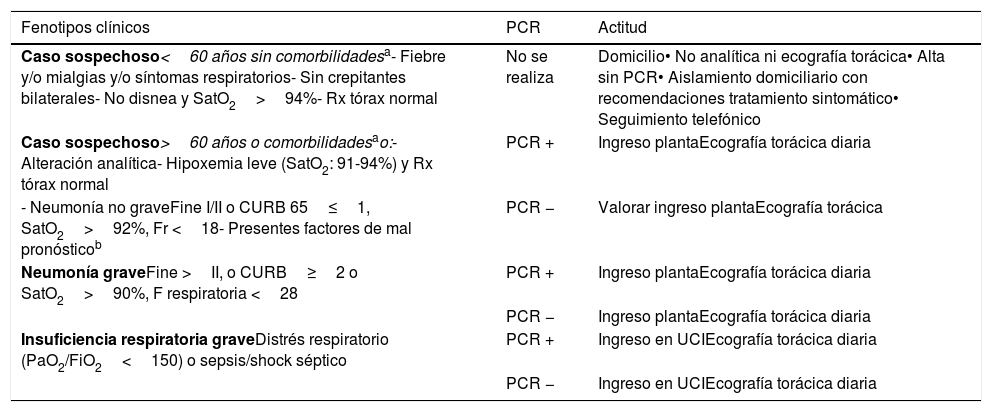
Con este protocolo elaborado por el área de Técnicas y Trasplante de la Sociedad Española de Neumología y Cirugía Torácica (SEPAR) y la Asociación Española de Endoscopia Respiratoria y Neumología Intervencionista (AEER) se propone la realización de una ecografía torácica a los pacientes con sospecha de infección por COVID-19 para confirmar su diagnóstico en los primeros síntomas y, en los casos confirmados, para realizar una rápida evaluación del estado de la enfermedad (tabla 1).
Manejo de los fenotípicos clinicos sugestivos de infección por COVID-19
| Fenotipos clínicos | PCR | Actitud |
|---|---|---|
| Caso sospechoso<60 años sin comorbilidadesa- Fiebre y/o mialgias y/o síntomas respiratorios- Sin crepitantes bilaterales- No disnea y SatO2>94%- Rx tórax normal | No se realiza | Domicilio• No analítica ni ecografía torácica• Alta sin PCR• Aislamiento domiciliario con recomendaciones tratamiento sintomático• Seguimiento telefónico |
| Caso sospechoso>60 años o comorbilidadesao:- Alteración analítica- Hipoxemia leve (SatO2: 91-94%) y Rx tórax normal | PCR + | Ingreso plantaEcografía torácica diaria |
| - Neumonía no graveFine I/II o CURB 65≤1, SatO2>92%, Fr <18- Presentes factores de mal pronósticob | PCR − | Valorar ingreso plantaEcografía torácica |
| Neumonía graveFine >II, o CURB≥2 o SatO2>90%, F respiratoria <28 | PCR + | Ingreso plantaEcografía torácica diaria |
| PCR − | Ingreso plantaEcografía torácica diaria | |
| Insuficiencia respiratoria graveDistrés respiratorio (PaO2/FiO2<150) o sepsis/shock séptico | PCR + | Ingreso en UCIEcografía torácica diaria |
| PCR − | Ingreso en UCIEcografía torácica diaria |
- 1.
Ecógrafo (preferiblemente portátil para minimizar la posibilidad de contagio).
- 2.
Sonda lineal de alta frecuencia o sonda miniconvex ajustada a la frecuencia más alta posible para dicha sonda. En caso de sonda convex abdominal, ajustar igualmente a la máxima frecuencia posible.
Las medidas de aislamiento y limpieza posterior serán iguales a las de un pase de visita convencional, añadiendo una funda protectora de un solo uso para la sonda ecográfica.
ProcedimientoLo ideal es que el procedimiento sea llevado a cabo por un solo facultativo mientras que un ayudante anotará los hallazgos ecográficos observados (anexo 1).
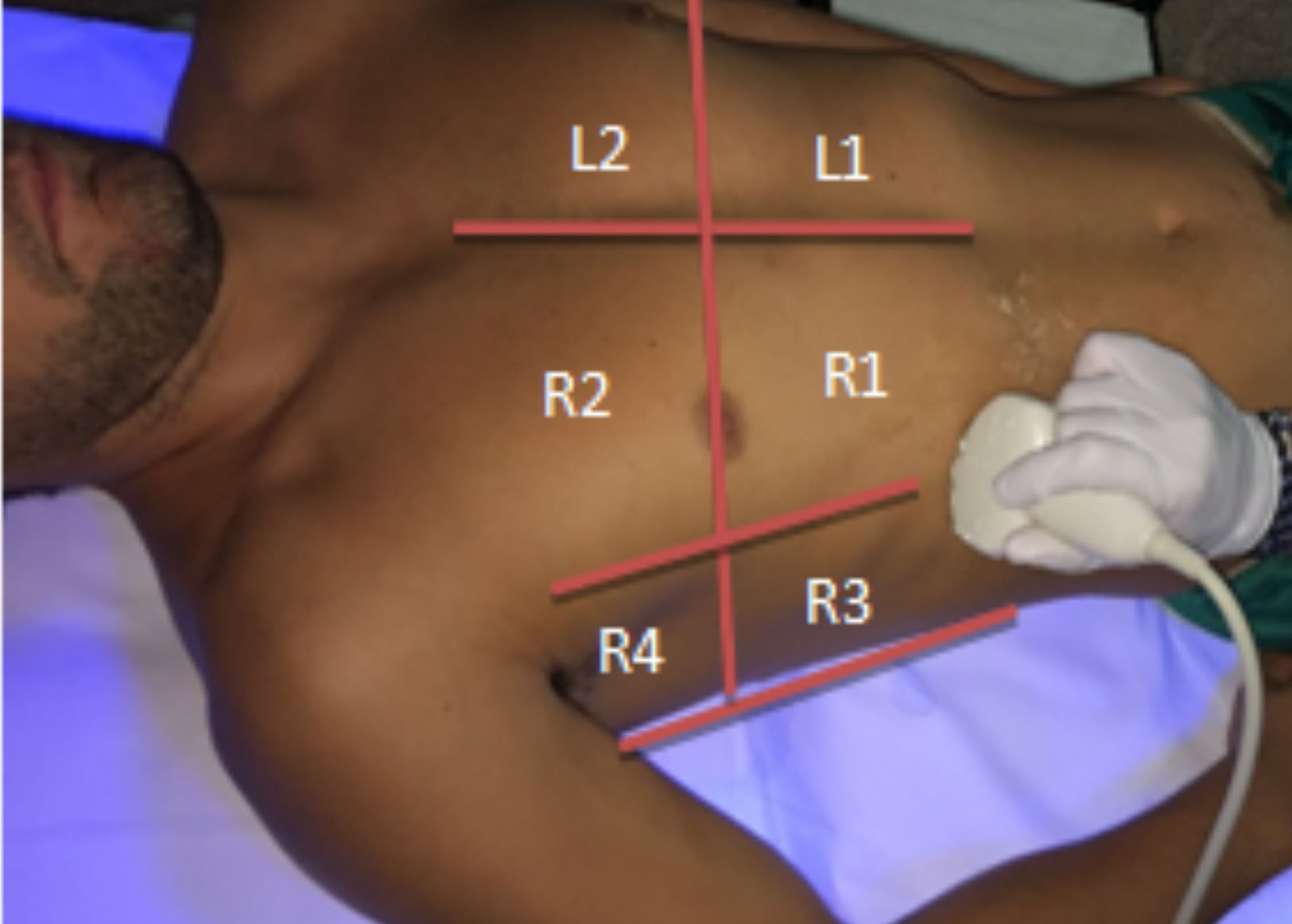
Para llevar a cabo la exploración de una manera sistemática se divide la zona anterior del tórax en 4 cuadrantes mediante una línea imaginaria que pasa por el esternón y otra que pasa por la areola que a su vez nos dividirá la zona axilar (entre línea axilar anterior y posterior) en superior e inferior (fig. 1).
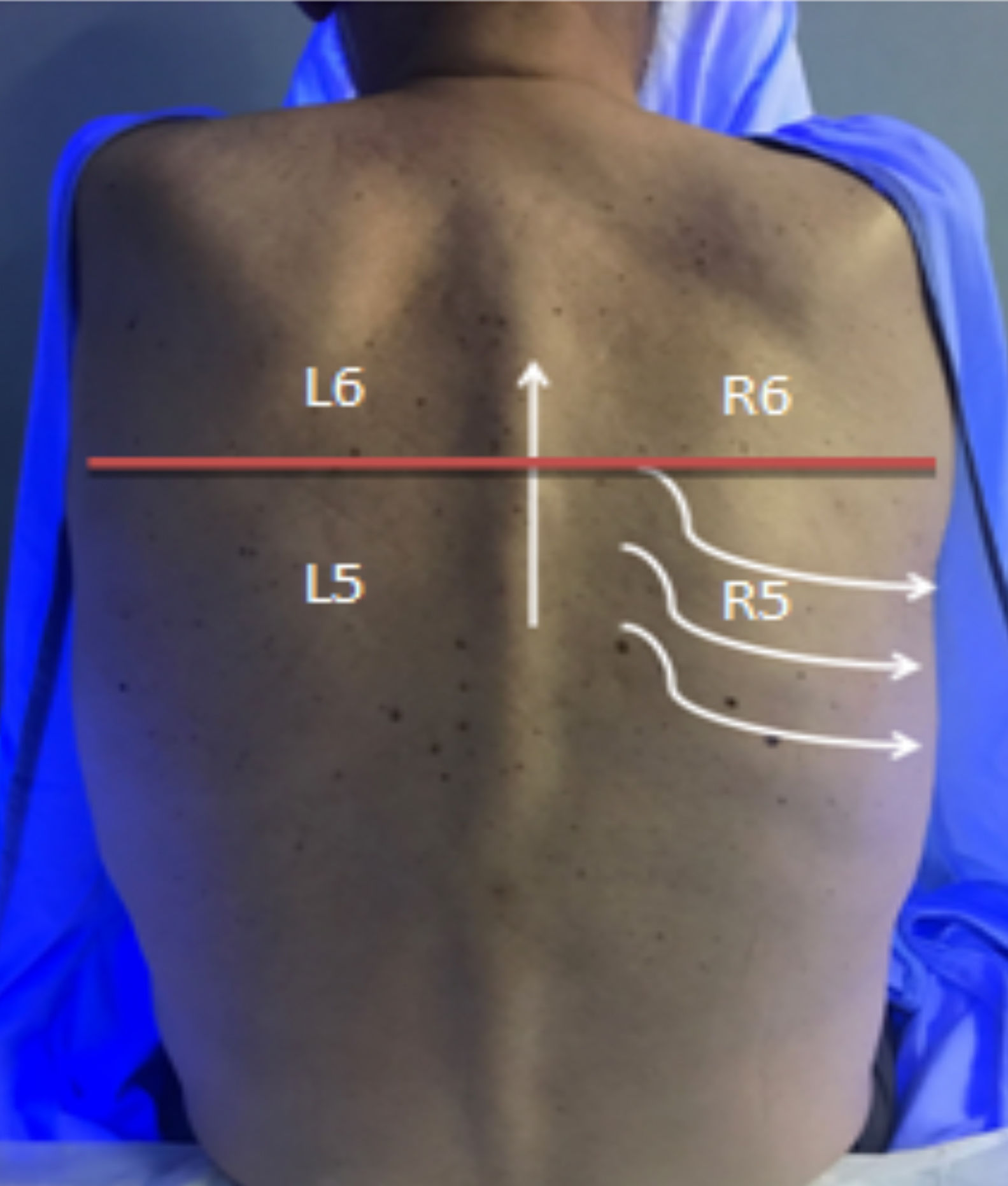
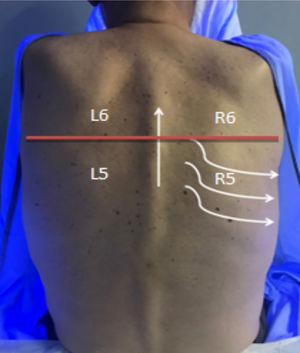
En cuanto a la zona posterior del tórax, se divide también en 4 zonas mediante la columna vertebral y una línea imaginaria que recorre horizontalmente la zona dorsal a la altura del borde inferior escapular y realizaremos la exploración de medial a lateral y de caudal a craneal (fig. 2).
Dado que la afectación es bilateral en el 87% y multilobar en el 78,8% de los casos1, la exploración ha de ser sistemática de todos los territorios. Comenzaremos siempre en las zonas anteriores más inferiores recorriendo longitudinalmente todo el espacio intercostal, de medial a lateral, y subiendo por los distintos espacios intercostales hasta cubrir todos los cuadrantes. Una vez explorada cada zona se anotarán (preferiblemente por un ayudante) en la hoja de recogida de datos los hallazgos ecográficos.
Hay dos tipos de escenarios: pacientes que permiten la sedestación y los que no la permiten por su situación clínica. En el caso de estos últimos no se explorarán los territorios posteriores, si bien es importante, al explorar las zonas laterales, deslizar la sonda lo más dorsalmente posible ya que se ven afectados en el 80% de los pacientes1.
Zonas subsidiarias de exploraciónPaciente que no permite sedestaciónDecúbito- -
R1: antero-inferior derecho.
- -
R2: antero-superior derecho.
- -
R3: axilar-inferior derecho.
- -
R4: axilar-superior derecho.
- -
L1: antero-inferior izquierdo.
- -
L2: antero-superior izquierdo.
- -
L3: axilar-inferior izquierdo.
- -
L4: axilar-superior izquierdo.
- -
R5: inferior derecho.
- -
R6: superior derecho.
- -
L5: inferior izquierdo.
- -
L6: superior izquierdo.
- -
R1: antero-inferior derecho.
- -
R2: antero-superior derecho.
- -
R3: axilar-inferior derecho.
- -
R4: axilar-superior derecho.
- -
L1: antero-inferior izquierdo.
- -
L2: antero-superior izquierdo.
- -
L3: axilar-inferior izquierdo.
- -
L4: axilar-superior izquierdo.
Presentes: normalidad.
Ausencia: se corresponde con patrón en vidrio deslustrado.
Líneas B: presencia de más de 3 líneas B por campo ecográficoB3: Separación de unos 3mm entre las líneas B medidas a la altura de la línea pleuralCorrespondencia con:
Patrón de vidrio deslustrado en TAC de tórax.
Condensación parenquimatosa subyacente que no contacta directamente con pleura visceral.
Edema alveolar: suele ser bilateral y distribuido de forma homogénea por ambos campos.
B7: Separación de unos 7mm entre las líneas B medidas a la altura de la línea pleuralCorrespondencia con:
Neumonía con afectación intersticial predominante.
Intersticial crónica.
Condensación parenquimatosaBroncograma aéreo.
Broncograma fluido.
Consolidación.
Vasculatura.
Línea pleuralNormal.
Engrosamiento difuso y/o nodular.
Discontinuidad.
Derrame pleuralEs muy raro y podría representar una neumonía bacteriana añadida a la infección vírica.
Evolución de los hallazgos ecográficos de la enfermedad4–8La afectación se sitúa de forma preferente en la zona posterior de los lóbulos inferiores (LLII), sobre todo en las etapas iniciales.
La evolución en el tiempo de los hallazgos ecográficos sería la siguiente (tabla 2):
- –
Líneas A: dado que estas líneas se relacionan con zonas de parénquima pulmonar sano suelen verse únicamente en los primeros días y en lóbulos superiores, desapareciendo con el paso de días y volviendo a aparecer en la fase de absorción, coincidiendo con la resolución del cuadro.
- –
Líneas B: en la etapa inicial se aprecia un aumento de líneas B de distribución focal y con una separación entre ellas, medida en la línea pleural, de unos 7mm (líneas B7). A medida que los infiltrados pulmonares van aumentando en tamaño y se distribuyen por el resto del parénquima, las líneas B se van fusionando y disminuyendo el espacio de separación entre ellas en la línea pleural hasta llegar a 3mm (líneas B3). Al mismo tiempo aumenta la distribución de las líneas B por ambos hemitórax hasta que comienza la fase de absorción en la que van desapareciendo progresivamente.
- –
Condensación parenquimatosa: no es típica en la fase temprana de la enfermedad. Puede aparecer a partir del cuarto día en zonas subpleurales. Comienza en forma de pequeñas consolidaciones que posteriormente van aumentando en número y tamaño, pudiendo apreciarse en esta fase zonas con broncograma aéreo y líquido. En la etapa de absorción comienzan a desaparecer de forma progresiva.
- –
Línea pleural: en los primeros días se visualizan zonas de pequeños engrosamientos difusos e irregulares. Con el avance de la enfermedad los engrosamientos se vuelven más nodulares con zonas de discontinuidad de la línea pleural que van desapareciendo si la enfermedad evoluciona favorablemente.
- –
Derrame pleural: es un hallazgo muy raro en todas las fases.
Hallazgos ultrasonográficos pulmonares según fase evolutiva de infección por COVID-19
| Hallazgos ecográficos en zonas patológicas | Etapa temprana (0-4 días) | Etapa progresiva (5-8 días) | Etapa máxima (9-13 días) | Etapa absorción (≥14 días) |
|---|---|---|---|---|
| Líneas A | EscasasLóbulos superiores (LLSS) | No | No | Reaparición progresiva |
| Líneas B | Predominante B7 focales | AumentoB3 y B7 | B3fusionadas y difusos | Resolución gradual |
| Condensación parenquimatosa | No | Subpleurales | Aumento | Resolución gradual |
| Línea pleural | Engrosamiento difuso | Engrosamiento difuso y/o nodularDiscontinuidad | Engrosamiento difuso y/o nodularDiscontinuidad | Resolución gradual |
| Derrame pleural | No | Raro | Raro | Raro |
Los autores declaran no tener ningún conflicto de intereses.