En el estudio de las partes inicial y final de la noche, la primera parte corresponde a la polisomnografía (PSG) estándar, que se utiliza para el establecimiento del diagnóstico del síndrome de apneas obstructivas durante el sueño, mientras que la segunda se usa para determinar el nivel adecuado de presión positiva continua de la vía aérea. El objetivo de nuestro estudio ha sido comparar los parámetros del sueño y respiratorios durante las primeras 3h de la noche con los valores de estos mismos parámetros obtenidos a lo largo del resto del sueño y durante toda la noche.
Pacientes y métodosEn el estudio participaron 45 pacientes. Todos ellos fueron evaluados mediante PSG estándar durante toda la noche. El registro y los datos de la PSG de cada paciente se dividieron en 2 períodos: PSG1, definido como las 3h iniciales del tiempo total de sueño, y PSG2, definido como el período restante. Después se calcularon por separado los datos correspondientes al sueño y a la respiración en los períodos PSG1 y PSG2, y se compararon entre sí y con los datos obtenidos en el registro de la PSG total (PSGt).
ResultadosEl porcentaje del tiempo total de sueño en las fases III-IV y el índice de apneas-hipopneas fueron significativamente mayores durante el período PSG1 que durante el período PSG2 (p<0,001), mientras que el porcentaje de tiempo del sueño con movimientos oculares rápidos (REM, de rapid eye movements) fue significativamente menor durante el primero que durante el segundo (p<0,001). De la misma manera, el porcentaje de tiempo en las fases III-IV fue significativamente mayor y el sueño REM fue significativamente menor durante el período PSG1, en comparación con el período PSGt (p<0,001), aunque no hubo diferencias significativas entre los períodos PSG1 y PSGt respecto al índice de apneas-hipopneas.
ConclusionesEl diagnóstico durante las primeras 3 h del sueño es fiable, pues refleja lo que ocurre a lo largo de toda la noche. Además, la presión positiva respiratoria óptima determinada durante la segunda mitad de la noche también es óptima respecto a la determinada en la primera mitad.
In a split-night study, the first part consists of standard polysomnography (PSG) for the diagnosis of obstructive sleep apnea syndrome while the second part is used to establish a suitable level of continuous positive airway pressure. The aim of our study was to compare the sleep and respiratory parameters during the first 3 hours of the night with the values found during the remainder of sleep and during the whole night.
Patients and methodsForty-five patients were included in the study. Each patient underwent a standard full-night PSG and the PSG data for each patient were divided into 2 periods: PSG1, defined as the initial 3 hours of the total sleep time and PSG2, defined as the remaining period. Sleep and breathing data from PSG1 and PSG2 were then separately computed and compared with each other and with data for the total sleep time (PSGt).
ResultsThe percentage of total sleep time in stage III-IV and the apnea–hypopnea index (AHI) were significantly higher and the percentage of time in rapid eye movement (REM) sleep was significantly lower during PSG1 than during PSG2 (P<.001). Similarly, the percentage of time in stage III-IV sleep was significantly higher and the percentage of REM sleep was significantly lower during PSG1 than during PSGt (P<.001), but there was no significant difference in the AHI between PSG1 and PSGt.
ConclusionThe diagnosis for the first 3hours of the night will give a reliable reflection of the whole night. In addition, optimal positive airway pressure titrated during the second half of the night is also optimal for the first half of the night.
La apnea del sueño es un trastorno frecuente, que afecta tanto a niños como a adultos y se caracteriza por episodios de apnea y períodos de hipopnea. Ambos problemas presentan una fisiopatología similar y habitualmente se han considerado conjuntamente respecto a su impacto sobre los pacientes. La forma más frecuente es la denominada apnea-hipopnea obstructiva durante el sueño, que se debe al colapso parcial o completo de la vía aérea superior. La gravedad del trastorno puede determinarse mediante el recuento del número de episodios de apneas e hipopneas por cada hora de sueño, esto es, el índice de apneas-hipopneas (IAH)1,2. En el Wisconsin Sleep Cohort Study se demostró que la prevalencia de un IAH mayor de 5 fue del 24% en los varones y del 9% en las mujeres de 30 a 60 años de edad3. La prevalencia de apnea del sueño sintomática (incluida la somnolencia diurna excesiva) en los varones y las mujeres fue del 4 y el 2%, respectivamente.
El abordaje diagnóstico convencional es la polisomnografía (PSG) realizada en el laboratorio de sueño y controlada por un técnico. La PSG requiere experiencia técnica y es un procedimiento que comporta una gran dedicación de tiempo y esfuerzo. La oportunidad para realizarla es un problema en muchos pacientes, dado que en el estudio de Wisconsin el 93% de las mujeres y el 82% de los varones con apnea del sueño de moderada a intensa no habían sido diagnosticados previamente4. En efecto, en muchos países del mundo los pacientes con sospecha de apnea del sueño tienen dificultades para acceder a los servicios diagnósticos y terapéuticos adecuados debido a la discrepancia entre la demanda de éstos y su capacidad de atenderla. En el estudio de Flemons et al5, publicado recientemente, se obtuvo información relativa a 5 países sobre el número de estudios del sueño realizados anualmente, el intervalo de espera de los pacientes para la realización de estos estudios y algunas de las estrategias utilizadas para abordar el desequilibrio entre la demanda de los estudios y la capacidad de oferta. La conclusión fue que la capacidad necesaria para evaluar a los pacientes no diagnosticados, durante un período de 10 años (el 82% del 9% de la población masculina y el 93% del 4% de la población femenina), sería de 555 PSG adicionales por cada 100.000 personas de la población general y año.
El tiempo necesario para examinar y tratar a los pacientes puede reducirse mediante los estudios de parte de la noche, en los que la PSG diagnóstica y la determinación de la presión positiva continua de la vía aérea (CPAP) se llevan a cabo la misma noche, en lugar de en 2 noches (una sesión de PSG durante toda la noche, seguida de la determinación de la CPAP durante una segunda noche). El protocolo recomendado por la American Academy of Sleep Medicine (AASM) para la realización de estudios de parte de la noche requiere que la PSG diagnóstica dure como mínimo 2h6. Documentación durante el componente diagnóstico de un IAH de al menos 40, o bien documentación de un IAH de 20-40 con factores clínicos asociados, como obstrucciones prolongadas y situaciones importantes de desaturación. Determinación de la CPAP durante más de 3h y documentación PSG de que la CPAP elimina o casi elimina los episodios respiratorios durante las fases del sueño con movimientos oculares rápidos (REM, de rapid eye movement) y no REM, incluso durante el sueño REM mientras el paciente permanece en decúbito supino.
En los estudios realizados con control se han comparado directamente los protocolos de parte de la noche y de noche completa en lo relativo a las tasas de precisión diagnóstica7, determinación de la CPAP necesaria8 y cumplimiento del tratamiento con ésta9. El objetivo de nuestro estudio ha sido comparar los parámetros del sueño y respiratorios durante las primeras 3h de la noche con los valores obtenidos durante las horas restantes de sueño y con los determinados a lo largo de toda la noche. De este modo se ha pretendido aclarar 2 cuestiones principales: a) ¿tiene la primera mitad del sueño nocturno las mismas características que el sueño nocturno completo y, si así fuera, sería posible diagnosticar todo lo que ocurre a lo largo de toda la noche evaluando únicamente la primera mitad de ésta?, y b) ¿tiene la segunda mitad del sueño nocturno características similares a las de la primera mitad y, si así fuera, sería posible solucionar los problemas que tienen lugar durante la primera mitad de la noche mejorando los parámetros de la segunda mitad?
Pacientes y métodosLa PSG se efectuó tras la evaluación clínica de los pacientes que cumplían los criterios siguientes: a) características clínicas clásicas del síndrome de apneas-hipopneas obstructivas durante el sueño (SAHOS: ronquidos sonoros durante la noche, somnolencia diurna excesiva y episodios de apnea nocturnos observados por una tercera persona), y b) puntuación en la escala Epworth mayor de 10.
Se realizó a todos los pacientes una PSG estándar de noche completa, en una habitación tranquila y aislada acústicamente de manera parcial, con valores estables de humedad y temperatura. Por lo general, el procedimiento se inició a las 22h y el técnico que lo llevó a cabo apagó la luz a solicitud del paciente. El procedimiento se interrumpió a las 7h. La PSG se efectuó mediante un sistema computarizado (Somnostar Alpha, Sensormedics, California EE.UU.) e incluyó seguimiento de: electrooculograma (2 canales), electroencefalograma (4 canales), electromiograma de los músculos submentonianos (2 canales), electromiograma del músculo tibial anterior de ambas piernas (2 canales), electrocardiograma y flujo de aire (con un termistor oronasal). Los movimientos torácicos y abdominales (2 canales) se registraron mediante pletismografía de inducción, y la determinación de la saturación arterial de oxihemoglobina (SaO2, un canal) se llevó a cabo mediante pulsioximetría con una sonda colocada en un dedo de la mano. Los registros se realizaron con una velocidad de papel de 10mm/s y la fase del sueño se puntuó según los criterios estándar de Rechtschaffen y Kales10. Los episodios de microdespertar se puntuaron según las definiciones aceptadas11. El índice de microdespertares se definió como el número de microdespertares por cada hora de sueño. La apnea se definió como una interrupción completa del flujo aéreo de al menos 10s de duración, y la hipopnea como una reducción mayor del 50% en una señal de flujo aéreo o en las señales respiratoria o abdominal de la pletismografía con inductancia respiratoria, con una disminución asociada de al menos el 3% en la SaO2 o con microdespertar. El IAH se definió como el número de episodios de apneas-hipopneas por cada hora de sueño. Cuando el IAH era de 5 o superior, se estableció el diagnóstico de SAHOS1. Se excluyó del estudio a los pacientes con una eficiencia del sueño (tiempo total de sueño/tiempo total en la cama × 100) menor del 75%, así como a aquéllos con trastornos del sueño distintos del SAHOS, tales como síndrome de resistencia de la vía aérea superior, síndrome de movimientos periódicos de las piernas y narcolepsia.
Se subdividió en 2 períodos el registro polisomnográfico de cada paciente: PSG1, que comprendía las 3h iniciales del tiempo total de sueño (TTS), y PSG2, definido como el período restante. Después se calcularon los datos relativos al sueño y la respiración en los períodos PSG1 y PSG2 y se compararon por separado respecto a los datos obtenidos en la PSG total (PSGt, durante toda la noche).
Análisis estadísticoSe utilizó la prueba de la t de Student para comparar los períodos PSG1 y PSG2, así como los períodos PSG1 y PSGt, respecto a las variables siguientes: tiempo de sueño en las fases I, II, III y IV (expresados en forma de porcentaje del TTS), sueño REM (expresado en forma de porcentaje del TTS), IAH, SaO2 media y SaO2 mínima durante el sueño. Las correlaciones entre los índices del patrón respiratorio durante los 3 períodos de estudio se evaluaron mediante el coeficiente de correlación de Pearson.
Todos los análisis se llevaron a cabo con el programa informático SPSS versión 11.5 para Macintosh (SPSS Inc., Chicago, IL, EE.UU.). Se consideró significativo un valor de p < 0,05.
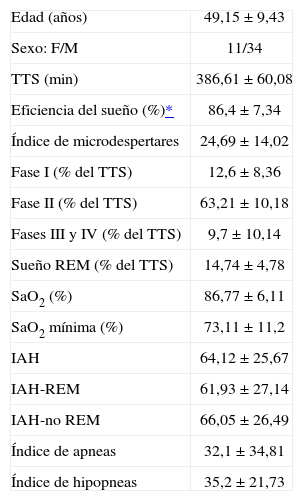
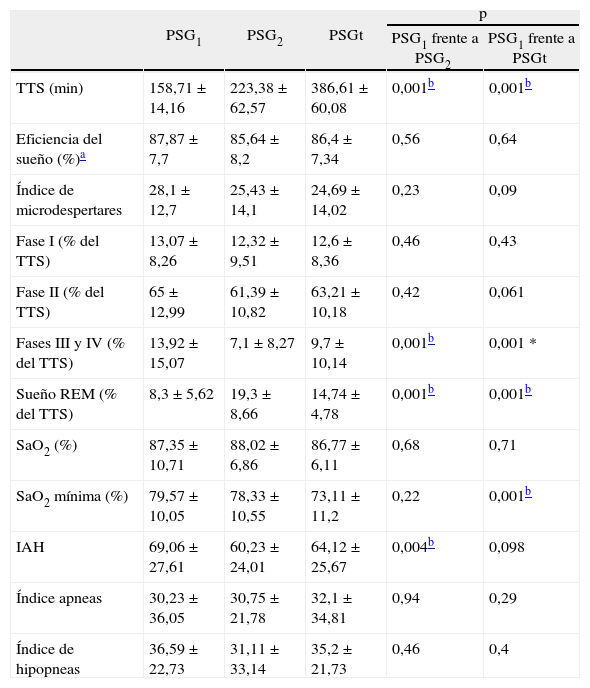
ResultadosEn el estudio participaron 45 pacientes, cuyos datos demográficos y polisomnográficos se recogen en la tabla I. En la tabla II se muestran por separado los datos del sueño y respiratorios correspondientes a los períodos PSG1, PSG2 y PSGt. En comparación con el período PSG2, durante el período PSG1 los valores de las fases III-IV y del IAH fueron significativamente mayores, mientras que el sueño REM fue significativamente menor (p < 0,001). De la misma manera, el valor de las fases III-IV fue significativamente mayor y el sueño REM significativamente menor durante el período PSG1 en comparación con el período PSGt (p < 0,001), pero no hubo diferencias significativas entre los períodos PSG1 y PSGt respecto al IAH. Tampoco se apreciaron diferencias significativas entre los períodos PSG1 y PSG2, ni entre los períodos PSG1 y PSGt, en lo relativo a la eficiencia del sueño, la SaO2 media y el índice de microdespertares.
Datos demográficos y polisomnográficos de los pacientes evaluados (n = 45)
| Edad (años) | 49,15 ± 9,43 |
| Sexo: F/M | 11/34 |
| TTS (min) | 386,61 ± 60,08 |
| Eficiencia del sueño (%)* | 86,4 ± 7,34 |
| Índice de microdespertares | 24,69 ± 14,02 |
| Fase I (% del TTS) | 12,6 ± 8,36 |
| Fase II (% del TTS) | 63,21 ± 10,18 |
| Fases III y IV (% del TTS) | 9,7 ± 10,14 |
| Sueño REM (% del TTS) | 14,74 ± 4,78 |
| SaO2 (%) | 86,77 ± 6,11 |
| SaO2 mínima (%) | 73,11 ± 11,2 |
| IAH | 64,12 ± 25,67 |
| IAH-REM | 61,93 ± 27,14 |
| IAH-no REM | 66,05 ± 26,49 |
| Índice de apneas | 32,1 ± 34,81 |
| Índice de hipopneas | 35,2 ± 21,73 |
Los datos corresponden a las medias ± desviación estándar, salvo en el caso del sexo, donde se indica el número.
F: femenino; IAH: índice de apneas-hipopneas; M: masculino; REM: movimientos oculares rápidos; SaO2: saturación arterial de oxihemoglobina, medida mediante pulsioximetría; TTS: tiempo total del sueño.
Datos de los pacientes estudiados mediante polisomnografía (n = 45) durante las 3h iniciales de sueño (PSG1), el tiempo restante de sueño (PSG2) y la noche completa (PSGt)
| PSG1 | PSG2 | PSGt | p | ||
| PSG1 frente a PSG2 | PSG1 frente a PSGt | ||||
| TTS (min) | 158,71 ± 14,16 | 223,38 ±62,57 | 386,61 ±60,08 | 0,001b | 0,001b |
| Eficiencia del sueño (%)a | 87,87 ±7,7 | 85,64 ±8,2 | 86,4 ± 7,34 | 0,56 | 0,64 |
| Índice de microdespertares | 28,1 ± 12,7 | 25,43 ± 14,1 | 24,69 ±14,02 | 0,23 | 0,09 |
| Fase I (% del TTS) | 13,07 ± 8,26 | 12,32 ±9,51 | 12,6 ±8,36 | 0,46 | 0,43 |
| Fase II (% del TTS) | 65 ± 12,99 | 61,39 ±10,82 | 63,21 ± 10,18 | 0,42 | 0,061 |
| Fases III y IV (% del TTS) | 13,92 ±15,07 | 7,1 ± 8,27 | 9,7 ±10,14 | 0,001b | 0,001 * |
| Sueño REM (% del TTS) | 8,3 ± 5,62 | 19,3 ± 8,66 | 14,74 ±4,78 | 0,001b | 0,001b |
| SaO2 (%) | 87,35 ± 10,71 | 88,02 ±6,86 | 86,77 ±6,11 | 0,68 | 0,71 |
| SaO2 mínima (%) | 79,57 ± 10,05 | 78,33 ± 10,55 | 73,11 ± 11,2 | 0,22 | 0,001b |
| IAH | 69,06 ±27,61 | 60,23 ± 24,01 | 64,12 ±25,67 | 0,004b | 0,098 |
| Índice apneas | 30,23 ± 36,05 | 30,75 ±21,78 | 32,1 ± 34,81 | 0,94 | 0,29 |
| Índice de hipopneas | 36,59 ± 22,73 | 31,11 ±33,14 | 35,2 ±21,73 | 0,46 | 0,4 |
Los datos corresponden a las medias ± desviación estándar.
IAH: índice de apneas-hipopneas; REM: movimientos oculares rápidos; SaO2: saturación arterial de oxihemoglobina, medida mediante pulsioximetría; TTS: tiempo total del sueño.
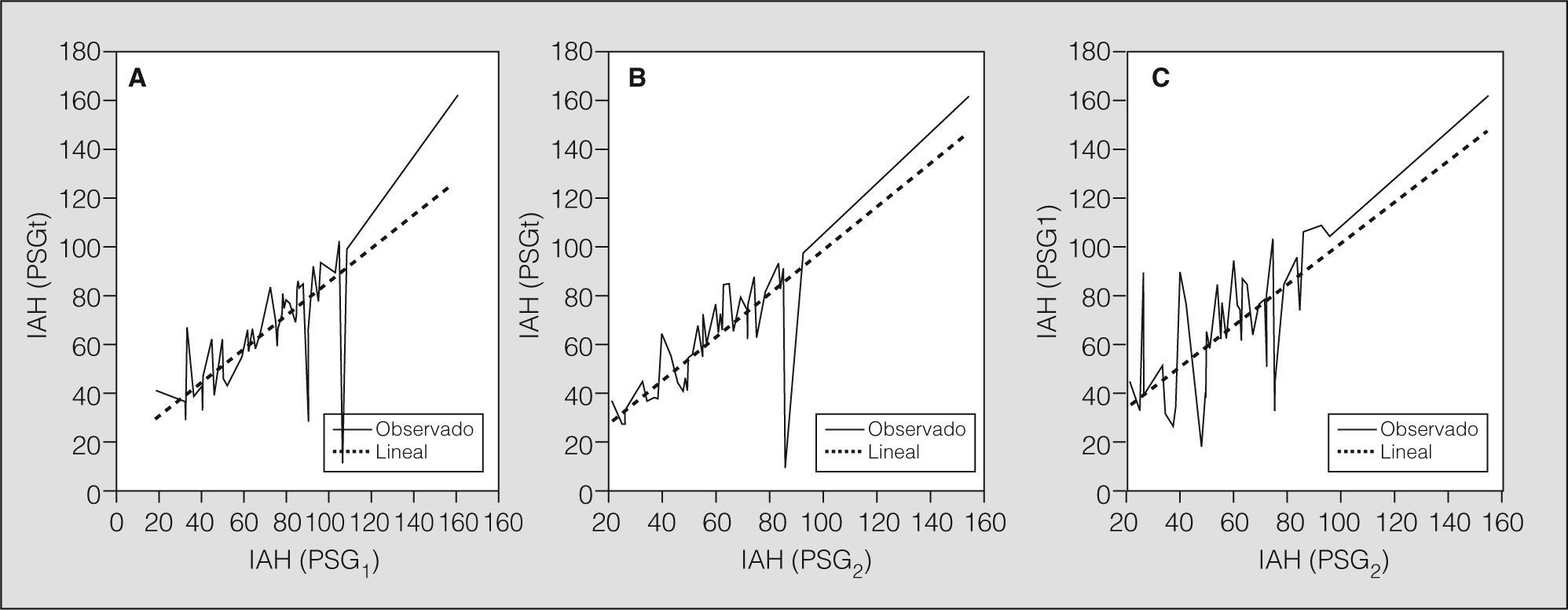
Se demostraron correlaciones estrechas entre el IAH medio a lo largo de toda la noche y el IAH en las fases PSG1 y PSG2, y también hubo correlación entre el IAH medio de la primera y la segunda partes de la noche (fig. 1).
DiscusiónLa fiabilidad del estudio de parte de la noche se ha evaluado sólo en unos pocos estudios. Yamashiro y Kryger8 estudiaron a 107 pacientes con respiración alterada durante el sueño para confirmar la hipótesis de que durante el protocolo de estudio de parte de la noche podía determinarse el nivel de CPAP efectiva. Dichos investigadores señalaron que el protocolo de estudio de parte de la noche podría ser tan eficaz para reducir el IAH como el protocolo de noche completa, especialmente en los pacientes con un IAH mayor de 40. McArdle et al7 evaluaron a 138 pacientes, con estudio de parte de la noche en 46 y de noche completa en 92. Según sus resultados, el estudio de parte de la noche dio lugar al uso de CPAP y a unas puntuaciones en la escala Epworth tras tratamiento similares al estudio de PSG diagnóstica y evaluación de la CPAP durante toda la noche. La conclusión fue que, dada la reducción de las hospitalizaciones nocturnas en el centro del sueño, sin un incremento de la intervención de seguimiento, el protocolo de estudio de parte de la noche podría generar un ahorro económico significativo. Por su parte, Iber et al12 observaron que el estudio de una sola noche era suficiente para establecer el tratamiento efectivo con CPAP en el 78% de sus pacientes, además de ofrecer un ahorro considerable de recursos en comparación con los estudios de noche completa. Sanders et al13 demostraron que el estudio de parte de la noche es un método apropiado para evaluar las alteraciones de la respiración durante el sueño, tras encontrar una correlación estrecha de los índices de alteración respiratoria entre los datos obtenidos en la primera parte del sueño y los registrados durante toda la noche. En su estudio no se efectuó ningún análisis para comparar las partes primera y segunda del sueño.
En nuestro estudio se ha hallado una correlación estrecha entre el IAH de la PSGt y el de la PSG1; entre el IAH de la PSGt y el de la PSG1, y entre el IAH de la PSG1 y el de la PSG2. El IAH fue mayor durante el período PSG1 que durante el período PSG2, lo que indica que la enfermedad se manifiesta de manera más intensa durante la primera parte del sueño y que, por tanto, la PSG durante las primeras 3h del sueño es un método apropiado para evaluar las alteraciones respiratorias durante del sueño. No hubo diferencias entre los períodos PSG1 y PSGt respecto al valor del IAH. Así pues, el diagnóstico efectuado durante la primera parte del sueño puede reflejar lo que ocurre durante el sueño completo. En nuestro estudio se ha demostrado que el porcentaje de las fases III-IV es mayor durante la primera parte del sueño y que la cantidad de sueño REM lo es en la segunda, lo que está en concordancia con la concepción clásica de la distribución de las fases del sueño14. En el estudio de Fanfulla et al15 se compararon los registros de PSG obtenidos durante las partes primera y segunda de la noche. Estos investigadores demostraron que en los pacientes que presentan sueño de fase REM durante la primera parte de la noche el IAH en el PSG de noche completa fue muy homogéneo. Por el contrario, los pacientes sin sueño de fase REM durante la primera parte presentaron valores inferiores de IAH durante la primera parte de la noche. En nuestro estudio no se evaluaron las conclusiones de Fanfulla et al15 porque no hubo ningún paciente sin sueño REM durante el estudio PSG1. Además, en la comparación de los períodos PSG1 y PSG2, el IAH fue mayor durante el primero de ellos, mientras que el período REM fue inferior. De la misma manera, al comparar los períodos PSG1 y PSGt no se observaron diferencias significativas en el IAH, aunque el sueño REM fue inferior en el período PSG1.
Otro resultado obtenido en nuestro estudio es la ausencia de diferencias significativas entre los períodos PSG1 y PSG2 respecto a la eficiencia del sueño, el índice de microdespertares y la SaO2 media. La similitud, durante los períodos PSG1 y PSG2, entre los valores de SaO2 media y el índice de microdespertares asociados a la apnea e hipopnea nos lleva a considerar la posibilidad de resolver los problemas que tienen lugar durante la primera mitad de la noche mediante la titulación por la CPAP durante la segunda mitad.
Aunque hay datos que indican que en la mayor parte de los pacientes es posible diagnosticar adecuadamente el SAHOS y calcular la CPAP efectiva mediante la PSG realizada durante la mitad de la noche16,17, en otros estudios se han considerado los problemas relativos al grado de aceptación y al cumplimiento del tratamiento con CPAP por parte de los pacientes tras la PSG realizada únicamente durante parte de la noche. Fleury et al9 llegaron a la conclusión de que los pacientes a quienes se realizan estudios durante parte de la noche presentan un uso de la CPAP similar al de los pacientes a los que se efectúan estudios de noche completa. La experiencia de Fleury et al9 se vio reforzada por los datos que aportaron Raucher et al18, que observaron un grado de cumplimiento de la CPAP a largo plazo del 80% y una tasa diaria de uso en el hogar de 6,5h tras el estudio polisomnográfico de parte de la noche. No obstante, en el estudio de Strollo et al19, de pequeño tamaño, el protocolo de PSG de parte de la noche se acompañó de una tasa de aceptación de la CPAP del 62-67%, inferior a la observada por Fleury et al9. En nuestro trabajo no se evaluaron el grado de aceptación ni el cumplimiento de la CPAP por parte de los pacientes a quienes se aplicó el protocolo de PSG de parte de la noche.
Por otro lado, en nuestro estudio participaron pacientes con SAHOS, para cuyo diagnóstico se utilizó el criterio de un IAH mayor 5, de acuerdo con la AASM1. Si se hubieran aplicado los criterios de la Sociedad Española de Neumología y Cirugía Torácica (SEPAR)20,21 para identificar los episodios respiratorios durante las pruebas de PSG nocturna (para el diagnóstico del SAHOS el IAH debe ser superior a 10), nuestros resultados habrían sido distintos.
En conclusión, el diagnóstico establecido durante las primeras 3h de la noche es fiable, pues refleja lo que ocurre a lo largo de toda la noche. Además, es posible que la CPAP óptima determinada durante la segunda mitad de la noche sea válida respecto a la primera mitad de la misma. Sin embargo, en nuestro estudio no se evaluaron los grados de aceptación y cumplimiento de la CPAP por parte de los pacientes. En comparación con el protocolo de 2 noches, uno de los inconvenientes principales del protocolo de evaluación durante parte de la noche es el hecho de que el paciente se despierta en la transición a la segunda mitad de la noche.