La neumonía organizada es una entidad clínico-histológica bien diferenciada, que suele presentarse de forma subaguda con síntomas respiratorios e infiltrados pulmonares. Puede ser de causa desconocida (criptogenética) o estar asociada a distintas enfermedades, infecciones o fármacos. El diagnóstico de seguridad requiere la demostración de focos de neumonía organizada en muestras de biopsia pulmonar. Presentamos el caso de un paciente de 49 años con infección por el virus de la hepatitis C en tratamiento con peginterferón α-2b que desarrolló un cuadro de tos seca, fiebre, disnea e infiltrados pulmonares en vidrio deslustrado, y a quien se diagnosticó por biopsia pulmonar abierta de neumonía organizada. Con la retirada del peginterferón y tratamiento con corticoides desaparecieron los síntomas y los infiltrados pulmonares. En nuestro conocimiento, éste es el Segundo caso comunicado de neumonía organizada en relación con peginterferón α-2b.
Organizing pneumonia is a well-differentiated clinical and histologic entity whose onset is usually subacute with respiratory symptoms and pulmonary infiltrates. Its origin may be unknown (cryptogenic) or it may be associated with various medical conditions, infectious diseases, or drugs. Diagnosis is confirmed by the presence of foci of organizing pneumonia in lung biopsy specimens. Our patient was a 49-year-old man infected with the hepatitis C virus who was receiving pegylated interferon alfa-2b. He presented with dry cough, fever, dyspnea, and ground glass pulmonary infiltrates. After an open lung biopsy, he was diagnosed with organizing pneumonia. When pegylated interferon was discontinued and corticosteroids started, the symptoms and pulmonary infiltrates disappeared. To our knowledge, this is the second report of organizing pneumonia related to pegylated interferon alfa-2b.
La neumonía organizada es una enfermedad pulmonar intersticial bien conocida desde hace más de 20 años1 y puede ser de causa desconocida (criptogenética) o bien secundaria a diferentes enfermedades o fármacos. Describimos el caso de un paciente con infección por el virus de la hepatitis C (VHC) que 6 meses después de iniciar tratamiento con peginterferón α-2b (Peg-IFN) presentó un cuadro subagudo de tos seca, fiebre y disnea de esfuerzo, y al que se diagnosticó por biopsia pulmonar abierta de neumonía organizada. Una exhaustiva búsqueda bibliográfica en MEDLINE (período 1976-2006; palabras clave: "interferon alpha-2b" and "bronchiolitis oliterans organizing pneumonia" and "hepatitis C") y en la página web Pneumotox®2 reveló que hasta la fecha se ha comunicado un solo caso de neumonía organizada en relación con el tratamiento de la hepatitis C con Peg-IFN3.
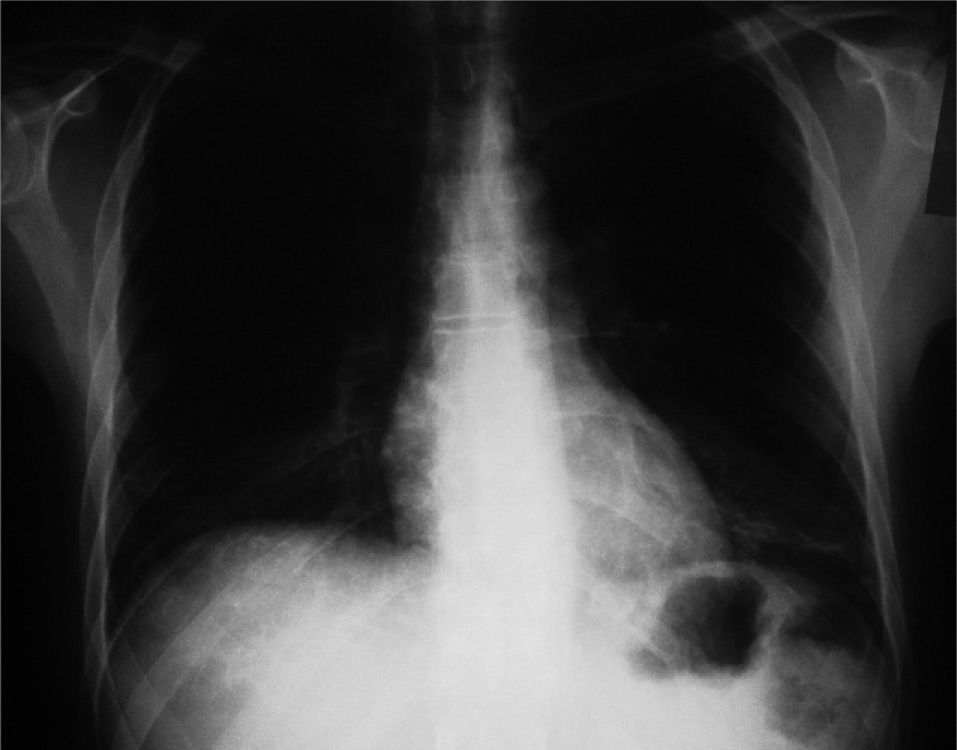
Observación clínicaVarón de 49 años, sin alergias conocidas, exfumador, diagnosticado a los 35 años de edad de infección crónica por el VHC (genotipo 1b) por análisis practicado antes de una donación de sangre. Ante la presencia de elevación persistente de transaminasas (valores de aspartato-transaminasa y alaninaaminotransferasa entre 50 y 100 U/l) y carga vírica plasmática (cuantificación del ARN del VHC), 6 meses antes del ingreso el paciente inició tratamiento con Peg-IFN (1,5μg/kg/semanal por vía subcutánea) y ribavirina (1.000mg/día por vía oral), con buena tolerancia y cumplimiento iniciales y sin necesidad de reducir las dosis al no aparecer efectos adversos. El paciente consultó por un cuadro de 2 semanas de evolución de disnea progresiva hasta hacerse de pequeños esfuerzos, junto a tos seca persistente y fiebre. Las constantes vitales al ingresar fueron las siguientes: presión arterial de 91/65mmHg, frecuencia respiratoria de 32 respiraciones/min, frecuencia cardíaca de 87 lat/min y temperatura axilar de 36°C. En la exploración física destacaron crepitantes gruesos en ambas bases pulmonares; el resto de la exploración física general fue normal. Ante los hallazgos en la gasometría arterial (con fracción inspiratoria de oxígeno de 0,21, pH de 7,42, presión arterial de oxígeno de 62mmHg, presión arterial de anhídrido carbónico de 34mmHg, HCO3 de 22mM/l) y la radiografía de tórax (fig. 1) se decidió el ingreso para estudio y tratamiento. Durante el ingreso se realizó una analítica general que mostró los siguientes valores: velocidad de sedimentación globular de 24mm/h, hemograma sin alteraciones, bioquímica general (incluía glucosa, urea, creatinina, sodio, potasio, calcio, aspartato-transaminasa, alanina-aminotransferasa, gammaglutamil transpeptidasa, fosfatasa alcalina, lactatodeshidrogenasa, creatincinasa, colesterol total, triglicéridos, proteínas totales, albúmina y hormona tirotropa) con todos los parámetros dentro de los límites de la normalidad, serologías (enzimoinmunoanálisis para el virus de la inmunodeficiencia humana, inmunoglobulinas G y M para Mycoplasma pneumoniae, Coxiella burnetii y Chlamydia pneumoniae negativas), anticuerpos antinucleares y anticitoplásmicos del neutrófilo negativos y enzima de conversión de la angiotensina dentro de los valores normales. El antígeno de Legionella en orina fue negativo. Se realizó una tomografía computarizada de tórax que mostró infiltrados parcheados en vidrio deslustrado, difusos y bilaterales de predominio en ambas bases, además de una fibrobroncoscopia con lavado broncoalveolar que mostró la siguiente celularidad: un 55% de macrófagos, un 40% de linfocitos y un 5% de eosinófilos; los cultivos para bacterias, micobacterias y hongos fueron negativos. Finalmente se realizó una biopsia pulmonar abierta que puso de manifiesto focos de neumonía organizada. Al ingresar el paciente se había interrumpido el tratamiento para el VHC e iniciado tratamiento antibiótico empírico (2g/24h de ceftriaxona por vía intravenosa y 500mg/12h de claritromicina por vía oral) sin ninguna mejoría clínica. Una vez descartadas razonablemente las causas infecciosas mediante cultivos y serologías, y al disponer del resultado de la biopsia pulmonar, se retiró el antibiótico y se inició metilprednisolona, a dosis de 1mg/kg de peso cada 24h por vía intravenosa, con lo que el paciente experimentó una rápida mejoría clínica y se le pudo dar de alta en tratamiento con prednisona por vía oral (1mg/kg de peso durante un mes, con posterior pauta descendente hasta la retirada del tratamiento a los 6 meses). A los 9 meses de seguimiento se encuentra asintomático y con completa resolución de los infiltrados pulmonares.
DiscusiónLa neumonía organizada (antes denominada bronquiolitis obliterante con neumonía organizada o BOOP) es una entidad clínico-histológica bien diferenciada desde hace 2 décadas1,4, con manifestaciones clínicas subagudas (tos, disnea y fiebre) junto a la presencia de infiltrados pulmonares alveolares y/o intersticiales (a veces migratorios e incluso recidivantes) y alteraciones en el lavado broncoalveolar que pueden ayudar a establecer el diagnóstico (linfocitosis marcada, a menudo asociada a neutrofilia y/o eosinofilia). Para establecer el diagnóstico de seguridad se requiere la demostración de focos de neumonía organizada en las muestras de biopsia transbronquial o quirúrgica. Puede ser secundaria a infecciones, neumonías por aspiración, inhalación de tóxicos, toxicidad por fármacos (bleomicina, derivados ergóticos, nitrofurantoína, fenitoína, amiodarona, carbamacepina, ciclofosfamida, etc.)2,5, radioterapia, enfermedades del colágeno, vasculitis, enfermedades inflamatorias de intestino, etc. Cuando no hay ningún trastorno asociado se denomina neumonía organizada criptogenética1,4. El Peg-IFN es un tratamiento cada vez más utilizado no sólo para tratar la infección por el VHC, sino también otras enfermedades (p. ej., la esclerosis múltiple), por lo que es importante que los clínicos conozcan sus efectos secundarios, entre los cuales los más frecuentes son los síntomas seudogripales, psiquiátricos y hematológicos6. Con menor frecuencia se ha descrito toxicidad pulmonar en relación con el Peg-IFN, siendo la mayoría casos de sarcoidosis7 y neumonitis intersticial8. De forma excepcional se han descrito también casos de neumonitis eosinofílica, exacerbaciones del asma y derrame pleural2. Nuestro paciente presentaba tos seca, disnea y fiebre desde hacía 2 meses, crepitantes secos a la auscultación respiratoria e infiltrados pulmonares intersticiales de predominio basal. Ante la negatividad de las pruebas microbiológicas, la falta de respuesta al tratamiento antibiótico y la rápida respuesta al tratamiento con corticoides se llegó al diagnóstico de neumonía organizada, que se confirmó con una biopsia pulmonar. Al retirar el Peg-IFN e iniciar tratamiento con corticoides los síntomas y los infiltrados pulmonares desaparecieron. Ante esto, y dada la ausencia de otra enfermedad médica u otros fármacos que puedan asociarse a la neumonía organizada, llegamos a la conclusión de que el Peg-IFN puede ser la causa de dicho trastorno, aunque no pueda demostrarse directamente la causalidad. En nuestro conocimiento, después de la búsqueda bibliográfica antes mencionada, éste es el segundo caso comunicado de neumonía organizada asociada al tratamiento con Peg-IFN.