Mujer de 21 años diagnosticada de cirrosis criptogénica desde los 9 años de edad, que presentó empiema izquierdo posneumónico que no remitió con el tratamiento médico convencional y evolucionó con fistulización hacia la piel en el séptimo espacio intercostal a nivel subescapular izquierdo. Se realizó una ventana torácica abierta y al sexto día se envió a su domicilio con colocación de sistema cerrado de succión portátil, con cambios cada 4días del material hasta la obliteración total de la cavidad (92 días). Se observó por imagen una expansión completa del pulmón y se realizó reconstrucción de la pared torácica con barras de titanio. La alta mortalidad del empiema, en los pacientes con hepatopatías, requiere la implementación y la búsqueda de nuevas terapias adyuvantes, como la utilización del sistema cerrado de succión y la reconstrucción con barras de titanio. Para una adecuada evaluación, se requieren estudios controlados con una serie de casos amplia.
The patient is a 21-year-old female, diagnosed with cryptogenic cirrhosis at the age of 9. She presented with left post-pneumonic empyema that did not remit with conventional medical management and evolved with fistulization to the skin in the 7th intercostal space in the left subscapular region. We performed an open thoracic window procedure, and on the 6th day the patient was sent home with a portable vacuum-assisted closure device, with changes of the material every 4 days until the cavity was completed obliterated (92 days). Imaging tests showed full expansion of the lung, and chest wall reconstruction was performed with titanium rods. The high mortality of empyema in patients with liver disease requires both implementing and searching for new adjuvant therapies, like the use of vacuum-assisted closure systems and reconstruction with titanium rods. Controlled studies with a wide range of cases are needed for proper evaluation.
El uso intratorácico del sistema cerrado de succión (Vacuum Assisted Closure™, VAC™) es una técnica novedosa con evidencia acumulada que lo propone como un tratamiento adyuvante en los pacientes con ventana torácica por empiema recidivante o persistente, ya que puede disminuir la morbilidad y la estancia intrahospitalaria; esta evidencia ha sido obtenida principalmente en pacientes con empiema posterior a resección pulmonar1.
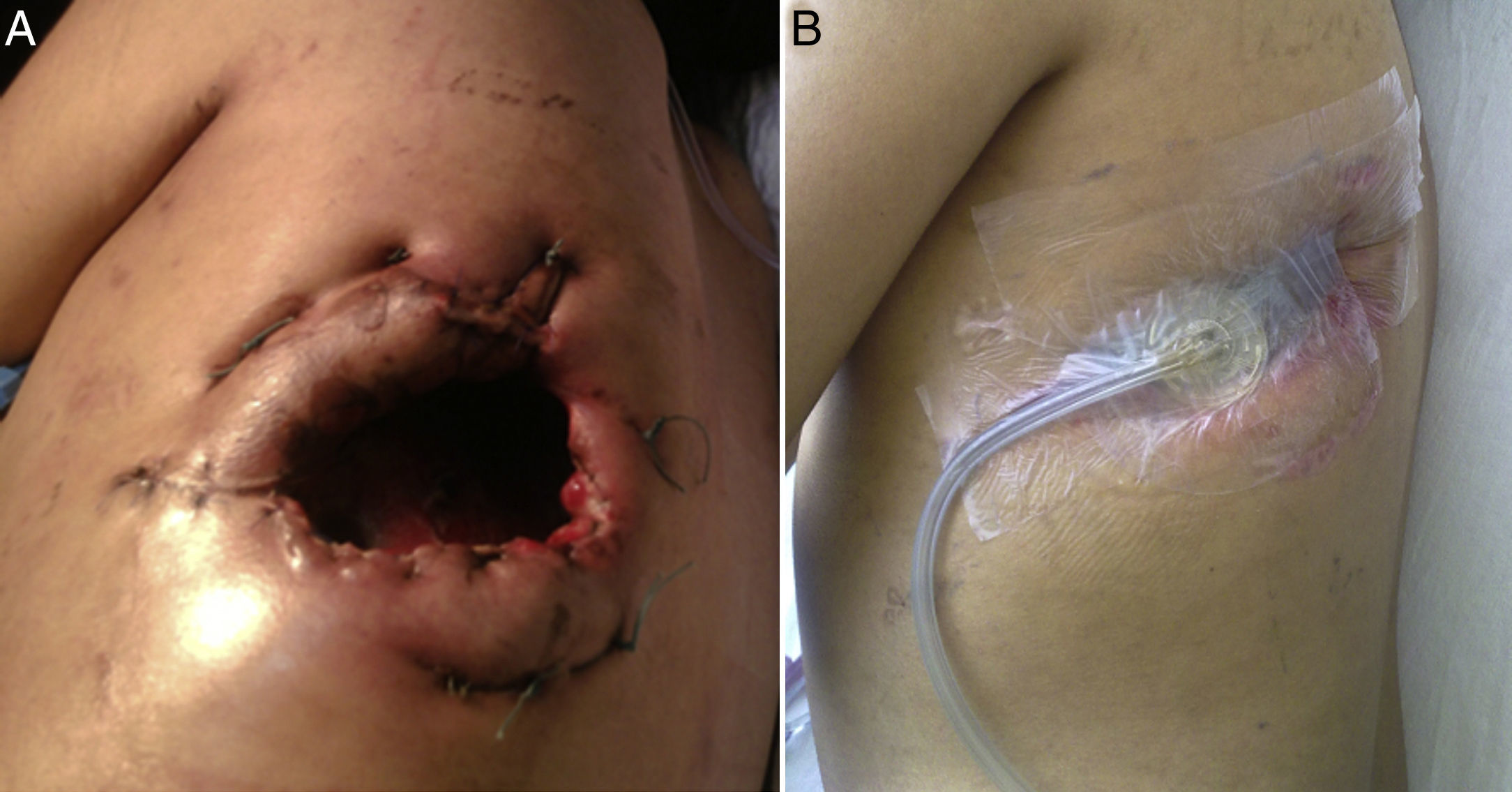
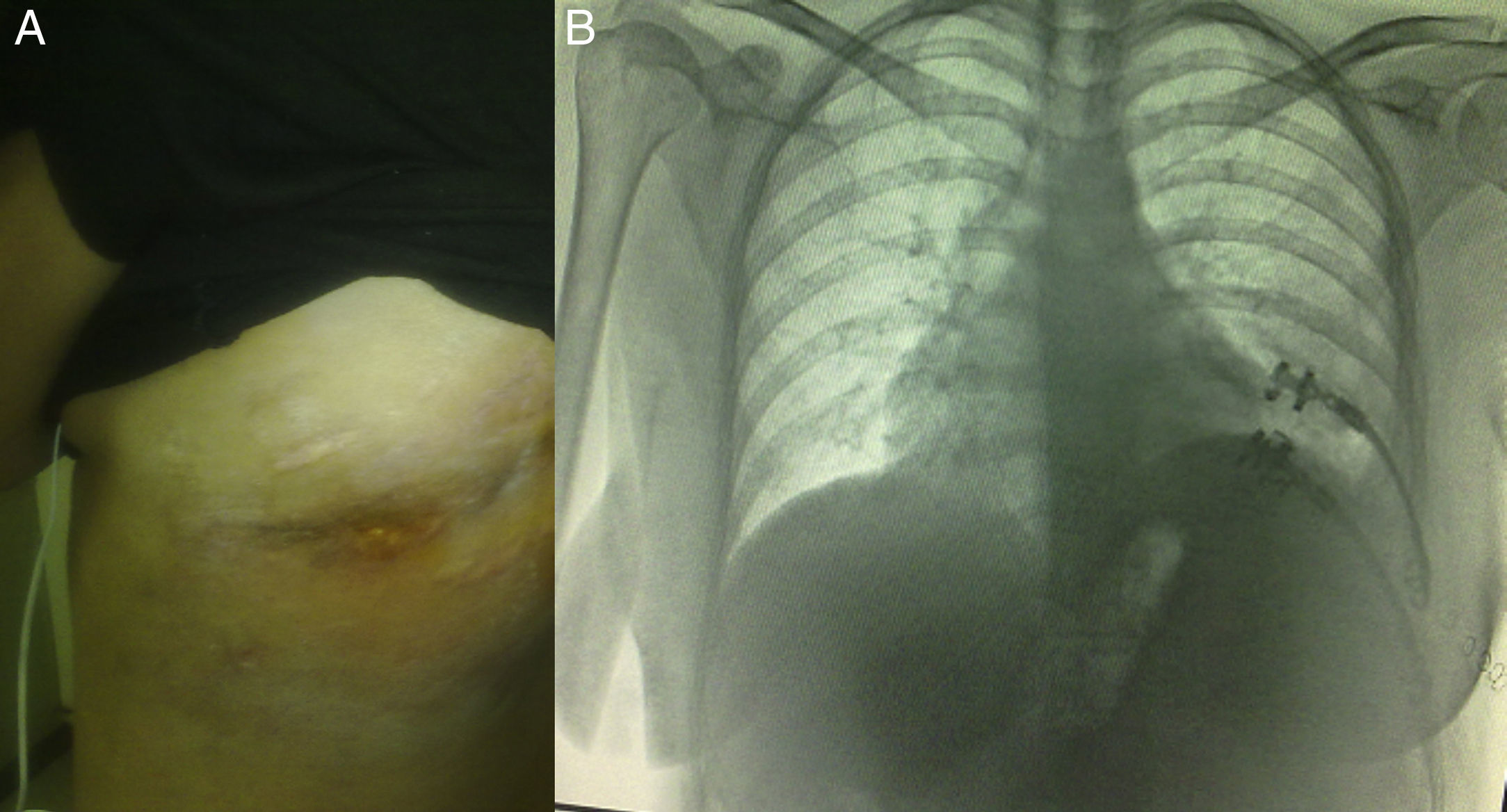
Observación clínicaMujer de 21 años, con cirrosis criptogénica diagnosticada desde los 9 años de edad, con síndrome de hipertensión portal y varices esofágicas. Cuatro meses antes de acudir a nuestro servicio fue diagnosticada de empiema izquierdo posneumónico, que no remitió con la terapia antimicrobiana; se realizó toracocentesis y colocación de tubo de drenaje torácico en 2 ocasiones, y evolucionó con infiltración de la pared y fistulización hacia la piel en el séptimo espacio intercostal a nivel subescapular izquierdo. Ingresó en nuestro servicio con deterioro del estado general y dolor torácico de características pleuríticas en el hemitórax izquierdo. A la exploración física destacaba semiología de derrame pleural en la mitad inferior de hemitórax izquierdo, con frecuencia cardiaca de 98latidos/min, frecuencia respiratoria de 30/min, presión arterial de 90/60mmHg y temperatura de 38,2°C; en el examen analítico los leucocitos eran de 15.900/mm3. Se clasificó como de severidad hepática CHILD-PUGHB. En el cultivo del empiema creció Staphylococcus haemolyticus. Las pruebas de imagen (radiografía de tórax y tomografía computarizada) objetivaron imagen de derrame posterobasal que ocupaba el 60% de la cavidad pleural del hemitórax izquierdo, pulmón colapsado y paquipleuritis. Se decidió realizar una ventana torácica abierta (fig. 1) resecando 9cm de longitud de los arcos costales 8 y 9 en su región posterolateral. Durante el procedimiento se encontró abundante material purulento, pleura visceral y parietal engrosadas de aproximadamente 1cm de espesor, y no se realizó decorticación; osteomielitis del octavo arco costal y trayecto fistuloso a nivel del séptimo espacio intercostal. La intervención también consistió en el relleno de la cavidad pleural con compresas durante 48h; esta decisión se tomó a partir de que la tromboelastografía reportara tiempo de reacción (R) y de coagulación (K) muy prolongados. Posteriormente se revisó la cavidad y se repitió el relleno con compresas durante 48h más; al cuarto día se colocó un sistema VAC™ intratorácico (IT) y al sexto día se le dio de alta a su domicilio con un sistema VAC™ portátil; utilizamos presión inicial de succión de 75mmHg e intensidad de 30mmHg durante 2días y posteriormente se incrementó la succión a 125mmHg e intensidad de 40mmHg; presentó disminución paulatina de los gastos, de un promedio de 300ml por día durante las 2 primeras semanas hasta un promedio de 300ml cada 4 días (al mes y medio de tratamiento). El cambio de esponja se realizó cada 4días, y se utilizó esponja tipo VAC Granufoam SilverMR Large Dressing (esponja gris larga impregnada de plata), con la que se observó mejoría evidente a los 15 días de su uso. Se reportó con una cavidad residual inicial de 18×9×9cm y evolucionó a una cavidad de 8×2×2cm al mes y medio de su utilización, por lo que se decidió continuar VAC™-IT por mes y medio más hasta la obliteración total de la cavidad (92 días). La imagen radiográfica mostró la expansión completa de pulmón. Durante la evolución se realizaron cultivos seriados por biopsia, al mes y a los 2 meses, con crecimiento de Staphylococcus haemolyticus y Staphylococcus hominis, por lo que se completó el esquema de antibioticoterapia ambulatoria, con un último cultivo a los 3 meses sin crecimiento. Se programó para reconstrucción de la pared torácica con barras de titanio (sistema STRATOS™), que se llevó a cabo sin complicaciones, evolucionando satisfactoriamente y con el alta hospitalaria a la semana del procedimiento. Las pruebas funcionales respiratorias de nuestra paciente mostraron preoperatoriamente una FVC del 54% del predicho y un FEV1 del 50% del predicho, y 4 meses tras la reconstrucción de la pared la FVC fue del 87% del predicho y el FEV1 del 92% del predicho. Los controles en consulta externa, hasta 8 meses después, no mostraron complicaciones (fig. 2).
La cirrosis hepática se considera como una contraindicación para la realización del lavado y decorticación, por las frecuentes anormalidades hemostáticas y nutricionales, lo cual incrementa de modo importante la morbimortalidad2-5. Chen et al. registraron una mortalidad del 31,5 al 48,4% cuando estos pacientes se tratan con toracocentesis o drenaje por sondas, y del 21,1% cuando se tratan con toracoscopia, sin encontrar diferencia significativa en la tasa de mortalidad al utilizar el tratamiento toracoscópico vs no-toracoscópico5. Varker y Ng6 describieron por primera vez en 2006 el uso exitoso de VAC™ intratorácico (VAC™-IT) en un empiema poslobectomía; desde entonces se han reportado casos aislados y series de casos con uso de VAC™-IT, principalmente en el empiema poslobectomía o posneumonectomía, sugiriéndose como un tratamiento adyuvante para el manejo de los empiemas en pacientes complicados, que disminuye la estancia intrahospitalaria y reduce potencialmente la morbilidad1,6-14. No encontramos informes del uso de VAC™ en la ventana torácica realizada por empiema en pacientes con cirrosis hepática.
El uso de VAC™-IT en nuestro caso significó un alta hospitalaria pronta y un seguimiento ambulatorio; durante el cambio de esponjas del sistema no se requirió analgesia o sedación, y la paciente refirió siempre un dolor tolerable. En comparación con los estudios de Palmen et al.12 y Saadi et al.13, en los que registran un tiempo de uso de VAC™ de 39±17 días (rango, 6 a 66 días), debemos recalcar que estos autores no describen las dimensiones de la cavidad residual ni el grado de paquipleuritis; al respecto, recordamos el tamaño de la ventana realizado en nuestra paciente (diámetros de 9×6,5cm), el espacio residual pleural intratorácico de 21×9×9cm, una corteza pleural de aproximadamente 1cm de promedio y en la cual no se realizó decorticación, y además decidimos el uso de VAC™-IT hasta la obliteración de la cavidad residual y la expansión completa pulmonar, factores que contribuyeron al tiempo de terapia con el sistema cerrado de succión. Es importante señalar que Rocco et al.15 han informado 2 casos en los que tuvieron que interrumpir definitivamente el sistema de succión debido a dolor torácico agudo y a la hipotensión, y describieron un caso en el que la esponja utilizada se adhirió al tejido en granulación y solo pudo retirarse bajo toracoscopia.
La reconstrucción de la pared torácica posterior a la realización de ventana torácica se ha reportado principalmente utilizando colgajos musculares (mioplastia) y con las toracomioplastias16-19. Al observar la adecuada expansión pulmonar de nuestro paciente posterior al uso de VAC™-IT, decidimos la reconstrucción de la pared con restitución costal con placas y clips de titanio (sistema STRATOS™), lo que creemos que es una restitución más fisiológica de la pared. No encontramos informe anterior de una reconstrucción con este sistema en caso similar.
ConclusiónLa alta mortalidad del empiema en los pacientes con hepatopatías requiere la implementación y la búsqueda de nuevas terapias adyuvantes, tales como la utilización de VAC™-IT y la posible reconstrucción con barras de titanio. Se requieren estudios controlados con una serie de casos amplia para una adecuada evaluación.
Conflicto de interesesLos autores declaramos no tener conflictos de intereses respecto al presente artículo.