La clasificación que hace la Organización Mundial de la Salud sobre las neoplasias pulmonares posiciona la hiperplasia idiopática difusa de células neuroendocrinas como lesión premaligna. Por las formas clínicas de presentación, tan inespecíficas como la tos, y radiológicas, como son los nódulos pulmonares, supone un reto diagnóstico para los clínicos. Describimos nuestra experiencia diagnóstica en esta enfermedad con los 2 casos que exponemos a continuación.
Caso 1. Mujer de 66 años con carcinoma intraductal de mama, con receptores hormonales positivos, tratada mediante tumorectomía, radioterapia y hormonoterapia adyuvantes. Padeció derrame pericárdico crónico asociado a la radioterapia que precisó evacuación. En TAC de control se observaron nódulos pulmonares que requirieron valoración.
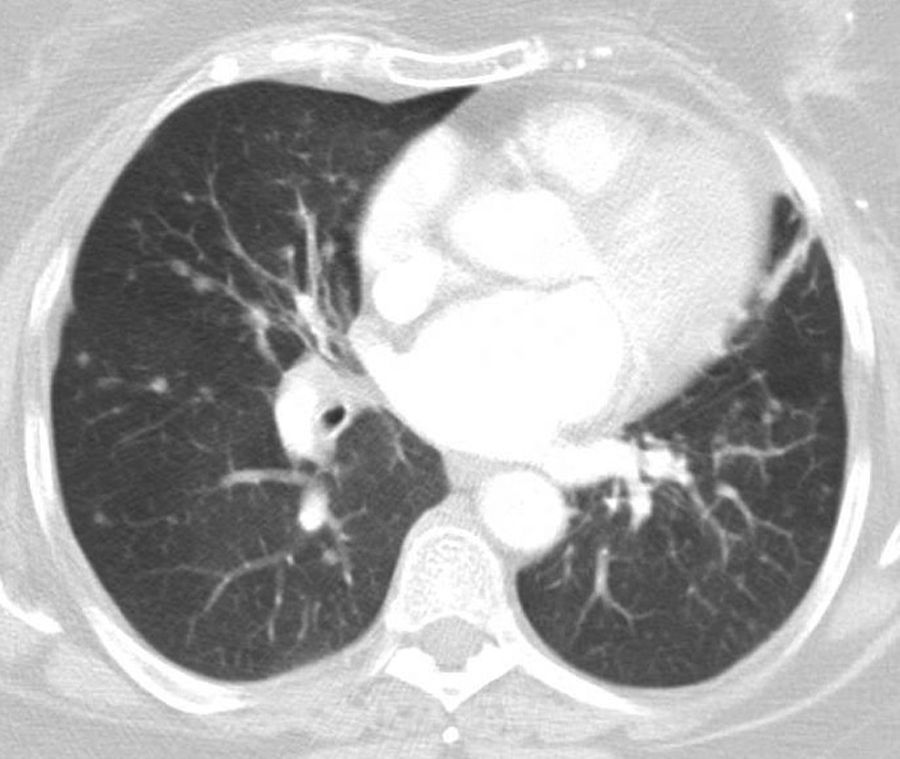
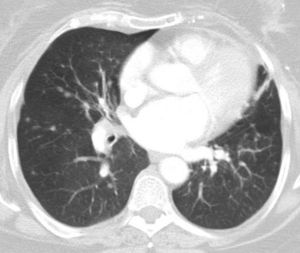
Contaba tos crónica desde hacía años. La exploración funcional mostraba una capacidad vital forzada de 1.820cm3 (80,5%) y un volumen espiratorio forzado en el primer segundo de 1.120cm3 (59,6%), cociente del 61,33%. En la TAC se observaron múltiples imágenes nodulares de diferentes tamaños distribuidas por ambos campos pulmonares. Seis meses después apreciamos un crecimiento del número y tamaño de los nódulos (fig. 1).
La tomografía con emisión de positrones (PET)-TAC detectó nódulos sólidos de entre 8 y 14mm, con SUV máximo de 3,88. Otros no presentaron captación. Además se detectaron 3 adenopatías con un SUV máximo de 6,8 hasta 8mm a nivel cervical derecho y retromandibular. La broncoscopia no aportó información relevante, salvo crecimiento de Aspergillus fumigatus en el aspirado bronquial que posteriormente se negativizó. Dos meses más tarde, una videotoracoscopia con resecciones en cuña del lóbulo medio e inferior derecho mostró una hiperplasia difusa idiopática de células neuroendocrinas asociada a tumorlets y tumores carcinoides típicos periféricos (fig. 2).
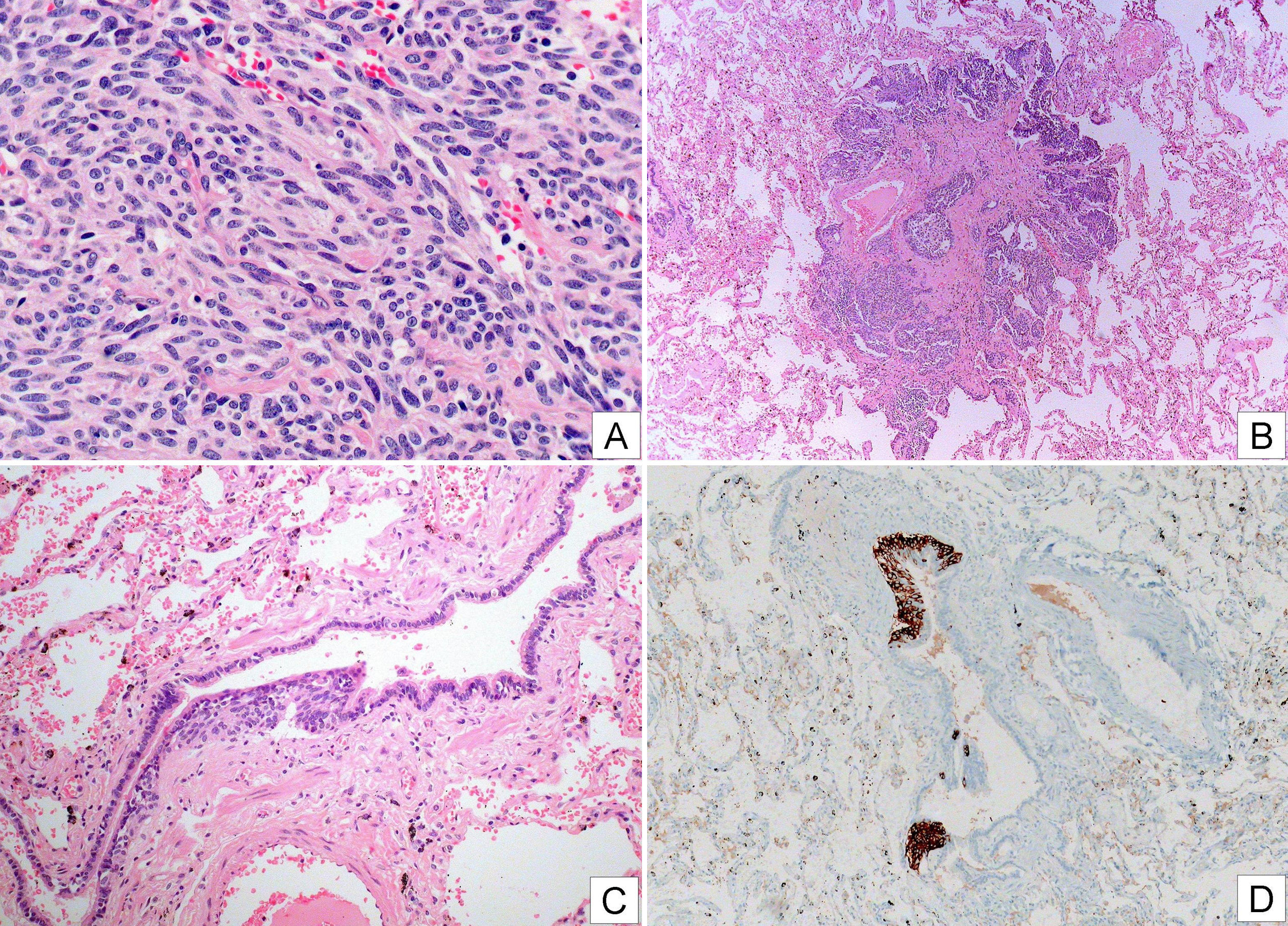
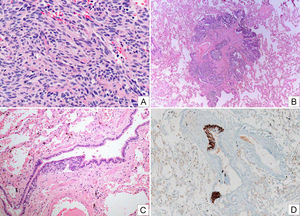
Composición fotográfica donde se muestran imágenes representativas de un tumor carcinoide (A, HE) con cierta morfología fusocelular donde no se advierte atipia, necrosis ni actividad mitótica significativa, de un tumorlet (B, HE) y de una hiperplasia intraepitelial de células neuroendocrinas (C, HE y D, inmunotinción con cromogranina).
Caso 2. Mujer de 29 años, con prótesis mamarias bilaterales, diagnosticada de asma bronquial extrínseco, con clínica de tos crónica. La espirometría, radiografía de tórax y senos paranasales fueron normales. En la TAC de tórax aparecían micronódulos pulmonares bilaterales de aspecto residual. Nueve meses más tarde, a la madre de la paciente le detectaron múltiples nódulos pulmonares que fueron extirpados mediante resección en cuña del lóbulo medio y lóbulo inferior derecho. El anatomopatólogo describía tumor carcinoide típico periférico asociado a tumorlets y a hiperplasia difusa idiopática de células neuroendocrinas. Los ganglios mediastínicos extirpados no mostraron alteraciones. Con más detalle, informaba sobre una proliferación multifocal de células neuroendocrinas que se distribuían en lesiones tumorales de más de 5mm en al menos 2 de ellas, en otras de menos de 5mm en más de 7, así como en forma de hiperplasia intraepitelial de células neuroendocrinas. Se observaron menos de 2 mitosis por 10 CGA. Cromogranina, sinaptofisina y CD 56 resultaron positivos, y el estudio con calcitonina resultó negativo. Con estos datos de este familiar de primer grado solicitamos TAC de control a nuestra paciente, a la que se informó más detalladamente de la existencia de múltiples nódulos pulmonares de menos de 1cm de diámetro, con un diámetro medio de unos 3mm, bilaterales, redondeados difusos, sin calcificaciones en su interior, en número de unos 25 en pulmón derecho y 15 en el pulmón izquierdo. La broncoscopia detectó signos directos de neoplasia en bronquio de la língula. La biopsia de la lesión resultó un carcinoide típico con buena diferenciación. La gammagrafía con fluoro 18-L dihidroxifenilalanina (F18.Flúor-DOPA) mostró 3 nódulos en el lóbulo inferior derecho, el mayor de ellos de 9mm, con un SUV máximo de 1,09 (SUV del parénquima 0,49), y 4 nódulos en el pulmón izquierdo, 2 de estos en la língula, el mayor de 13mm con SUV máximo de 0,78 (SUV del parénquima de 0,37) y otro de 9mm con SUV máximo de 0,79.
La hiperplasia idiopática difusa de células neuroendocrinas (DIPNECH, siglas en inglés) es una entidad que cada año la encontramos con más facilidad en la literatura1. Es un sobrecrecimiento generalizado y extenso de células neuroendocrinas en la vía aérea periférica y es considerada lesión premaligna. Las formas clínicas de presentación asintomática, como es el caso de la madre de nuestra segunda paciente, tos, disnea, sibilantes, propios de enfermedades tan prevalentes como el asma o la bronquiolítis contribuyen a no sospecharla, no investigarla y no conocer su prevalencia real. La exploración funcional respiratoria puede ir desde normal hasta patrón obstructivo o mixto. En las pruebas de imagen, el patrón micronodular bilateral es su forma de presentación más frecuente2. En nuestro caso 2, no tenemos muestra más amplia, como se recomienda para el diagnóstico de esta enfermedad3, pero el antecedente familiar de hiperplasia idiopática difusa de células neuroendocrinas, la historia clínica, las alteraciones radiográficas, junto con los resultados de la biopsia conllevaron una reinterpretación de lesiones que inicialmente se entendieron como residuales. No conocemos datos sobre acúmulo familiar de esta enfermedad. En el estudio de Gorshtein et al.4, no encuentran esta relación en ninguno de los 11 casos recogidos. En otras ocasiones, la radiología demuestra atrapamiento aéreo, patrón en mosaico, los cuales podrían pasar desapercibidos si no realizamos TAC en espiración5. La PET-TAC convencional con glucosa no es sensible para los tumores carcinoides, por su tamaño y por su escasa actividad mitótica. Se emplean marcadores como el octeótrido o el análogo de un aminoácido F18.Flúor-DOPA. El pronóstico global es favorable, aunque casos puntuales pueden cursar con mala evolución por la aparición de metástasis a distancia.