Evaluar el efecto de la presión positiva continua en la vía aérea (CPAP) sobre las fosas nasales de pacientes con síndrome de apnea hipopnea del sueño y su impacto en la calidad de vida, e identificar factores predictivos de cumplimiento.
MétodosEstudio prospectivo longitudinal. Treinta y seis pacientes consecutivos evaluados antes y 2 meses tras CPAP usando las siguientes variables clínicas (síntomas otorrinolaringológicos, test de Epworth, escala de ansiedad/depresión, calidad de vida general y específica para rinoconjuntivitis); anatómicas (exploración otorrinolaringológica, tomografía computarizada); funcionales (función auditiva y tubárica, flujo nasal, transporte mucociliar); biológicas (citología nasal), y polisomnográficas. Se dividió la muestra entre cumplidores (≥4h/d) y no cumplidores (<4h/d).
ResultadosSe objetivó una mejoría significativa en la somnolencia diurna (p=0,000), la ansiedad (p=0,006) y la depresión (p=0,023). Se evidenció sequedad nasal (p=0,000), aumento de neutrófilos en la citología nasal (p=0,000) y deterioro de la función ciliar, especialmente en cumplidores. No se evidenciaron diferencias significativas en el resto de las variables. La somnolencia inicial fue el único factor pronóstico de cumplimiento.
ConclusionesEl tratamiento con CPAP en pacientes sin patología nasal previa mejora una serie de parámetros clínicos y provoca rinitis y sequedad en la vía aérea. Algunas de las variables otorrinolaringológicas empeoran en los cumplidores. La somnolencia fue el único factor pronóstico de mala tolerancia.
To evaluate the effect of continuous positive airway pressure (CPAP) on the nostrils of patients with sleep apnea-hypopnea syndrome and its impact on quality of life, and to identify predictive factors for compliance.
MethodsLongitudinal prospective study. Thirty-six consecutive patients evaluated before and 2 months after CPAP using the following variables: clinical (eye, nose and throat [ENT] symptoms, Epworth test, anxiety/depression scales, general and rhinoconjunctivitis-specific quality of life); anatomical (ENT examination, computed tomography); functional (auditive and Eustachian tube function, nasal flow, mucociliary transport); biological (nasal cytology); and polisomnographics. The sample was divided into compliers (≥4h/d) and non-compliers (<4h/d).
ResultsA significant improvement was observed in daytime sleepiness (p=0.000), anxiety (P=.006), and depression (P=.023). Nasal dryness (P=.000), increased neutrophils in nasal cytology (P=.000), and deteriorating ciliary function were evidenced, particularly in compliers. No significant differences were observed in the other variables. Baseline sleepiness was the only factor predictive of compliance.
ConclusionsCPAP in patients without previous nasal pathology leads to an improvement in a series of clinical parameters and causes rhinitis and airway dryness. Some ENT variables worsened in compliers. Sleepiness was the only prognostic factor for poor tolerance.
El síndrome de apnea hipopnea del sueño (SAHS) se caracteriza por la obstrucción completa o parcial de la vía aérea superior mientras el paciente duerme, acompañado de desaturación de la oxihemoglobina o de microdespertares. Se asocia a mayor riesgo cardiovascular, hipertensión arterial, alteraciones neurocognitivas y aumento de mortalidad1. El tratamiento con presión positiva continua en la vía aérea (CPAP) es de elección en la mayoría de los pacientes con SAHS moderado-severo, controlando la enfermedad, mejorando la calidad de vida y disminuyendo la morbimortalidad2.
Para un adecuado tratamiento, su aplicación debe ser continuada, pero debido a sus posibles reacciones adversas, su cumplimiento a medio plazo solo se produce en un 60% de los pacientes3. El análisis de la tolerancia y el cumplimiento de la CPAP muestra resultados variables en la literatura4. El incumplimiento se ha asociado a incomodidad de la mascarilla, sensación claustrofóbica, molestias por ruido, inflamación nasal, sequedad faríngea, clínica ocular, molestias óticas inespecíficas, somnolencia o fatiga excesiva5,6. También hemos de tener en cuenta el perfil psicológico del paciente, siendo muy importante el soporte educacional y conductual para aumentar la tolerancia y el cumplimiento7,8.
La rinitis asociada a la CPAP es un problema trascendente, aunque no siempre se correlaciona con menor cumplimiento9. Nuestra hipótesis es que un adecuado estudio de los cambios producidos en el área otorrinolaringológica tras tratamiento con CPAP puede permitir detectar y tratar precozmente a los pacientes no cumplidores, realizando una medicina personalizada optimizando su manejo.
Nuestro objetivo ha sido analizar los cambios producidos en las fosas nasales de pacientes con SAHS sin patología nasal previa tras la instauración de CPAP y su repercusión en el cumplimiento del tratamiento.
Material y métodosDiseñoEstudio longitudinal prospectivo. Cuarenta y un pacientes consecutivos diagnosticados de SAHS por polisomnografía (índice de apnea-hipopnea [IAH] > 10) y tributarios de tratamiento con CPAP fueron evaluados antes y a los 2 meses de tratamiento con CPAP mediante variables clínicas, anatómicas, funcionales, biológicas y polisomnográficas. Tanto las evaluaciones clínicas otorrinolaringológicas como las pruebas complementarias fueron realizadas por el mismo explorador, diferente según la variable a analizar, antes y después del tratamiento con CPAP, el cual en todos los casos fue ciego para el resto de las variables.
Criterios de inclusión y exclusiónSe incluyó únicamente a pacientes mayores de 18 años. Se excluyó a aquellos que tomaban corticoides, antihistamínicos (nasales o sistémicos) o fármacos inductores de rinitis (tabla 1); a aquellos tratados anteriormente con CPAP, BIPAP u oxígeno, y a pacientes con apneas centrales o patología nasal previa. Todos los pacientes firmaron un consentimiento informado previo al inicio del estudio.
Fármacos inductores de rinitis
| Antihipertensivos (reserpina, guanetidina, fentolamina, inhibidores del enzima de conversión de la angiotensina, metildopa, bloqueantes α-adrenérgicos [teratozina], β-bloqueantes, teratozina, hidralazina, doxasozina, clonidina, prasozina) |
| Ácido acetilsalicílico y otros antiinflamatorios no esteroideos derivados del mismo |
| Antihistamínicos |
| Antidepresivos tricíclicos |
| Ketotifeno y astemizol |
| Corticoides orales o tópicos |
| Anticonceptivos orales y preparados con estrógenos y/o progestágenos |
| Clorpromacina |
| Neurolépticos |
| Agentes tópicos oculares (betabloqueantes, pilocarpina, etc.) |
| Cloruro de benzalconio (en algunos vasoconstrictores tópicos) |
| Antibióticos (espiramicina, penicilina, etc.) |
| Descongestionantes nasales |
| Cocaína |
Se cuantificó la somnolencia diurna mediante la escala de Epworth10, considerando excesivo un resultado superior a 1111. El estado anímico se analizó mediante la escala de ansiedad-depresión12 (HAD) y la calidad de vida general utilizando el cuestionario SF-1213.
Los síntomas clínicos otorrinolaringológicos se estudiaron del modo siguiente: la obstrucción nasal fue valorada según la escala de evaluación de la obstrucción nasal (NOSE14; 0 = no obstrucción, 1 = obstrucción leve, 2 = obstrucción moderada; 3 = obstrucción severa). La clínica de rinitis (secreción nasal, prurito nasal y estornudos) se clasificó según sistema de estadificación de Rasp15 (0 = asintomático, 1 = sintomatología leve, 2 = sintomatología moderada, 3 = sintomatología severa). La sequedad nasofaríngea, la clínica ótica(hipoacusia y acúfenos) y la clínica cutáneo-ocular (molestias cutáneas en zona de contacto con la mascarilla e irritación ocular por fuga de aire de la mascarilla) fueron valoradas individualmente, a similitud con la escala de Rasp, de 0 a 3. La calidad de vida específica relacionada con la sintomatología otorrinolaringológica se estudió mediante el Rhinoconjunctivitis Quality of Life Questionnaire16.
Variables anatómicasLa otoscopia y la rinoscopia se evaluaron como normales o alteradas.
Se evaluó la presencia de sobrepeso u obesidad mediante el índice de masa corporal y el perímetro cervical.
Los volúmenes nasosinusales se calcularon en cm3 partir de imágenes adquiridas mediante tomografía computarizada (TC) Siemens con sistema de multidetector Sensation 64 con cortes de 3mm.
Variables funcionalesSe evaluó el flujo respiratorio nasal (cm3/s) mediante rinomanometría anterior activa (rinomanómetro Rinospir Pro, SIBEL S.A. España), en cada fosa nasal, con el paciente sentado a una presión de 150Pa. Se consideró normal un flujo total (derecho+izquierdo) a partir de 630 cm3/s en mujeres y de 700 cm3/s en hombres17.
El transporte mucociliar fue medido mediante el test de la sacarina18, considerándose anormal cuando este era superior a 60 min.
La función tubárica19 fue evaluada mediante timpanometría (impedanciómetro GSI TympStar, Grason-Stadler, Eden Prairie, MN, EE. UU.), considerándose normal un máximo de distensibilidad entre +50 y –100mm de agua. La función auditiva19 fue estudiada por audiometría tonal liminar (audiómetro GSI TympStar, Grason-Stadler, Eden Prairie, MN, EE. UU.) a frecuencias de 250 a 8.000Hz. Se valoraba normal la audición del estímulo por debajo de los 25 decibelios en frecuencias conversacionales.
Variables biológicasSe cuantificaron, la inmunoglobulina E total en sangre (normal ≤ 100 U/ml (240 mg/l) y los eosinófilos en sangre (normal<5%). La presencia de inflamación nasal fue evaluada por citología obtenida a partir de raspado en mucosa de la cabeza del cornete inferior (Rhinoprobe®). Se calculó el número de eosinófilos y neutrófilos sobre la base de 500 células epiteliales (en individuos sanos y sin patología no se observan eosinófilos ni neutrófilos).
Variables polisomnográficasEvaluadas según las normativas de la Sociedad Española de Neumología y Cirugía Torácica (SEPAR)20,21, las respiratorias siguiendo las normativas de la SEPAR20,21 y las neurológicas de acuerdo con los criterios de Rechtschaffen y Kales22. Se cuantificaron el IAH; el porcentaje del tiempo con saturación de oxígeno menor al 90% (CT 90), la desaturación máxima de oxígeno durante la noche (nadir) y la presión de CPAP.
SeguimientoTodos los pacientes fueron controlados en la Unidad de Sueño del hospital siguiendo el protocolo asistencial habitual, que incluye una primera visita a las 2-4 semanas de la titulación de la CPAP; los pacientes sin dificultades específicas se controlan nuevamente en 2-3 meses y aquellos que precisan reajustes específicos se controlan en base a ellos hasta solventar el problema. Los pacientes con intolerancia e incumplimiento son estudiados a la presión recomendada mediante un equipo CPAP que permite durante varios días la detección de eventos residuales, la presión de CPAP, las fugas y el cumplimiento.
En nuestro trabajo reevaluamos, por protocolo, todas las variables a estudiar a los 2 meses de instaurarse la CPAP y ningún paciente fue sometido a ningún tratamiento que pudiera alterar los resultados.
El grado de cumplimiento se valoraba de forma subjetiva mediante cuestionario estandarizado y escala analógica visual 0 a 10 y de forma objetiva mediante sistema automático a través del registro en el contador del CPAP (tiempo en horas y en noches de uso de CPAP). Se consideró un cumplimiento adecuado un mínimo de 4h al día todos los días de la semana23; según esto, se establecieron 2 grupos, cumplidores (≥ 4h/d) y no cumplidores (< 4h/d).
Metodología estadísticaLas variables se recogieron en una base de datos y se analizaron mediante el programa estadístico SPSS 18. Las variables cuantitativas se expresan como media±desviación estándar o como porcentaje, según proceda. Se utilizó el test de Wilcoxon o la chi al cuadrado para analizar las variables antes y después de la CPAP. Para comparar las diferencias entre pacientes cumplidores y no cumplidores se utilizó la U de Mann-Whitney. Se realizó un análisis multivariado para evaluar factores predictivos de falta de cumplimiento de la CPAP. Se consideró estadísticamente significativa una p<0,05.
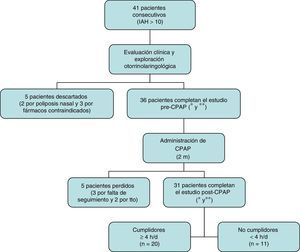
ResultadosSe incluyó a 41 pacientes consecutivos con SAHS tributarios de tratamiento con CPAP. Cinco fueron descartados tras la evaluación inicial por presentar criterios de exclusión; de los 36 restantes (31 hombres y 5 mujeres, con edad media 55,72±9,50 años) únicamente 31 completaron el estudio a los 2 meses (fig. 1). Veinte fueron cumplidores y 11 no cumplidores.
Diagrama de pacientes incluidos en el estudio.
* Incluye anamnesis completa, índice de masa corporal, perímetro cervical, exploración mediante otoscopia y nasofibroendoscopia flexible.
** Incluye cuestionarios estandarizados de síntomas y calidad de vida, audiometría, impedanciometría, rinomanometría, test de la sacarina, frotis nasal y tomografía computarizada nasosinusal.
Los resultados de las variables antes y después de la CPAP se describen en la tabla 2. Se objetivó una mejora significativa en la somnolencia diurna (p=0,000), la ansiedad (p=0,006) y la depresión (p=0,023). También se evidenció aparición de sequedad nasal (p=0,000) y aumento de neutrófilos en la citología nasal (p=0,000). No se evidenciaron diferencias significativas en el resto de las variables.
Variables clínicas, anatómicas, funcionales, biológicas y de calidad de vida antes y después de la CPAP en todos los pacientes del estudio
| Variables | Pre-CPAP | Post-CPAP | p |
|---|---|---|---|
| (n=31) | (n=31) | ||
| Media±desviación estándar | Media±desviación estándar | ||
| Epworth | 13,61±5,22 | 8,19±3,67 | 0,000 |
| Obstrucción nasal | 1,45±1,31 | 1,55±1,39 | 0,700 |
| Clínica de rinitis | 0,86±1,06 | 134±1,76 | 0,090 |
| Sequedad nasal | 0,00±0,00 | 1,52±1,29 | 0,000 |
| Clínica ótica | 0,43±0,62 | 0,33±0,67 | 0,180 |
| Clínica cutáneo-ocular | 0,68±1,19 | 0,71±1,16 | 0,705 |
| HAD | |||
| Ansiedad | 7,48±3,92 | 5,55±3,16 | 0,006 |
| Depresión | 5,16±3,90 | 3,68±3,43 | 0,023 |
| TC (cm3) | 80,46±53,80 | 79,78±55,83 | 0,395 |
| Otoscopia (normal/alterada) | 29/2 | 29/2 | 1 |
| Rinoscopia (normal/alterada) | 6/25 | 6/25 | 1 |
| Rinomanometría (cm3/s) | 833,07±286,72 | 834,53±259,73 | 0,665 |
| Test de la sacarina (min) | 31,06±23,13 | 36,97±2452 | 0,117 |
| Impedanciometría (normal/alterada) | 30/1 | 30/1 | 1 |
| Audiometría (normal/alterada) | 31/0 | 31/0 | 1 |
| IgE (U/ml) | 134,71±393,16 | 87,13±147,60 | 0,195 |
| Eosinofilia (%) | 2,45±1,38 | 2,87±1,87 | 0,090 |
| Citología (número de células inflamatorias/500 células epiteliales) | |||
| Eosinófilos | 0,03±0,11 | 0,09±0,27 | 0,234 |
| Neutrófilos | 0,69±1,71 | 5,66±9,39 | 0,000 |
| SF-12 | |||
| GH | 44,51±25,73 | 48,50±26,33 | 0,587 |
| PF | 74,19±24,56 | 72,50±28,87 | 0,642 |
| RP | 70,16±22,97 | 75,41±24,00 | 0,083 |
| RE | 73,61±22,11 | 75,81±21,89 | 0,277 |
| BP | 76,61±21,34 | 82,50±23,80 | 0,115 |
| MH | 63,70±22,90 | 68,33±21,20 | 0,233 |
| VT | 41,93±24,48 | 47,50±25,72 | 0,193 |
| SF | 76,61±28,08 | 82,50±25,55 | 0,148 |
| RQLQ | 1,48±1,10 | 1,26±1,13 | 0,493 |
BP: dolor corporal; HAD: escala de ansiedad-depresión; GH: salud general; IgE: inmunoglobulina E; MH: salud mental; PF: funcionamiento físico; RE: rol emocional; RP: rol físico; RQLQ: Rhinoconjunctivitis Quality of Life Questionnaire; SF: funcionamiento social; SF-12: versión reducida del cuestionario de calidad de vida SF-36; TC: tomografía computarizada; VT: vitalidad.
Los cumplidores (tabla 3) presentaron una mejoría en el test de Epworth más relevante que los no cumplidores (p=0,000), con clara tendencia a mejorar la ansiedad (p=0,052) y la depresión (p=0,054). Sorprendentemente, estos presentaron mayor sequedad nasal (p=0,001), mayor aumento de neutrófilos en la citología nasal (p=0,002), tendencia al empeoramiento del transporte mucociliar (p=050) y mayor eosinofilia sanguínea (p=0,058) pero dentro de los límites normales (< 5%).
Variables clínicas, anatómicas, funcionales, biológicas y de calidad de vida antes y después de la CPAP en pacientes cumplidores y no cumplidores
| Variables | Cumplidores (n = 20) | No cumplidores (n = 11) | ||||
|---|---|---|---|---|---|---|
| Pre-CPAP | Post-CPAP | p | Pre-CPAP | Post-CPAP | p | |
| Media±desviación estándar | Media±desviación estándar | Media±desviación estándar | Media±desviación estándar | |||
| Epworth | 11,90±4,70 | 7,55±2,66 | 0,000 | 16,73±4,83 | 9,36±4,94 | 0,005 |
| Obstrucción nasal | 1,65±1,39 | 1,50±1,40 | 0,582 | 1,09±1,13 | 1,64±1,43 | 0,221 |
| Clínica de rinitis | 1,06±1,11 | 1,50±1,76 | 0,305 | 0,55±0,93 | 1,09±1,81 | 0,131 |
| Sequedad nasal | 0,00±0,00 | 1,55±1,23 | 0,001 | 0,00±0,00 | 1,45±1,44 | 0,023 |
| Clínica ótica | 0,47±0,70 | 0,42±0,77 | 0,564 | 0,36±0,50 | 0,18±0,40 | 0,157 |
| Clínica cutáneo-ocular | 0,60±1,19 | 0,60±1,14 | 1,000 | 0,82±1,25 | 0,91±1,22 | 0,317 |
| HAD | ||||||
| Ansiedad | 7,20±4,14 | 5,45±3,02 | 0,052 | 8,00±3,63 | 5,73±3,55 | 0,040 |
| Depresión | 4,65±4,12 | 3,15±3,05 | 0,054 | 6,09±3,44 | 4,64±4,00 | 0,233 |
| TC (cm3) | 73,80±51,47 | 71,91 ±51,13 | 0,113 | 93,02±58,94 | 94,64±64,30 | 0,441 |
| Otoscopia (normal/alterada) | 19/1 | 19/1 | 1 | 10/1 | 10/1 | 1 |
| Rinoscopia (normal/alterada) | 4/16 | 4/16 | 1 | 2/9 | 2/9 | 1 |
| Rinomanometría (cm3/s) | 832,12±301,94 | 848,80 ±224,75 | 0,758 | 834,55±224,46 | 806,00±330,71 | 0,878 |
| Test de la sacarina (min) | 30,40 ±23,72 | 39,40 ±24,85 | 0,050 | 32,27±23,12 | 32,55±24,46 | 0,735 |
| Impedanciometría (normal/alterada) | 19/1 | 19/1 | 1 | 11/0 | 11/0 | 1 |
| Audiometría (normal/alterada) | 20/0 | 20/0 | 1 | 11/0 | 11/0 | 1 |
| IgE (U/ml) | 64,56±89,77 | 49,63±39,86 | 0,221 | 261,00±648,79 | 151,91±230,24 | 0,540 |
| Eosinofilia (%) | 2,70 ±1,53 | 3,35 ±2,13 | 0,058 | 2,00±1,00 | 2,00±0,77 | 1,000 |
| Citología (número de células inflamatorias por 500 células epiteliales) | ||||||
| Eosinófilos | 0,50 ±0,14 | 0,07 ±0,21 | 0,457 | 0,00±0,00 | 0,10±0,36 | 0,317 |
| Neutrófilos | 0,76 ±2,04 | 7,47 ±11,15 | 0,002 | 0,55±0,94 | 2,39±3,14 | 0,033 |
| Variables | Cumplidores (n = 20) | No cumplidores (n = 11) | ||||
|---|---|---|---|---|---|---|
| Pre-CPAP | Post-CPAP | p | Pre-RECPAP | Post-CPAP | p | |
| Media±desviación estándar | Media±desviación estándar | Media±desviación estándar | Media±desviación estándar | |||
| SF-12 | ||||||
| GH | 50,71 ± 23,47 | 48,50 ± 26,06 | 0,491 | 31,50±26,56 | 48,50±28,28 | 0,213 |
| PF | 73,81 ± 25,59 | 73,75 ± 26,25 | 0,917 | 75,00±23,57 | 70,00±34,96 | 0,414 |
| RP | 72,62 ± 22,57 | 80,00 ± 23,79 | 0,079 | 65,00±24,15 | 66,25±22,85 | 0,705 |
| RE | 73,21 ± 22,11 | 77,50 ± 20,92 | 0,415 | 67,50±24,43 | 71,25±24,33 | 0,524 |
| BP | 79,76 ± 20,34 | 83,75 ± 24,70 | 0,454 | 70,00±22,97 | 80,00±22,97 | 0,046 |
| MH | 66,67 ± 20,66 | 70,00 ± 20,03 | 0,483 | 57,50±27,13 | 65,00±24,15 | 0,304 |
| VT | 41,67 ± 24,15 | 48,75 ± 24,97 | 0,222 | 42,50±26,48 | 45,00±28,32 | 0,655 |
| SF | 80,95 ± 27,28 | 87,50 ± 22,21 | 0,222 | 67,50±28,98 | 72,50±29,93 | 0,458 |
| RQLQ | 1,42 ±1,13 | 1,03 ±0,91 | 0,209 | 1,60±1,10 | 1,72±1,43 | 0,575 |
BP: dolor corporal; HAD: escala de ansiedad-depresión; GH: salud general; IgE: inmunoglobulina E; MH: salud mental; PF: funcionamiento físico; RE: rol emocional; RP: rol físico; RQLQ: Rhinoconjunctivitis Quality of Life Questionnaire; SF: funcionamiento social; SF-12: versión reducida del cuestionario de calidad de vida; SF-36; TC: tomografía computarizada; VT: vitalidad.
En los no cumplidores solo se evidenció un empeoramiento del dolor corporal (p=0,046).
En el estudio univariante (tabla 4), la somnolencia diurna fue el único factor predictivo de no cumplimiento (p=0,014), observándose una tendencia también a menor cumplimiento en los pacientes con peor estado general de salud (p=0,059) y mejor CT 90 (p=0,064). En el análisis multivariante la mayor puntuación en el test de Epworth fue el único factor independiente de no cumplimiento (odds ratio: 1,243; intervalo de confianza: 1,000-1,545, p = 0,050).
Variables clínicas, anatómicas, funcionales, biológicas, polisomnográficas, terapéuticas y de calidad de vida pre-CPAP en pacientes cumplidores y no cumplidores
| Variables pre-CPAP | Cumplidores | No cumplidores | p |
|---|---|---|---|
| Media±desviación estándar (n=20) | Media±desviación estándar (n=11) | ||
| Edad (años) | 57,40±8,83 | 54,55±10,49 | 0,549 |
| IAH | 44,30±23,12 | 37,27±22,73 | 0,386 |
| CT 90 | 37,36±25,26 | 17,10±16,90 | 0,069 |
| Nadir | 67,70±15,94 | 73,29±8,51 | 0,526 |
| Índice de masa corporal | 29,17±3,72 | 29,83±3,02 | 0,726 |
| Perímetro cervical (cm) | 43,40±5,21 | 44,36±4,05 | 0,575 |
| Presión CPAP | 9,15±1,42 | 8,36±0,92 | 0,148 |
| Horas CPAP | 5,99±1,27 | 2,01±1,35 | 0,000 |
| Epworth | 11,90±4,70 | 16,73±4,83 | 0,014 |
| Obstrucción nasal | 1,65±1,39 | 1,09±1,13 | 0,242 |
| Clínica de rinitis | 1,06±1,11 | 0,55±0,93 | 0,213 |
| Sequedad nasal | 0,00±0,00 | 0,00±0,00 | 1,000 |
| Clínica ótica | 0,47+/-0,70 | 0,36±0,50 | 0,819 |
| Clínica cutáneo-ocular | 0,60±1,19 | 0,82±1,25 | 0,716 |
| HAD | |||
| Ansiedad | 7,20±4,14 | 8,00±3,63 | 0,574 |
| Depresión | 4,65±4,12 | 6,09±3,44 | 0,290 |
| TC (cm3) | 73,81±51,47 | 93,03±58,94 | 0,397 |
| Otoscopia (normal/alterada) | 19/1 | 10/1 | 1 |
| Rinoscopia(normal/alterada) | 4/16 | 2/9 | 1 |
| Rinomanometría (cm3/s) | 833,12+/-301,94 | 834,55±224,46 | 0,888 |
| Test de la sacarina (min) | 30,40+/-23,71 | 32,27±23,12 | 0,539 |
| Impedanciometría (normal/alterada) | 19/1 | 11/0 | 1 |
| Audiometría (normal/alterada) | 20/0 | 11/0 | 1 |
| IgE (U/ml) | 64,56±89,77 | 261,00±648,79 | 0,962 |
| Eosinofilia (%) | 2,70±1,53 | 2,00±1,00 | 0,458 |
| Citología nasal (número de células inflamatorias/500 células epiteliales) | |||
| Eosinófilos | 0,50±0,14 | 0,00±0,00 | 0,184 |
| Neutrófilos | 0,76±2,04 | 0,55±0,94 | 0,629 |
| SF-12 | |||
| GH | 50,71±23,47 | 31,50±26,56 | 0,059 |
| PF | 73,81±25,59 | 75,00±23,57 | 0,964 |
| RP | 72,62±22,57 | 65,00±24,15 | 0,343 |
| RE | 73,61±22,11 | 67,50±24,43 | 0,444 |
| BP | 79,76±20,34 | 70,00±22,97 | 0,272 |
| MH | 66,67±20,66 | 57,50±27,13 | 0,386 |
| VT | 41,67±24,15 | 42,50±26,48 | 0,947 |
| SF | 80,95±27,28 | 67,50±28,98 | 0,160 |
| RQLQ | 1,42±1,13 | 1,60±1,10 | 0,696 |
BP: dolor corporal; CT 90: porcentaje del tiempo de registro transcurrido con una saturación < 90%; HAD: escala de ansiedad-depresión; GH: salud general; IgE: inmunoglobulina E; MH: salud mental; PF: funcionamiento físico; RE: rol emocional; RP: rol físico; RQLQ: Rhinoconjunctivitis Quality of Life Questionnaire; SF: funcionamiento social; SF-12: versión reducida del cuestionario de calidad de vida SF-36; TC: tomografía computarizada; VT: vitalidad.
Los resultados de este estudio pueden ser sorprendentes y no se avienen a la hipótesis planteada pues muestran que aunque la CPAP mejora la somnolencia y la ansiedad-depresión, provoca, especialmente en cumplidores, rinitis, sequedad en la vía aérea y alargamiento del transporte mucociliar. Las otras variables estudiadas no cambian significativamente. Asimismo, el único factor pronóstico de intolerancia es la somnolencia inicial pero ninguna de las variables otorrinolaringológicas.
Algunos autores consideran que la principal causa de intolerancia a la CPAP es la rinitis secundaria al tratamiento, aunque los resultados publicados son dispares. Otros han evaluado si pacientes con rinitis asociada a la CPAP mejoran al tratarla, sin hallar resultados satisfactorios24. Nosotros no hemos encontrado ningún dato que indique que la CPAP administrada en pacientes sin patología previa produce una rinitis clínica relevante, ni que sea una causa de incumplimiento del tratamiento. Tampoco hemos objetivado mejoría de sintomatología nasal en los pacientes cumplidores.
Estudios previos han evaluado la aparición o aumento de neutrófilos y/u otras células inflamatorias en citología nasal de pacientes y modelos animales de CPAP, encontrando resultados dispares25,26. Otros han hallado mediadores específicos de inflamación nasal27. Se supone que el flujo de aire seco estimularía las terminaciones nerviosas que liberarían mediadores celulares inflamatorios28, que podrían estimular la secreción de neuropéptidos29 implicando a los neutrófilos (ello explicaría su aumento en la mucosa nasal de pacientes con CPAP).
En un estudio en modelo murino realizado en nuestro centro, pudimos demostrar la presencia de inflamación neutrofílica tras la aplicación aguda de CPAP30. Por el contrario, Lacedonia et al.26 no objetivaron aumento de neutrófilos en la mucosa nasal de pacientes tratados con CPAP, aunque casi todos ellos tenían antes de empezar la CPAP el nivel de neutrófilos elevado, indicando posibilidad de patología nasal previa. Es más, en un trabajo reciente publicado por Gelardi et al., los autores indican que el uso continuado de CPAP mejora la rinitis de pacientes con SAHS, disminuyendo el número de células inflamatorias en la citología nasal31.
En el presente estudio, hemos confirmado la presencia de inflamación nasal, mayor en los cumplidores. Aunque nuestros resultados apoyan la presencia de inflamación nasal celular, se trataría habitualmente de una inflamación subclínica si atendemos al resto de variables analizadas. Por ello, sería interesante evaluar si con el tiempo de uso se produce un fenómeno adaptativo con mejoría del infiltrado inflamatorio o, por el contrario, un empeoramiento del mismo que pueda exacerbar los síntomas.
Asumiendo que la CPAP produce inflamación nasal, esta podría reflejarse en una hipertrofia de la mucosa nasosinusal y en consecuencia disminuir el espacio aéreo de las cavidades nasosinusales. En nuestro estudio el análisis del volumen aéreo nasosinusal medido mediante TC no ha mostrado diferencias significativas tras la CPAP. Esta situación, descrita previamente por de Weerdt et al.32, apoya que la inflamación sea leve-moderada. Tampoco la permeabilidad nasal, medida clínicamente y por rinomanometría, se ha visto alterada significativamente en nuestro estudio, coincidiendo con Skoczinski et al.33, que describen que la CPAP no provoca obstrucción nasal ni la obstrucción nasal predispone al incumplimiento del tratamiento.
En referencia a la sequedad nasal, algunas series han descrito que afecta a más del 60% de los pacientes con CPAP. Nosotros también hemos encontrado esta relación, aunque no ha interferido con el cumplimiento del tratamiento. Para tratar esta sequedad se utilizan habitualmente humidificadores, que si bien mejoran la clínica de los pacientes, no siempre mejoran la tolerancia o el cumplimiento34,35.
En nuestra serie, hemos evidenciado una tendencia al empeoramiento del transporte mucociliar únicamente en los cumplidores. Ello sugeriría que el fenómeno capaz de alterar el transporte mucociliar es dependiente del tiempo. Trabajos similares en la literatura muestran resultados contradictorios36,37, aunque en ellos no se valoraba ni el grado de cumplimiento ni la presión media de la CPAP.
Es evidente que la CPAP produce una situación inusual de presión positiva en la rinofaringe y orofaringe38. Esta situación podría aumentar la presión en el oído medio, produciendo síntomas óticos de diversa índole; incluso existen trabajos que plantean la CPAP como posible tratamiento de oídos con presiones medias negativas39,40. Sin embargo, nuestros resultados coinciden con los de Aksoy et al.41, que no hallan diferencias significativas en la presión del oído medio. En cuanto a la valoración auditiva, y coincidiendo también con trabajos anteriores42, no hemos podido demostrar cambios auditivos relevantes tras el tratamiento.
Factores predictivos de intolerancia a la presión positiva continua en la vía aéreaEl hecho más relevante de nuestro estudio es la ausencia de las diversas variables otorrinolaringológicas como factores predictivos de cumplimiento. Solo hemos hallado una mayor probabilidad de intolerancia al tratamiento en los pacientes con peor estado general y mayor somnolencia diurna. Así, el test de Epworth se ha mostrado como el único factor predictivo de mal cumplimiento a la CPAP. Este hecho llama mucho la atención ya que se ha postulado que los pacientes con mayor somnolencia son los que cumplen mejor. Debe considerarse, sin embargo, que los nuestros pacientes no tenían patología nasosinusal previa y por lo tanto estos resultados pueden no ser extrapolables a poblaciones no seleccionadas. Además, aunque la somnolencia diurna fue un factor independiente de mal cumplimiento, la significación estadística no fue muy alta por lo que nuestros resultados deberían considerarse con cautela. Deben existir otros factores, quizás de índole psicológica, previos o secundarios al propio SAHS, que puedan explicar la peor tolerancia en nuestro grupo.
En la literatura los factores predictivos de tolerancia a la CPAP son variables43, no habiendo forma precisa de establecer a priori el grado de cumplimiento del tratamiento. Los resultados son contradictorios respecto al IAH y al nivel de presión de CPAP. Se ha indicado que altas presiones de CPAP podrían ser un factor relevante, por ello, Sanders y Kem44 y Gulati et al.45 indican que los sistemas bipresión son de utilidad. En nuestro estudio, no hemos hallado relación entre la presión y el cumplimiento, aunque debemos considerar que la presión media de nuestra serie no ha sido muy elevada (7-12cm de H2O en pacientes cumplidores y 7-10cm H2O en los no cumplidores).
En referencia a la existencia de clínica de rinitis previa a la CPAP, Farhad et al.46 relacionan la existencia de marcadores inflamatorios o neutrófilos en mucosa nasal antes del tratamiento con el cumplimiento de la CPAP, encontrando que los pacientes con más inflamación o clínica de rinitis tienden a cumplir menos. En nuestro trabajo, los pacientes no presentaban ni aumento de neutrófilos en la mucosa nasal ni clínica de rinitis relevante de inicio. De hecho, los pacientes con patología nasal previa fueron excluidos, de forma que solo podemos valorar si los pacientes que presentaron un aumento de neutrófilos de la mucosa nasal tras la CPAP, pese a no presentar clínica, cumplían peor, cosa que no sucedió. Tampoco hallamos relación entre el cumplimiento y la sequedad nasal, como Kreivi et al.47.
Deben de existir una serie de fenómenos asociados de buena o mala adaptación o de percepción de la misma, que justificarían los hallazgos obtenidos, así como otros fenómenos que van desde aspectos psicológicos y sociales hasta de creencias y expectativas personales que dificultan la tolerancia a la CPAP48-50.
Como limitaciones de este trabajo debemos mencionar, en primer lugar, que nuestra población de estudio es pequeña. A pesar de ello, hemos podido valorar, con una amplia metodología, distintas variables para diferentes propósitos y estudiarlas a diferentes niveles (clínico, anatómico, funcional, biológico y polisomnográfico), coincidiendo globalmente en los resultados obtenidos. Otra limitación del estudio es el momento en que hemos hecho la valoración postratamiento, a los 2 meses. Desde este punto de vista, variables como la clínica de rinitis quizás aparecerían más o menos marcadas con el tiempo, reflejando el aumento de neutrófilos hallado en la mucosa nasal o bien al contrario, debido a posteriores fenómenos de adaptación. Lo mismo sucede con la somnolencia diurna como factor pronóstico de mal cumplimiento del tratamiento con CPAP; se precisarían estudios con mayor número de pacientes o un mayor tiempo de uso de la CPAP para afianzar estos resultados.
ConclusionesComo conclusión, puede decirse que globalmente el tratamiento con CPAP mejora una serie de parámetros clínicos pero provoca rinitis y sequedad nasal. Las diferentes variables otorrinolaringológicas analizadas no difieren mayormente entre los cumplidores y no cumplidores, y ninguna predice el grado de cumplimiento. La somnolencia inicial es el único factor predictivo de mal cumplimiento.
La importancia de este estudio es que por primera vez cuestiona la impresión generalizada de que fenómenos otorrinolaringológicos adversos secundarios a la CPAP son importantes en su cumplimiento. Son precisos estudios más amplios, aleatorizados y traslacionales, y que incluyan también a pacientes con patología nasal previa, para comprender mejor la relación entre la CPAP y la patología nasal en pacientes con SAHS en tratamiento con CPAP.
FinanciaciónBeca FISS PI07/0318.
AutoríaFrancina Aguilar y Ariel Cisternass: diseño del estudio. Visitas, exploraciones otorrinolaringológicas y realización de citología nasal y test sacarina. Coordinación de pruebas complementarias en todos los pacientes, pre y post-CPAP. Recogida de datos y realización de base de datos. Análisis estadístico y redacción del manuscrito.
Antonio Manuel Ávila y Juan Berenguer: estudio y cálculo de los volúmenes nasosinusales pre y post-CPAP en todos los pacientes y lectura crítica del manuscrito.
Isabel Vilaseca: diseño del estudio. Seguimiento clínico, análisis estadístico y redacción del manuscrito.
Alejandro Iranzo: diagnóstico y seguimiento de los pacientes y lectura crítica del manuscrito.
Josep Maria Montserrat: diagnóstico y seguimiento de los pacientes y lectura crítica del manuscrito.
Marta Torres-López: estudio citológico y lectura crítica del manuscrito.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Los autores declaran su agradecimiento a Maite Carrión, Ainhoa Asensio y Carmen León, por su ayuda en la realización de este proyecto.