El objetivo del estudio ha sido comparar la atenuación pulmonar inspiratoria y espiratoria en varones con enfermedad pulmonar obstructiva crónica (EPOC), según la gravedad, así como valorar la relación entre la atenuación del parénquima y la función pulmonar.
Pacientes y métodosSe seleccionó a 55 varones con EPOC moderada-muy grave y clínicamente estables. Se les realizaron gasometría arterial, espirometría, pletismografía, difusión de monóxido de carbono y prueba de la marcha. La gravedad de la EPOC se clasificó en función de la escala GOLD y del índice BODE. Se realizó una tomografía computarizada de tórax de alta resolución en inspiración y espiración, utilizando un programa informático específico para medir la atenuación de las diferentes áreas pulmonares.
ResultadosLa atenuación de los lóbulos inferiores fue menor en pacientes con EPOC grave y muy grave que en casos con enfermedad moderada, tanto en inspiración como en espiración. En los varones con EPOC moderada y grave se detectaron diferencias en la atenuación media de los lóbulos superiores. No se hallaron diferencias en función de los cuartiles del índice BODE. Los parámetros de obstrucción de la vía aérea se relacionaron principalmente con la atenuación de los lóbulos inferiores en espiración, mientras que los parámetros de hiperinsuflación se correlacionaron con la atenuación en inspiración. Por último, la capacidad de difusión se relacionó de forma independiente con el valor de atenuación espiratoria/inspiratoria de los lóbulos inferiores y la atenuación de los lóbulos inferiores en inspiración.
ConclusionesSe observan diferencias en la atenuación pulmonar entre los diferentes grados de gravedad de la EPOC establecidos según la clasificación GOLD.
We compare the inspiratory and expiratory regional lung densities between different levels of COPD severity (as assessed by the GOLD scale and by the BODE index), and to assess the relationship between regional lung densities and functional lung parameters.
Patients and methodsFifty-five stable moderate-severe COPD men were selected. Functional evaluation included dyspnoea scale, blood gases, spirometry, plethysmography, diffusing capacity and six-minute walk test. Severity was classified according the GOLD scale and the BODE index. High resolution computed tomography (HRCT) scans of the entire lung at full inspiration and two sections at full expiration were obtained. Densitometry software was used to calculate the densities of the lung areas.
ResultsInspiratory and expiratory mean lung densities (MLD) of the lower lobes were significantly lower in very severe and severe COPD patients than in moderate patients. In contrast, we only found differences between the upper lobe MLD values of moderate and severe COPD patients. Inspiratory and expiratory HRCT densities were similar among all BODE quartiles, for both the upper and lower lobes. In a multiple regression analysis, airway obstruction parameters were mainly related to the expiratory MLD of the lower lobes, whereas lung hyperinflation parameters were predicted by the inspiratory MLD of the lower lobes. Lastly, diffusion capacity was independently related to the expiratory/inspiratory MLD of the lower lobes and to the inspiratory MLD of the upper lobes.
ConclusionsThere are differences in lung attenuation measurements by HRCT between the varying levels of COPD severity as assessed by the GOLD scale.
La enfermedad pulmonar obstructiva crónica (EPOC) se caracteriza por un déficit en la función pulmonar con obstrucción de las vías respiratorias1–4, aunque su cuadro clínico muestra una heterogeneidad fenotípica importante5,6. Además de la evaluación convencional de la gravedad7, recientemente se ha propuesto utilizar el índice BODE (basado en el grado de limitación del flujo aéreo, la disnea, la tolerancia al ejercicio y el índice de masa corporal) para predecir la mortalidad8.
La tomografía computarizada de alta resolución (TACAR) es una herramienta no invasiva y muy útil para evaluar los enfisemas. Se ha demostrado que el análisis de la densidad del parénquima pulmonar en la TACAR está correlacionado con las alteraciones patológicas observadas en muestras tisulares9,10 y con el déficit de la función pulmonar (obstrucción del flujo aéreo y capacidad de difusión)11,12. Además, si bien las mediciones por TACAR en inspiración reflejan el grado de destrucción enfisematosa, el análisis densitométrico en espiración y el cociente de atenuación pulmonar espiratoria/inspiratoria parecen reflejar la obstrucción de las vías respiratorias periféricas y el atrapamiento aéreo11–13.
A pesar de que hay indicadores objetivos de la atenuación pulmonar en la TACAR, pocos estudios han evaluado su relación con la gravedad de la enfermedad. En los pacientes asmáticos, la atenuación pulmonar en la TACAR se relaciona con la gravedad de la enfermedad y disminuye durante las exacerbaciones14,15. Un estudio anterior no logró encontrar diferencias en la atenuación pulmonar en inspiración o espiración en 10 pacientes con EPOC leve y un grupo heterogéneo de 17 pacientes con EPOC moderada o grave–estadios II-IV de la Global Initiative for Chronic Obstrutive Lung Disease (GOLD)16–Es más, no se han investigado las diferencias de atenuación pulmonar en varones con EPOC moderada y grave. El objetivo de este estudio ha sido comparar la atenuación pulmonar entre distintos grados de EPOC, evaluados mediante la obstrucción del flujo aéreo o mediante un sistema de clasificación multidimensional (índice BODE). También hemos evaluado la relación de la atenuación pulmonar con los parámetros de función pulmonar en la EPOC moderada-muy grave.
Pacientes y métodosPacientesEstudiamos clínicamente de forma consecutiva a 55 varones con EPOC moderada-muy grave–volumen espiratorio forzado en el primer segundo (FEV1) tras broncodilatador<80% del valor predicho y FEV1/capacidad vital forzada (FVC)<70%–en situación estable7. Los criterios de exclusión eran: antecedentes de asma, otra enfermedad pulmonar activa, discapacidad mental o física, u otras enfermedades importantes que pudieran contribuir a la disnea o a la limitación del ejercicio, tales como la insuficiencia cardíaca congestiva, cardiopatía isquémica o valvular o enfermedad neuromuscular. Ninguno de los pacientes había experimentado una exacerbación de la EPOC ni infección de las vías respiratorias durante las 4 semanas anteriores, y ninguno había mostrado reversibilidad significativa tras la administraciónn de broncodilatador (> 12% del FEV1 basal o > 200ml). Tampoco habían recibido tratamiento con corticoides orales durante los últimos 3 meses como mínimo. Todos ellos dieron su consentimiento informado por escrito y el comité de ética local aprobó el estudio.
ProcedimientosTodos los pacientes se abstuvieron de utilizar broncodilatadores de acción corta o prolongada durante 6 y 12h, respectivamente, e interrumpieron el tiotropio 24h antes. Ninguno consumió cafeína ni cigarrillos durante las 2h previas a las pruebas de función pulmonar. Se les pesó descalzos y en ropa interior, y se calculó el índice de masa corporal.
La disnea funcional se evaluó mediante la escala de disnea modificada del Medical Research Council (MRC)17, la cual contempla 5 grados de actividad física que provocan disnea.
Todas las mediciones de la función pulmonar se realizaron como se describe en una publicación anterior18, con los pacientes en sedestación, y siempre en el mismo orden, permitiendo suficiente descanso entre una maniobra y otra. Todos los procedimientos los efectuó un mismo técnico, que desconocía los resultados. Se realizaron gasometría arterial y medición del pH en reposo, mientras el paciente respiraba aire ambiental, con un analizador de gases sanguíneos (ABL330, Radiometer, Copenhague, Dinamarca). Las espirometrías lentas y forzadas se efectuaron por medio de un neumotacógrafo, y los volúmenes pulmonares estáticos se midieron con un pletismógrafo de cuerpo entero con volumen constante (MasterLab Body, Jaeger, Würzburg, Alemania), según las directrices de la European Respiratory Society19. La capacidad inspiratoria (CI) se midió según el protocolo descrito por O’Donnell y Web20, y el cociente CI/capacidad pulmonar total (TLC) se utilizó como medida de la hiperinsuflación en reposo. Se determinó la capacidad de difusión del monóxido de carbono (DLCO) mediante el método de una respiración única (MasterLab)21 y se corrigió para los valores de hemoglobina (DLCOc)22. Los valores predictivos para los parámetros de función pulmonar se derivaron a partir de los publicados por la Comunidad Europea del Carbón y el Acero19,23.
La prueba de la marcha de 6min se llevó a cabo en un pasillo de 50m, según las normas de la American Thoracic Society24. Se tomó el mejor resultado de 2 pruebas, separadas por un intervalo de 30min como mínimo.
Se clasificó a los pacientes en 3 grupos en función de la gravedad de la EPOC, según las directrices GOLD7: EPOC en estadio II con limitación moderada del flujo aéreo (FEV1 50–80% del valor predicho), estadio III (FEV1 30–50% del valor predicho) y estadio IV (FEV1 <30% del valor predicho). Además, el porcentaje predicho de FEV1 (FEV1%), el índice de masa corporal, la prueba de la marcha de 6min y el resultado de la escala MRC se incorporaron en el índice BODE, y se calcularon los cuartiles de éste8.
La tomografía computarizada (TAC) se realizó en decúbito supino mediante un escáner helicoidal de corte único (Somaton Plus 4A, Siemens, Erlangen, Alemania), con un tiempo de barrido de 0,75s. Primero se obtuvo un TACAR de todo el pulmón durante una inspiración completa, con cortes de 1mm y desplazamiento de la mesa de 10mm. Después se estudiaron 2 secciones del pulmón durante la espiración completa: a la altura del arco aórtico, e inferior, a la altura de la confluencia de las venas pulmonares inferiores.
El voltaje y la corriente eléctrica se ajustaron al peso de cada paciente, con unas variaciones de 120–140kW y 200–300mA. Todas las imágenes se obtuvieron con una ventana apropiada de la ventana para visualizar el mediastino y el parénquima pulmonar (el último con un ancho de ventana de 1.500 y un centro de ventana de 500HU). El campo de visualización se ajustó a la corteza externa de las costillas para optimizar la matriz. Con estos límites (−800/−1.024HU) se utilizó el programa informático de densitometría pulmonar Somaton Plus 4 de Siemens para calcular las densidades, después de validar los valores densitométricos con fantomas. Establecimos el área dibujando a mano alzada la región de interés, luego se establecieron los límites (en HU) y el programa informático calculó la atenuación (MLD, del inglés mean lung density) de los lóbulos inferior y superior. El lóbulo medio y la língula no se incluyeron porque las TAC se tomaron en posición supina y, por lo tanto, se hubiese producido más atrapamiento aéreo en estas zonas. El tiempo transcurrido entre las pruebas de función pulmonar y la TAC nunca fue superior a los 3 días.
Análisis estadísticoLos valores se expresan como media±desviación estándar. Se utilizó la prueba de la χ2 para evaluar las frecuencias. Las comparaciones entre los grupos se realizaron mediante análisis de la variancia con comparaciones múltiples post hoc mediante la prueba de Bonferroni. Las relaciones entre las variables se determinaron mediante el análisis de correlaciones de Pearson y el análisis de regresión lineal múltiple25. Dichos análisis se realizaron con el programa estadístico SPSS versión 11.0 de Windows (SPSS Inc., Chicago, IL, EE.UU.). En todos los casos los valores de p<0,05 se consideraron significativos.
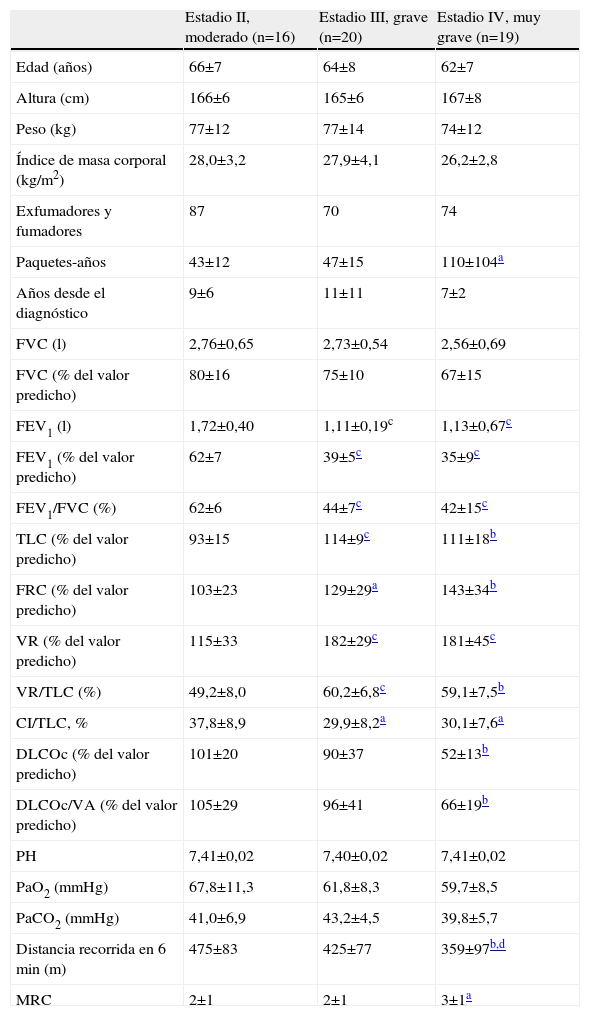
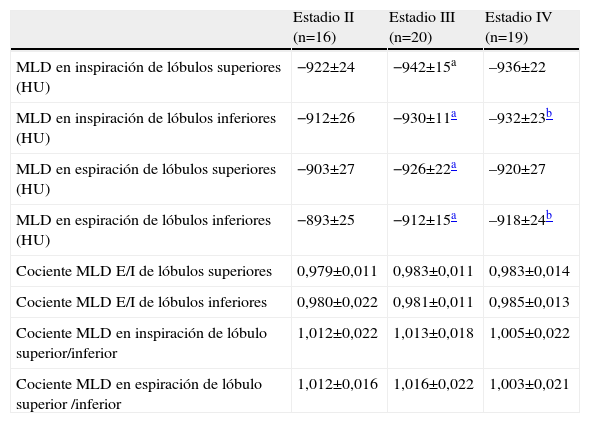
ResultadosLas características de los pacientes y los resultados de las pruebas de función pulmonar se muestran en la tabla 1. En la tabla 2 se recogen los resultados del análisis de máscara de densidad en la TACAR según la clasificación GOLD. Las MLD en inspiración y espiración de los lóbulos inferiores eran menores en los pacientes con EPOC muy grave y grave que en aquéllos con enfermedad moderada. Por otra parte, las únicas diferencias en la MLD de los lóbulos superiores se observaron entre los pacientes con EPOC moderada y grave. Las MLD en inspiración y espiración y los cocientes superior/inferior fueron similares en los 3 grados de gravedad de la EPOC.
Características clínicas y funcionales de los varones con EPOC según la clasificación de la Global Initiative for Chronic Obstrutive Lung Disease (GOLD)
| Estadio II, moderado (n=16) | Estadio III, grave (n=20) | Estadio IV, muy grave (n=19) | |
| Edad (años) | 66±7 | 64±8 | 62±7 |
| Altura (cm) | 166±6 | 165±6 | 167±8 |
| Peso (kg) | 77±12 | 77±14 | 74±12 |
| Índice de masa corporal (kg/m2) | 28,0±3,2 | 27,9±4,1 | 26,2±2,8 |
| Exfumadores y fumadores | 87 | 70 | 74 |
| Paquetes-años | 43±12 | 47±15 | 110±104a |
| Años desde el diagnóstico | 9±6 | 11±11 | 7±2 |
| FVC (l) | 2,76±0,65 | 2,73±0,54 | 2,56±0,69 |
| FVC (% del valor predicho) | 80±16 | 75±10 | 67±15 |
| FEV1 (l) | 1,72±0,40 | 1,11±0,19c | 1,13±0,67c |
| FEV1 (% del valor predicho) | 62±7 | 39±5c | 35±9c |
| FEV1/FVC (%) | 62±6 | 44±7c | 42±15c |
| TLC (% del valor predicho) | 93±15 | 114±9c | 111±18b |
| FRC (% del valor predicho) | 103±23 | 129±29a | 143±34b |
| VR (% del valor predicho) | 115±33 | 182±29c | 181±45c |
| VR/TLC (%) | 49,2±8,0 | 60,2±6,8c | 59,1±7,5b |
| CI/TLC, % | 37,8±8,9 | 29,9±8,2a | 30,1±7,6a |
| DLCOc (% del valor predicho) | 101±20 | 90±37 | 52±13b |
| DLCOc/VA (% del valor predicho) | 105±29 | 96±41 | 66±19b |
| PH | 7,41±0,02 | 7,40±0,02 | 7,41±0,02 |
| PaO2 (mmHg) | 67,8±11,3 | 61,8±8,3 | 59,7±8,5 |
| PaCO2 (mmHg) | 41,0±6,9 | 43,2±4,5 | 39,8±5,7 |
| Distancia recorrida en 6min (m) | 475±83 | 425±77 | 359±97b,d |
| MRC | 2±1 | 2±1 | 3±1a |
Los valores se expresan como media±desviación estándar. CI: capacidad inspiratoria; DLCOc: capacidad de difusión del monóxido de carbono corregida por hemoglobina; FEV1: volumen espiratorio forzado en el primer segundo; FRC: capacidad funcional residual; FVC: capacidad vital forzada; MRC: escala de disnea del Medical Research Council; PaCO2: presión arterial de anhídrido carbónico; PaO2: presión arterial de oxígeno; TLC: capacidad pulmonar total; VA: volumen alveolar; VR: volumen residual.
Medidas en la tomografía computarizada de alta resolución, en varones con EPOC, según la clasificación de la la Global Initiative for Chronic Obstrutive Lung Disease (GOLD)
| Estadio II (n=16) | Estadio III (n=20) | Estadio IV (n=19) | |
| MLD en inspiración de lóbulos superiores (HU) | −922±24 | −942±15a | –936±22 |
| MLD en inspiración de lóbulos inferiores (HU) | −912±26 | −930±11a | –932±23b |
| MLD en espiración de lóbulos superiores (HU) | −903±27 | −926±22a | –920±27 |
| MLD en espiración de lóbulos inferiores (HU) | −893±25 | −912±15a | –918±24b |
| Cociente MLD E/I de lóbulos superiores | 0,979±0,011 | 0,983±0,011 | 0,983±0,014 |
| Cociente MLD E/I de lóbulos inferiores | 0,980±0,022 | 0,981±0,011 | 0,985±0,013 |
| Cociente MLD en inspiración de lóbulo superior/inferior | 1,012±0,022 | 1,013±0,018 | 1,005±0,022 |
| Cociente MLD en espiración de lóbulo superior /inferior | 1,012±0,016 | 1,016±0,022 | 1,003±0,021 |
Los valores se expresan como media±desviación estándar. E/I: espirhatorio/inspiratorio; HU: unidades Hounsfield; MLD: medias de la atenuación pulmonar.
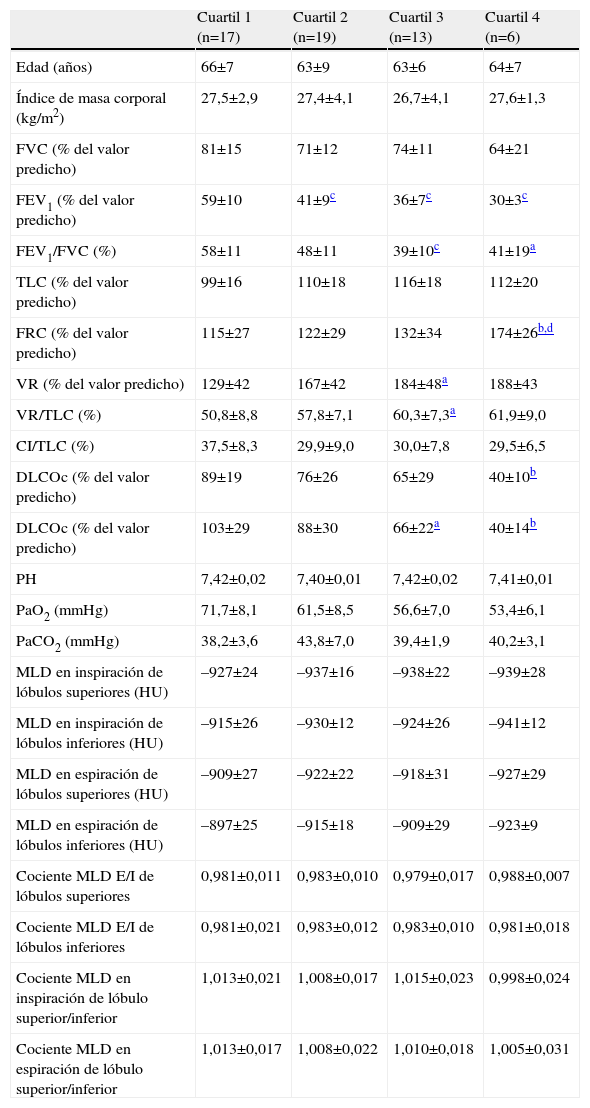
La determinación del índice BODE permitió clasificar a 17 pacientes en el cuartil 1, a 19 en el cuartil 2, a 13 en el cuartil 3 y a 6 en el cuartil 4 (tabla 3). Las atenuaciones en inspiración y espiración fueron similares en los cuatro cuartiles, tanto para el lóbulo superior como para el inferior. No se detectaron diferencias entre los 4 grados de gravedad del índice BODE para los cocientes espiratorio/inspiratorio o superior/inferior.
Medidas tomadas en las tomografías computarizadas de alta resolución, realizadas en inspiración y espiración, según el índice BODE
| Cuartil 1 (n=17) | Cuartil 2 (n=19) | Cuartil 3 (n=13) | Cuartil 4 (n=6) | |
| Edad (años) | 66±7 | 63±9 | 63±6 | 64±7 |
| Índice de masa corporal (kg/m2) | 27,5±2,9 | 27,4±4,1 | 26,7±4,1 | 27,6±1,3 |
| FVC (% del valor predicho) | 81±15 | 71±12 | 74±11 | 64±21 |
| FEV1 (% del valor predicho) | 59±10 | 41±9c | 36±7c | 30±3c |
| FEV1/FVC (%) | 58±11 | 48±11 | 39±10c | 41±19a |
| TLC (% del valor predicho) | 99±16 | 110±18 | 116±18 | 112±20 |
| FRC (% del valor predicho) | 115±27 | 122±29 | 132±34 | 174±26b,d |
| VR (% del valor predicho) | 129±42 | 167±42 | 184±48a | 188±43 |
| VR/TLC (%) | 50,8±8,8 | 57,8±7,1 | 60,3±7,3a | 61,9±9,0 |
| CI/TLC (%) | 37,5±8,3 | 29,9±9,0 | 30,0±7,8 | 29,5±6,5 |
| DLCOc (% del valor predicho) | 89±19 | 76±26 | 65±29 | 40±10b |
| DLCOc (% del valor predicho) | 103±29 | 88±30 | 66±22a | 40±14b |
| PH | 7,42±0,02 | 7,40±0,01 | 7,42±0,02 | 7,41±0,01 |
| PaO2 (mmHg) | 71,7±8,1 | 61,5±8,5 | 56,6±7,0 | 53,4±6,1 |
| PaCO2 (mmHg) | 38,2±3,6 | 43,8±7,0 | 39,4±1,9 | 40,2±3,1 |
| MLD en inspiración de lóbulos superiores (HU) | –927±24 | –937±16 | –938±22 | –939±28 |
| MLD en inspiración de lóbulos inferiores (HU) | –915±26 | –930±12 | –924±26 | –941±12 |
| MLD en espiración de lóbulos superiores (HU) | –909±27 | –922±22 | –918±31 | –927±29 |
| MLD en espiración de lóbulos inferiores (HU) | –897±25 | –915±18 | –909±29 | –923±9 |
| Cociente MLD E/I de lóbulos superiores | 0,981±0,011 | 0,983±0,010 | 0,979±0,017 | 0,988±0,007 |
| Cociente MLD E/I de lóbulos inferiores | 0,981±0,021 | 0,983±0,012 | 0,983±0,010 | 0,981±0,018 |
| Cociente MLD en inspiración de lóbulo superior/inferior | 1,013±0,021 | 1,008±0,017 | 1,015±0,023 | 0,998±0,024 |
| Cociente MLD en espiración de lóbulo superior/inferior | 1,013±0,017 | 1,008±0,022 | 1,010±0,018 | 1,005±0,031 |
Los valores se expresan como media±desviación estándar. CI: capacidad inspiratoria; DLCOc: capacidad de difusión del monóxido de carbono corregida por hemoglobina; E/I: espiratoria/inspiratoria; FEV1: volumen espiratorio forzado en el primer segundo; FRC: capacidad funcional residual; FVC: capacidad vital forzada;HU: unidades Hounsfield; MLD: medias de atenuación pulmonar; PaCO2: presión arterial de anhídrido carbónico; PaO2: presión arterial de oxígeno; TLC: capacidad pulmonar total; VA: volumen alveolar; VR: volumen residual.
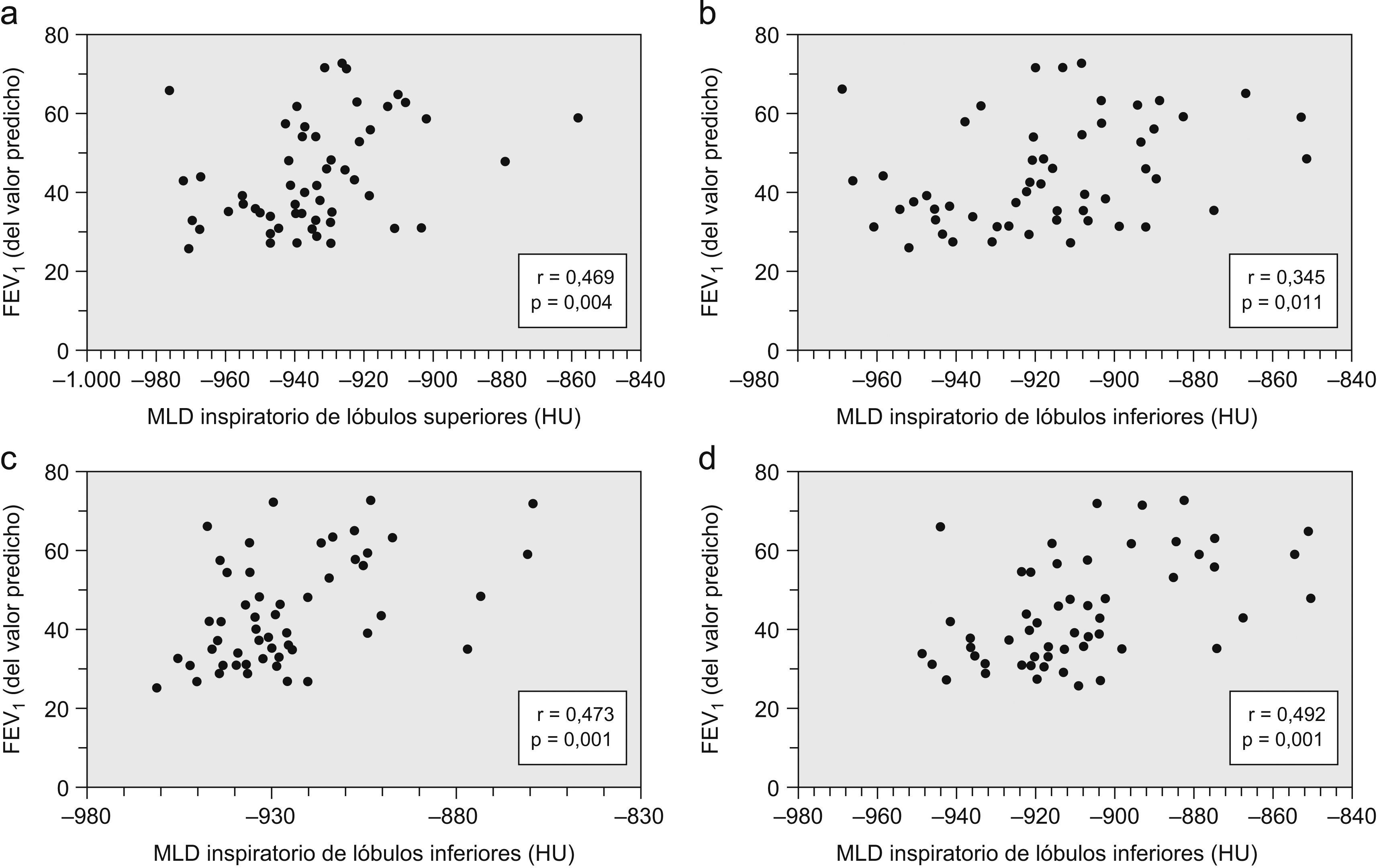
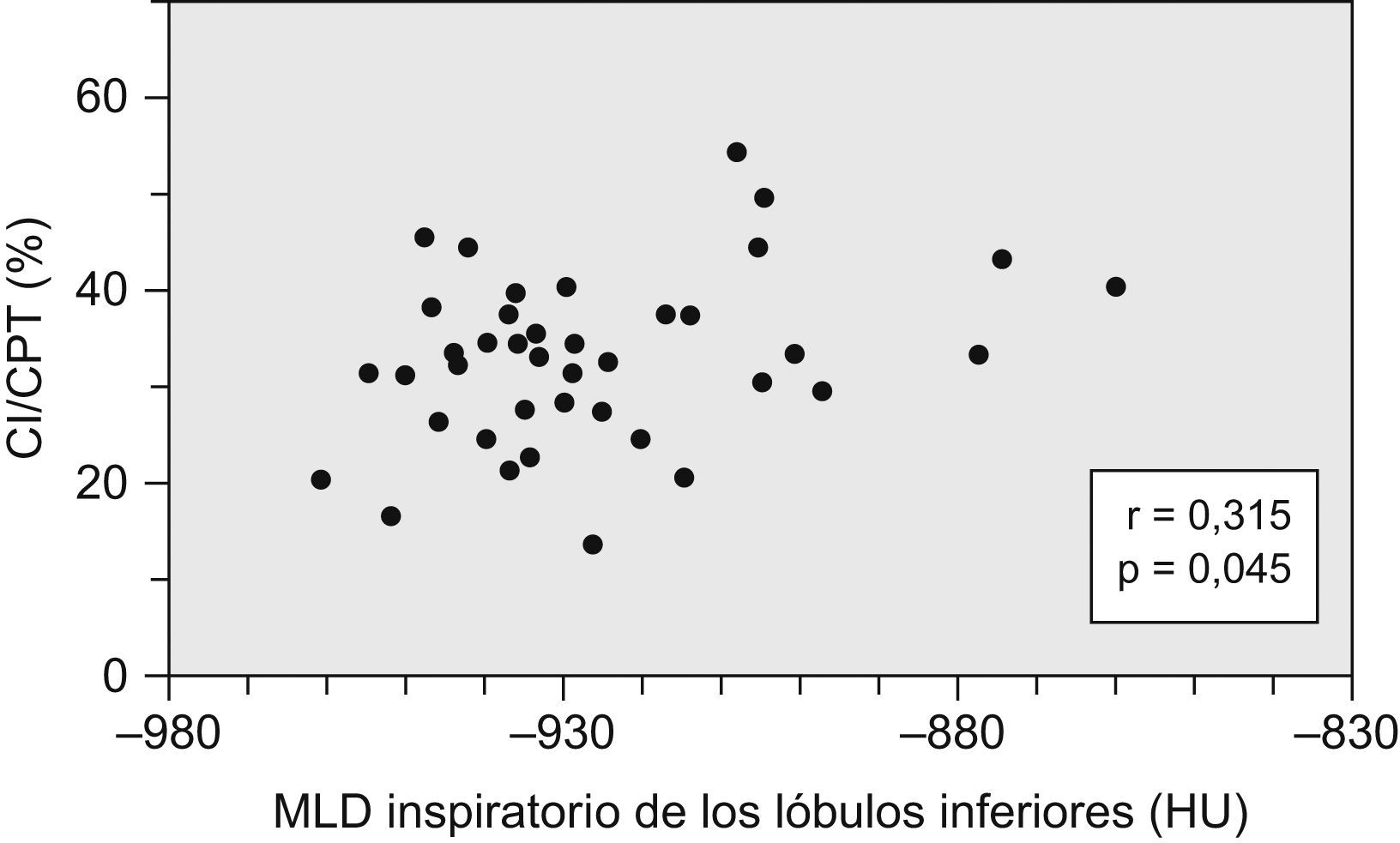
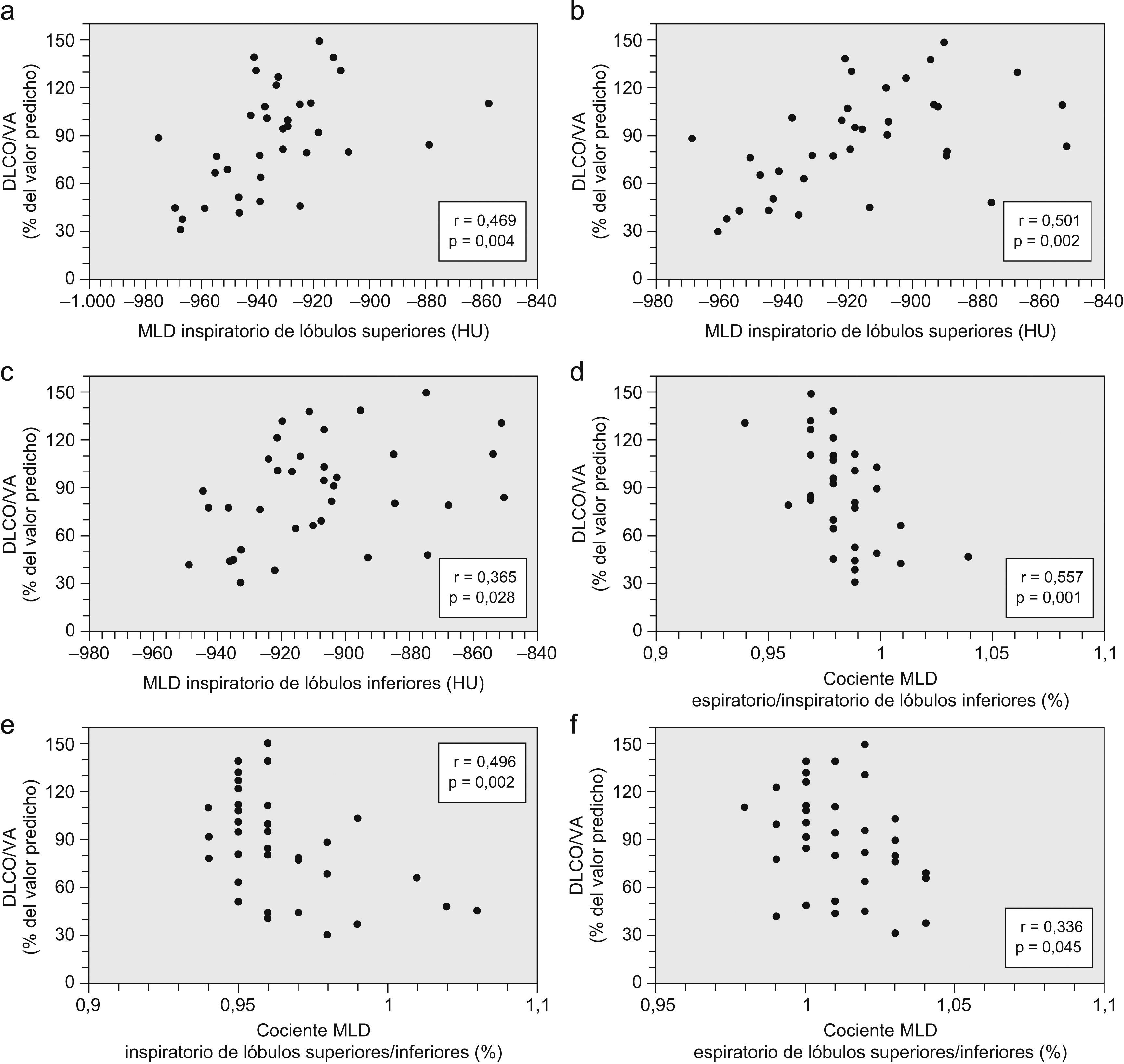
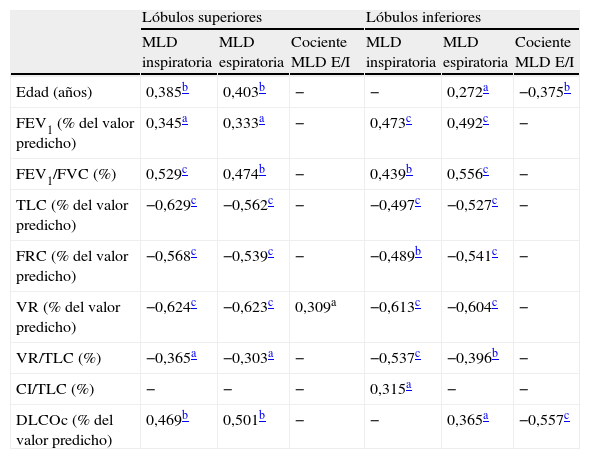
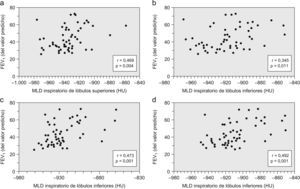
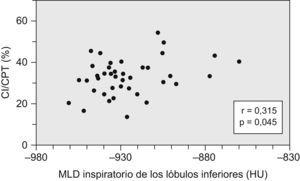
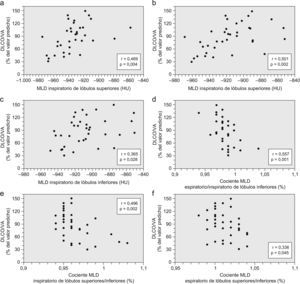
Los resultados del análisis de correlación entre la atenuación pulmonar en la TACAR y los parámetros funcionales se muestran en la tabla 4. Los parámetros relacionados con la limitación del flujo aéreo, el atrapamiento aéreo y la hiperinsuflación pulmonar estaban principalmente relacionados con la atenuación pulmonar tanto del lóbulo superior como del inferior (figs. 1 y 2). Por otra parte, la DLCOc relacionada con el volumen alveolar (fig. 3) estuvo principalmente relacionada con la atenuación del lóbulo superior, así como con el cociente espiratorio/inspiratorio del lóbulo inferior (r=−0,557; p<0,001) y con los cocientes inspiratorios y espiratorio superior/inferior (r=−0,496; p<0,01, y r=−0,336; p<0,05, respectivamente).
Coeficientes de correlación entre la atenuación pulmonar en la tomografía computarizada de alta resolución y las características clínicas de los pacientes con EPOC
| Lóbulos superiores | Lóbulos inferiores | |||||
| MLD inspiratoria | MLD espiratoria | Cociente MLD E/I | MLD inspiratoria | MLD espiratoria | Cociente MLD E/I | |
| Edad (años) | 0,385b | 0,403b | − | − | 0,272a | −0,375b |
| FEV1 (% del valor predicho) | 0,345a | 0,333a | − | 0,473c | 0,492c | − |
| FEV1/FVC (%) | 0,529c | 0,474b | − | 0,439b | 0,556c | − |
| TLC (% del valor predicho) | −0,629c | −0,562c | − | −0,497c | −0,527c | − |
| FRC (% del valor predicho) | −0,568c | −0,539c | − | −0,489b | −0,541c | − |
| VR (% del valor predicho) | −0,624c | −0,623c | 0,309a | −0,613c | −0,604c | − |
| VR/TLC (%) | −0,365a | −0,303a | − | −0,537c | −0,396b | − |
| CI/TLC (%) | − | − | − | 0,315a | − | − |
| DLCOc (% del valor predicho) | 0,469b | 0,501b | − | − | 0,365a | −0,557c |
CI: capacidad inspiratoria; DLCOc: capacidad de difusión del monóxido de carbono corregida por hemoglobina; FEV1: volumen espiratorio forzado en el primer segundo; FRC: capacidad funcional residual; FVC: capacidad vital forzada; MLD: medias de atenuación pulmonar; TLC: capacidad pulmonar total; VA: volumen alveolar; VR: volumen residual.
En el análisis de regresión múltiple, el FEV1% y el cociente FEV1/FVC se relacionaron con la MLD en espiración de los lóbulos inferiores (r2=0,242; p<0,001, y r2=0,306; p=0,001, respectivamente). Por otra parte, la MLD en inspiración de los lóbulos inferiores fue la única variable independiente que se relacionó con los cocientes volumen residual/TLC (r2=0,288; p<0,001) y CI/TLC (r2=0,099; p<0,05). Por último, la DLCOc relacionada con el volumen alveolar (en porcentaje del valor predicho) se relacionó de forma independiente con el cociente MLD espiratorio/inspiratorio de los lóbulos inferiores y con la MLD en inspiración de los lóbulos superiores (r2=0,415; p<0,001).
DiscusiónEl principal resultado de este estudio es que la atenuación del parénquima pulmonar en la evaluación por TACAR es diferente dependiendo de la gravedad de la EPOC, establecida de acuerdo con la clasificación GOLD. Por otra parte, el índice BODE no discierne entre los pacientes con diferentes atenuaciones del parénquima pulmonar. A pesar de que numerosos estudios han abordado la capacidad de la TAC para cuantificar con exactitud el grado de daño pulmonar mediante la correlación de la atenuación pulmonar y la función pulmonar26,27, aún no se habían investigado las diferencias en la atenuación pulmonar de pacientes con EPOC moderada y grave.
Se han desarrollado varios métodos para cuantificar objetivamente el enfisema pulmonar: la medición de la atenuación pulmonar media, las zonas del pulmón ocupadas por valores de atenuación inferiores a los umbrales predeterminados, y un percentil predeterminado de la curva de distribución de la atenuación pulmonar.
En el presente estudio, el programa informático de densitometría pulmonar se utilizó para calcular la atenuación pulmonar media de los lóbulos superiores e inferiores durante una inspiración profunda y una espiración total.
La MLD es un parámetro de TAC muy utilizado para evaluar el enfisema26. Varios estudios han demostrado sus ventajas respecto a otros parámetros de la TAC en la predicción del enfisema. Por ejemplo, Moroni et al28 compararon las mediciones de la atenuación pulmonar obtenidas con y sin control espirométrico mediante TACAR. En dicho estudio, las mediciones de la MLD derivadas de los escáner realizados sin y con control espirométrico eran semejantes, mientras que otras mediciones de la TAC no coincidían. Además, la MLD es un parámetro que se continúa utilizando de forma recurrente en estudios recientes; por ejemplo, en 2009, Akira et al29 publicaron en la American Journal of Roentgenology un estudio cuya finalidad era determinar si las mediciones de la atenuación pulmonar en la inspiración y la espiración, obtenidas a partir de reconstrucciones pulmonares en 3D, reflejan la gravedad de la enfermedad pulmonar obstructiva crónica; para ello, se realizó una TAC multicorte con procesamiento posterior en 3D, en inspiración y espiración completas, a 76 pacientes con EPOC, y se midieron las atenuaciones pulmonares medias inspiratoria y espiratoria, así como el cociente de atenuación pulmonar espiratoria/inspiratoria.
Por consiguiente, decidimos utilizar este parámetro mediante el cálculo de la atenuación media de los lóbulos superiores como de los inferiores en inspiración profunda y espiración total. Establecimos como límite −800/−1.024HU, al suponer que este intervalo incluiría todos los grados de enfisema pulmonar. Aunque los valores de atenuación inferiores a −910HU se han considerado adecuados para establecer objetivamente la presencia de enfisema con TACAR, elegimos valores inferiores para asegurar la inclusión de hipotéticos pacientes con cambios sutiles en la TACAR pero con expresión clínica de EPOC. Según algunos estudios, la atenuación pulmonar media en barridos realizados durante una inspiración completa es de alrededor de −800HU (−806HU) para las personas sin deficiencia ventilatoria, de manera que por debajo de este límite sólo deberían producirse mínimos cambios enfisematosos. Además, incluíamos 2 cortes en espiración completa de cada paciente y, puesto que los valores de atenuación pulmonar en la espiración aumentaron26 (existe una cantidad relativamente grande de vasos y tejido conjuntivo), necesitábamos un intervalo mayor.
Usamos la TAC helicoidal con un algoritmo de reconstrucción de alta frecuencia. Incluimos 2 cortes en espiración completa porque algunos autores han señalado que los barridos obtenidos en espiración completa aportan más información funcional que los obtenidos en inspiración completa11.
En nuestro estudio, la cuantificación por TACAR del parénquima pulmonar nos permitió discriminar entre los grados moderado, grave y muy grave de la clasificación GOLD. No se incluyó a pacientes con EPOC leve porque sus alteraciones morfológicas y funcionales son todavía muy sutiles. En nuestro estudio, la imposibilidad de detectar diferencias entre algunos estadios GOLD en los valores de atenuación de los lóbulos superiores podría atribuirse sencillamente al tamaño pequeño de la muestra. No obstante, y siempre que la diferencia principal entre la EPOC grave y muy grave sea la presencia de insuficiencia respiratoria, nuestros resultados podrían también indicar la escasa contribución que tienen los lóbulos superiores en el intercambio de gas en pacientes con EPOC30.
La relación entre la atenuación pulmonar y los determinantes principales de la clasificación GOLD (FEV1 y cociente FEV1/FVC) se ha documentado en otros estudios10,11,31,32. Sin embargo, no se había documentado hasta ahora si diferentes umbrales de la FEV1 serían capaces de discriminar entre diferentes grados de atenuación pulmonar.
Además, nuestro estudio permite evaluar el efecto de las diferencias pulmonares regionales y la influencia de la adquisición de las imágenes en inspiración‐espiración en la relación entre la atenuación y la función pulmonar. Nakano et al31 ya mostraron que la limitación del flujo aéreo estaba relacionada con el porcentaje de baja atenuación del segmento interno del lóbulo inferior, mientras que la transferencia de gas se relacionaba con el segmento interno de los lóbulos superiores. Otros autores han observado que las mediciones por TACAR en espiración, en comparación con la TACAR en inspiración, se relacionan más estrechamente con deficiencias en la función pulmonar en fumadores con y sin obstrucción de las vías respiratorias16.
En nuestros pacientes, el análisis de regresión múltiple reveló que las medidas pulmonares que reflejaban la obstrucción de las vías respiratorias (FEV1 y FEV1/FVC) se correlacionan con la MLD espiratoria de los lóbulos inferiores, mientras que el atrapamiento aéreo y los índices de hiperinsuflación pulmonar (volumen residual/TLC y CI/TLC) se correlacionan con la MLD en inspiración de los lóbulos inferiores.
La obstrucción de las vías aéreas en los pacientes con EPOC se debe en parte a un aumento de la resistencia intrínseca de las vías respiratorias y a la pérdida de retracción elástica del pulmón. En estos pacientes, se espera que el calibre de las vías respiratorias intraparenquimales sea mucho menor en la espiración que en la inspiración, ya que o bien las paredes de la vía respiratoria son más comprimibles, o la fuerza de tracción del parénquima pulmonar se reduce.
Por otra parte, los parámetros de la TACAR en inspiración podrían representar la extensión relativa de la hiperinsuflación del pulmón, que es la consecuencia principal de la limitación del flujo espiratorio y tiene implicaciones clínicas importantes. En los pacientes con EPOC, la CI en reposo, un reflejo del volumen pulmonar al final de la espiración, se ha correlacionado con la capacidad de ejercicio medida por la captación máxima de oxígeno y la retención de dióxido de carbono durante el ejercicio33. Usamos el cociente CI/TLC porque refleja no sólo el grado de hiperinsuflación del pulmón, sino también la reserva funcional en los pacientes con EPOC34. Es interesante señalar que 2 estudios prospectivos recientes han mostrado que la hiperinsuflación contribuye a la mortalidad por EPOC. Nishimura et al35 encontraron que la hiperinsuflación pulmonar, expresada como cociente volumen residual/TLC, es una potente variable predictiva de la mortalidad. En la misma línea, Casanova et al34 mostraron que el cociente CI/TLC predecía la mortalidad en una cohorte de 689 pacientes con EPOC y un seguimiento medio de 34 meses. Además, el cociente CI/TLC predijo la mortalidad independientemente del índice BODE.
Contrariamente a lo observado con la clasificación GOLD, no se encontraron diferencias en la atenuación pulmonar entre diferentes cuartiles del índice BODE, probablemente debido a la participación de factores extrapulmonares en esta puntuación pronóstica. No obstante, un estudio reciente ha observado que los pacientes con enfisema documentado por TACAR tenían una puntuación BODE mayor que los sujetos sin enfisema documentado por TACAR y los controles36. Varios factores explican esta discordancia. Para empezar, el método que emplearon en la cuantificación del enfisema fue diferente del nuestro: el enfisema se definía como una porción de pulmón superior al 15% que mostrase valores de atenuación inferiores a −950HU, lo que en nuestra opinión podría subestimar cambios enfisematosos sutiles en la TACAR. Por consiguiente, no se habrían considerado algunos pacientes enfisematosos. En segundo lugar, utilizaron un algoritmo de reconstrucción volumétrica, mientras que en este trabajo se empleó uno secuencial para estudiar y cuantificar la atenuación del parénquima pulmonar, ya que consideramos más apropiado lo último para el estudio del espacio intersticial pulmonar y, por consiguiente, del enfisema pulmonar. Además, el número de pacientes con enfisema documentado por TACAR en el estudio de estos autores no fue grande (11 pacientes). Finalmente, el objetivo de su estudio no fue discriminar entre los diferentes grados de EPOC clínica mediante TACAR, por lo que su finalidad era distinta de la nuestra. Pensamos que deben desarrollarse más estudios para determinar si existe correlación entre los cuartiles BODE y los hallazgos de la TACAR.
Por último, esperamos que estos resultados sean relevantes para permitir la estimación radiológica de la gravedad de la EPOC, lo que ayudaría a los médicos a clasificar mejor a cada paciente dentro de los grupos de gravedad de la EPOC, pues esto conduciría a tratamientos e información apropiados.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.