La ventilación mecánica no invasiva (VMNI) actúa en el tratamiento de la insuficiencia respiratoria aguda mejorando las alteraciones del intercambio gaseoso y reduciendo los signos de trabajo respiratorio, la disnea y la actividad de la musculatura respiratoria accesoria. La broncoscopia es una técnica clave en el estudio de las enfermedades respiratorias que es necesario practicar, en ocasiones en pacientes agudos o críticos; la única opción es ser realizada tras intubación orotraqueal (IOT), debido a las posibles complicaciones de la técnica. En la presente revisión evaluamos la evidencia del uso de la VMNI en el transcurso de la broncoscopia, concluyendo que su utilización debiera considerarse, en pacientes graves, como alternativa capaz de evitar complicaciones relacionadas con la IOT y la ventilación mecánica invasiva (VMI), especialmente en pacientes con enfermedad pulmonar obstructiva crónica y con tendencia a la hipercapnia.
Non-invasive mechanical ventilation (NIMV) is used to treat acute respiratory failure by improving gas exchange abnormalities and reducing the signs of respiratory effort, dyspnea and the activity of accessory respiratory muscles. Bronchoscopy is a key technique in the study of respiratory diseases that is necessary to perform in acute and critical patients, often times only after orotracheal intubation (OTI) due to possible complications of the technique. In this review, we evaluate the evidence of NIMV use during bronchoscopy, concluding that its use should be considered in severe patients as an alternative that is capable of preventing the complications related with OTI and mechanical ventilation, especially in patients with chronic obstructive pulmonary disease and with a tendency towards developing hypercapnia.
La ventilación mecánica no invasiva (VMNI) aplicada en el tratamiento de la insuficiencia respiratoria aguda actúa mejorando las alteraciones del intercambio gaseoso y reduciendo los signos de trabajo respiratorio, la disnea y la actividad de la musculatura respiratoria accesoria mientras aparecen los efectos de los fármacos administrados1. Puede así producirse una más rápida estabilización del paciente, evitar la intubación orotraqueal (IOT), la ventilación mecánica invasiva (VMI) y su ingreso en una unidad de cuidados intensivos (UCI)2.
La fibrobroncoscopia (FBC) es una técnica fundamental en el estudio de las enfermedades respiratorias: permite la visualización de la vía aérea superior y las primeras divisiones del árbol traqueobronquial, así como la toma de muestras de la tráquea, bronquios, mediastino y parénquima pulmonar3. Además, es fundamental en el manejo terapéutico de los pacientes con hemoptisis, aspiración de un cuerpo extraño, exceso de secreciones, lesiones neoplásicas y obstrucción de la vía aérea central. Se ha convertido en un elemento esencial en la neumología moderna: en sus indicaciones diagnósticas abarca la mayor parte de las enfermedades respiratorias, y es pieza clave en algunos aspectos de la terapéutica neumológica actual4. Dentro de la broncoscopia, la flexible, introducida en 1968 por Shigeto Ikeda5, es la técnica más utilizada, aunque existen otras modalidades, como la broncoscopia rígida (BR)6 o la ecobroncoscopia (EBUS)7,8.
Ventilación mecánica no invasiva y broncoscopiaAl analizar la FBC en pacientes sometidos a VMNI, deberían diferenciarse los casos agudos (paciente críticos con necesidad de una intervención urgente o preferente) de aquellos con VMNI crónica o domiciliaria, que pudieran requerir una FBC no urgente o programada9.
En el primer grupo se incluyen los pacientes que precisan de una acción terapéutica preferente como la aspiración de secreciones, la intubación guiada por fibrobroncoscopio10 —especialmente en pacientes con alteración de la deglución y riesgo de aspiración pulmonar (miopatías con afectación bulbar)— o la extracción de cuerpos extraños.
La presencia de secreciones abundantes en pacientes con fallo respiratorio agudo es una de las causas de fracaso de la VMNI, que puede contraindicar su empleo11. Sin embargo, la FBC puede facilitar su eliminación, mejorar la ventilación y evitar la intubación traqueal. Esta FBC terapéutica incluso ha permitido la adaptación a la VMNI de pacientes con patologías como la fibrosis quística con exacerbaciones graves y secreciones abundantes12. También deben considerarse aquí los pacientes con infiltrados pulmonares de origen no aclarado que pudieran precisar de la toma de muestras microbiológicas, o aquellos de otra naturaleza (hemorragia alveolar difusa o neumonía organizada13). Otras indicaciones de FBC en pacientes con VMNI incluyen el estudio de atelectasias, hemoptisis, procesos neumónicos de evolución tórpida en pacientes inmunodeprimidos, la sospecha de neoplasia pulmonar, fístulas broncopleurales o fístulas traqueoesofágicas.
La realización de la FBC presenta complicaciones potenciales, que pueden estar relacionadas con la propia realización de la misma, con factores individuales del paciente, o con la habilidad, la cualificación y la experiencia del broncoscopista.
Las alteraciones del intercambio gaseoso que se producen durante la FBC pueden desencadenarse por la propia causa que motivó su realización, pero el broncoscopio de por sí también ocasiona disfunciones, ya que ocupa alrededor del 10% de la luz traqueal —disminuyendo su calibre—, aumenta la resistencia de la vía aérea y reduce el volumen corriente. El impacto de la FBC sobre el aumento de la resistencia del flujo dependerá del calibre de las vías respiratorias y/o del calibre del broncoscopio. El incremento del trabajo respiratorio asociado al aumento de la carga resistiva puede precipitar insuficiencia respiratoria aguda en el paciente crítico. Además, la aplicación de la aspiración por el canal del FBC disminuye las presiones de la vía aérea al final de la espiración, facilitando el cierre alveolar precoz. Ello puede originar que la presión arterial de oxígeno (PaO2) disminuya entre 10 y 20mmHg durante la realización de la FBC14. Estos cambios persisten tras la finalización del procedimiento, y el tiempo que tarda en normalizarse el intercambio gaseoso oscila entre 15min en sujetos normales y varias horas en pacientes con enfermedades pulmonares. Todo ello justifica la utilización de O2 suplementario en pacientes con riesgo de desaturación durante la FBC15.
A lo comentado debe añadirse el efecto irritativo del broncoscopio sobre las superficies mucosas que atraviesa a su paso, generando frecuentemente tos, náuseas, vómitos, espasmo laríngeo, traqueal o bronquial. Los reflejos anteriormente descritos, en su gran mayoría dependientes de los pares craneales IX, X y XI, ocasionan molestias y sobreestimulación neurovegetativa. Ello se contrarresta con la administración de anestesia tópica, como la lidocaína, o con anestésicos intravenosos como el propofol, empleados en casos de alergia a aquella16,17. La administración de estos anestésicos tópicos, la de suero salino o la realización de técnicas como el lavado broncoalveolar (LBA) pueden empeorar la hipoxemia como consecuencia de una alteración de la relación ventilación-perfusión18. Ello puede agravarse cuando se requiera una mayor sedación con anestesia por la propia intolerancia al procedimiento.
En pacientes con enfermedad pulmonar obstructiva crónica (EPOC) y otras enfermedades obstructivas, el broncoscopio puede promover el atrapamiento de aire al incrementar la capacidad residual funcional hasta en un 17% y aumentar la auto-PEEP. Estos efectos pueden ser deletéreos en pacientes con fallo ventilatorio hipercápnico o en los que inician descompensación de su enfermedad de base19.
Cabe recordar que en ocasiones la FBC se indica en pacientes críticos o de alto riesgo para lograr un diagnóstico etiológico, optando por la IOT para la realización de la FBC o asumiendo un tratamiento empírico en los casos de patología infecciosa pulmonar, con el fin de evitar la exploración. Teniendo en cuenta que asociaciones como la American Thoracic Society contraindican la realización de una FBC con LBA cuando no se logra una PaO2 de 75mmHg o una FiO2 del 90% en ventilación espontánea con aporte de O2, suele optarse por la IOT cuando la FBC es imprescindible20. Sin embargo, la VMI comporta una serie de riesgos en relación con la inserción del tubo endotraqueal, infecciones respiratorias asociadas, problemas intrínsecos de la VMI o aquellos objetivados tras la retirada del tubo endotraqueal. La VMNI es una alternativa capaz de evitar complicaciones relacionadas con la intubación y la ventilación mecánica, sobre todo en pacientes con EPOC y tendencia a la hipercapnia21. Al persistir la ventilación espontánea durante el procedimiento, garantiza el equilibrio de la relación V/Q y la estabilidad hemodinámica, permitiendo que pueda realizarse la FBC22.
Es conocido que la VMNI puede mantener la permeabilidad de la vía aérea, facilitar el drenaje de secreciones y mejorar el trabajo respiratorio. Se ha demostrado que la simple administración de presión continua en vías aéreas (CPAP) puede mejorar el volumen minuto y disminuir la probabilidad de atelectasias. Este hecho es más llamativo en los pacientes con traqueomalacia23. La CPAP, que actúa mediante un mecanismo de tipo «stent neumático», puede incrementar la presión transmural de las vías aéreas centrales, incrementando su diámetro transversal. Sin embargo, este no es el único mecanismo que puede explicar la mejoría en las variables ventilatorias, dado que al elevar el volumen pulmonar incrementa el flujo espiratorio pico, la capacidad funcional residual y la eficacia de la tos, hecho importante, sobre todo, en pacientes con enfermedad neuromuscular o debilidad de la musculatura respiratoria24.
Aunque estrictamente la CPAP no se considera un sistema de VMNI por ausencia de apoyo inspiratorio, se ha comprobado la reducción de riesgo de aparición de fallo respiratorio agudo tras la FBC en los casos en que se ha utilizado este sistema25,26. Otros estudios similares mostraron una mejoría de la relación PaO2/FiO2 a expensas de la elevación de la PaO2, en comparación con pacientes tratados solo con oxigenoterapia convencional27. El efecto beneficioso de la VMNI en la FBC también ha sido confirmado en pacientes con EPOC afectos de neumonía y encefalopatía hipercápnica28,29. Además, se ha demostrado que en la encefalopatía hipercápnica moderada-severa de pacientes con EPOC agudizados, la supervivencia a corto y largo plazo es similar al emplear la VMNI o la VMI, aunque el número de complicaciones de origen séptico es menor en la primera de ellas21.
ProcedimientoEntornoSuele recomendarse la realización en un entorno de UCI o unidad de cuidados intermedios respiratorios o cumpliendo los estándares de una sala de broncoscopia con capacidad para abordar las complicaciones19.
Aplicación de la ventilación mecánica no invasivaEl inicio de la VMNI en un paciente no ventilado previamente debe instaurarse, al menos, 15 o 20min antes de la FBC14,27.
No existen estudios comparativos entre diferentes modalidades de VMNI. Inicialmente se emplearon sistemas de doble presión, modalidad de soporte (IPAP de 17cm y EPAP de 5cm) y FiO2 del 100%30, pero han sido descritos procedimientos con presiones inspiratorias menores y FiO2 del 70%31. Se recomienda una presión de soporte de 10cm durante el procedimiento28. También se ha propuesto la realización de FBC con modo CPAP, en concreto CPAP Boussignac, acoplada a una mascarilla facial26. Este sistema se basa en el denominado principio de la conservación de la energía en movimiento, por el que la entrada de gas a alta velocidad procedente de un caudalímetro, y su paso por unos microcapilares, genera una aceleración en forma de microjets que provoca que las moléculas de aire del jet transfieran una parte de la energía cinética a las moléculas de aire situadas en el cuerpo de la CPAP, que son así aceleradas (efecto de turbulencia o válvula virtual). Esta transformación en presión de la velocidad del gas dependerá del flujo de gas aportado desde el caudalímetro32.
De manera orientativa, se recomienda comenzar con una IPAP de 14-15cm y EPAP de 5cm en sistemas bipresión (o 10cm de presión de soporte, en su caso) y 5cm cuando se emplee CPAP, salvo que se hubieran establecido parámetros diferentes previamente por las características clínicas del paciente27,28. Se suele utilizar una FiO2 que permita obtener una saturación de O2 mayor del 90%. A nivel práctico, ello implica una FiO2 mayor de 0,5 o un flujo entre 6-12 l/min. Preferentemente, suele iniciarse con FiO2 de 1 para disminuir según la tolerancia del paciente33. Obviamente, en la CPAP modelo Boussignac se empleará, para conseguir la presión deseada, el adecuado nivel marcado por el caudalímetro.
El resto de parámetros incluiría, a modo orientativo, el modo S/T (spontaneous/timed), una frecuencia de 4-8 respiraciones mandatorias y una relación I/E (inspiración/espiración) según las características del paciente (habitualmente 1:2, 1:3 en algunos pacientes con obstrucción a flujo aéreo y 1:1 en algunos pacientes restrictivos). En el ventilador que permitiera su monitorización, debiera lograrse un volumen corriente espiratorio (Vt) entre 8-10ml/kg y objetivarse una frecuencia respiratoria siempre menor de 25/min. La disponibilidad de la monitorización de la curva de presión y flujo puede ser de ayuda en la valoración de la interacción paciente-ventilador, aunque faltan aún datos que demuestren la utilidad en este escenario de VMNI y FBC.
InterfasesEn relación con la interfase o mascarilla, se han empleado casi todos los tipos de mascarillas. La más extendida es la mascarilla facial30,31, que permite la entrada por vía oral o nasal del fibrobroncoscopio.
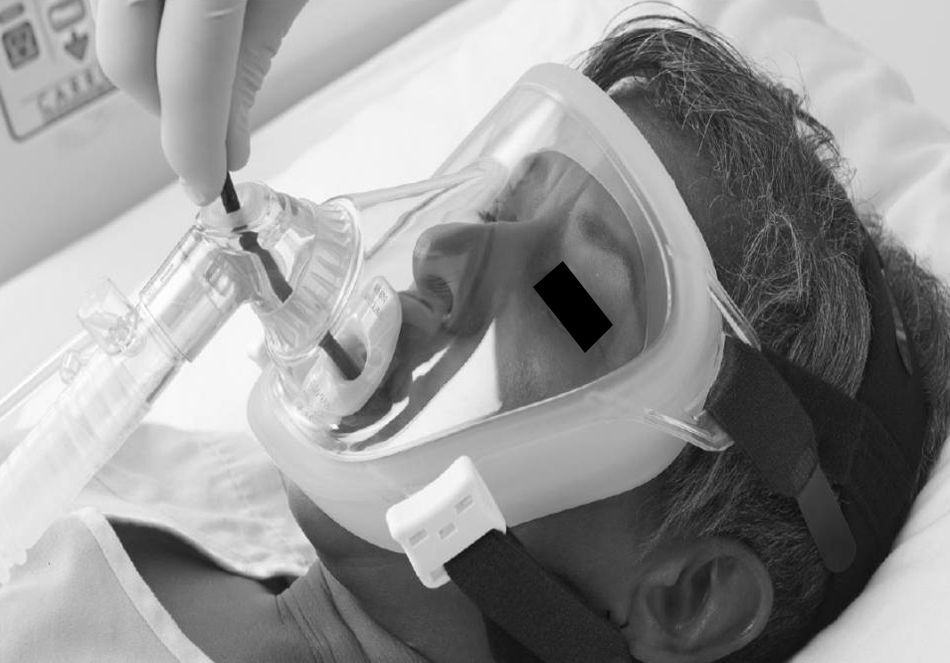
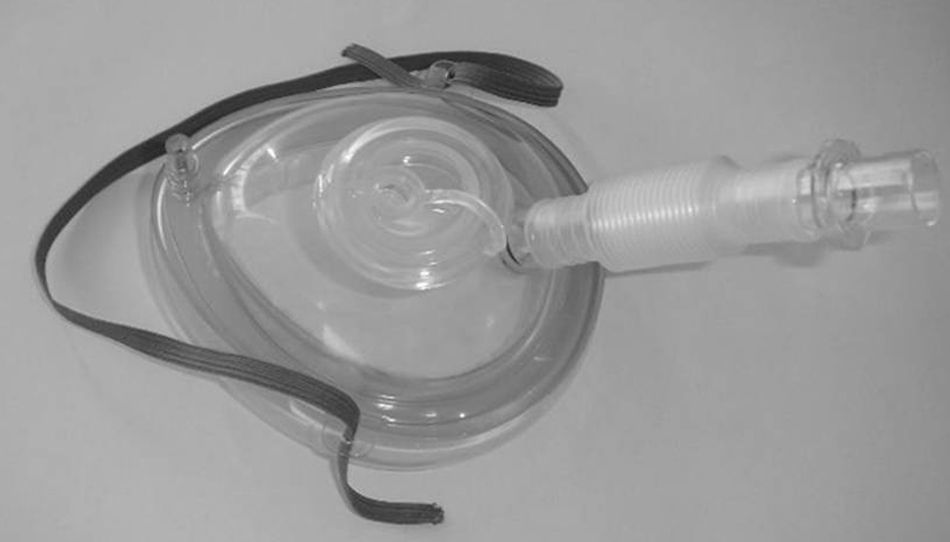
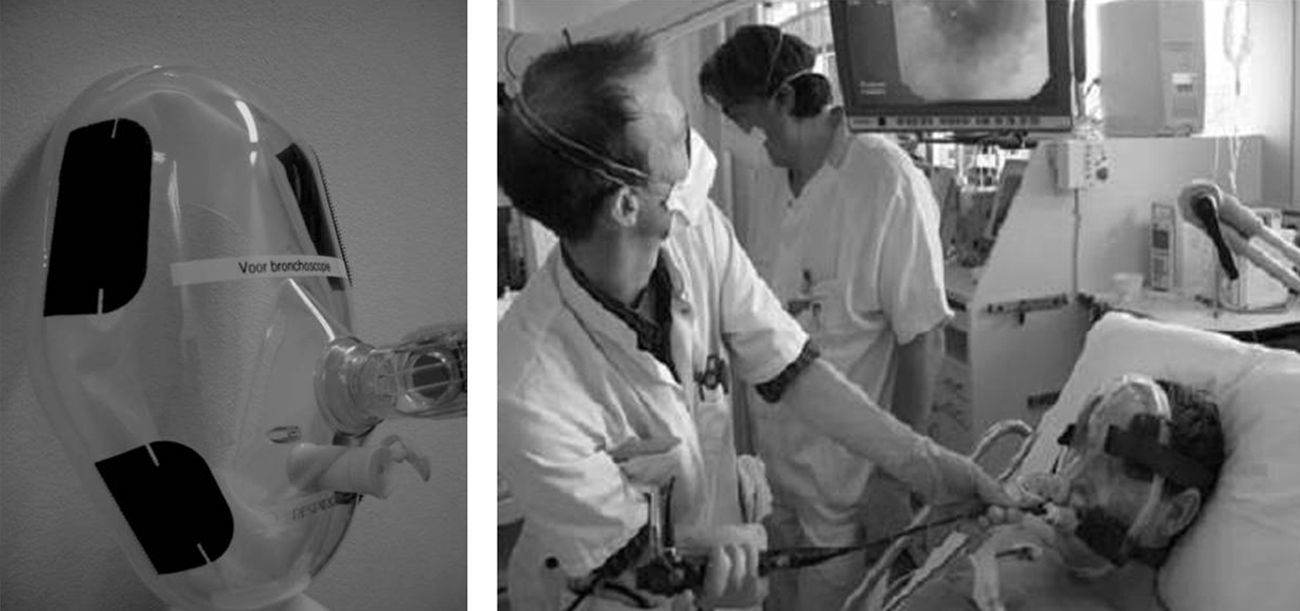
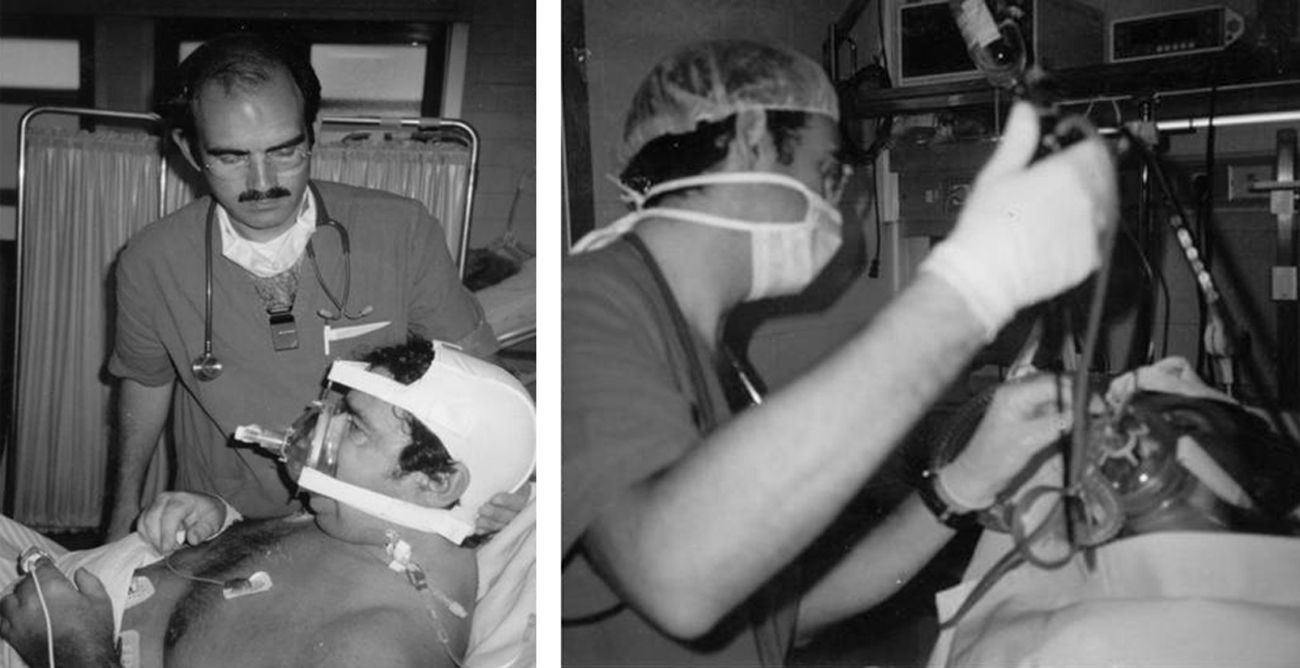
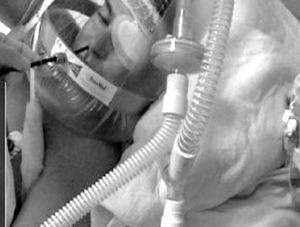
Actualmente las mascarillas faciales endoscópicas suelen disponer de 2 orificios: uno para la administración del gas y un segundo orificio, obturado y distensible, que permite la introducción de un endoscopio (figs. 1 y 2).
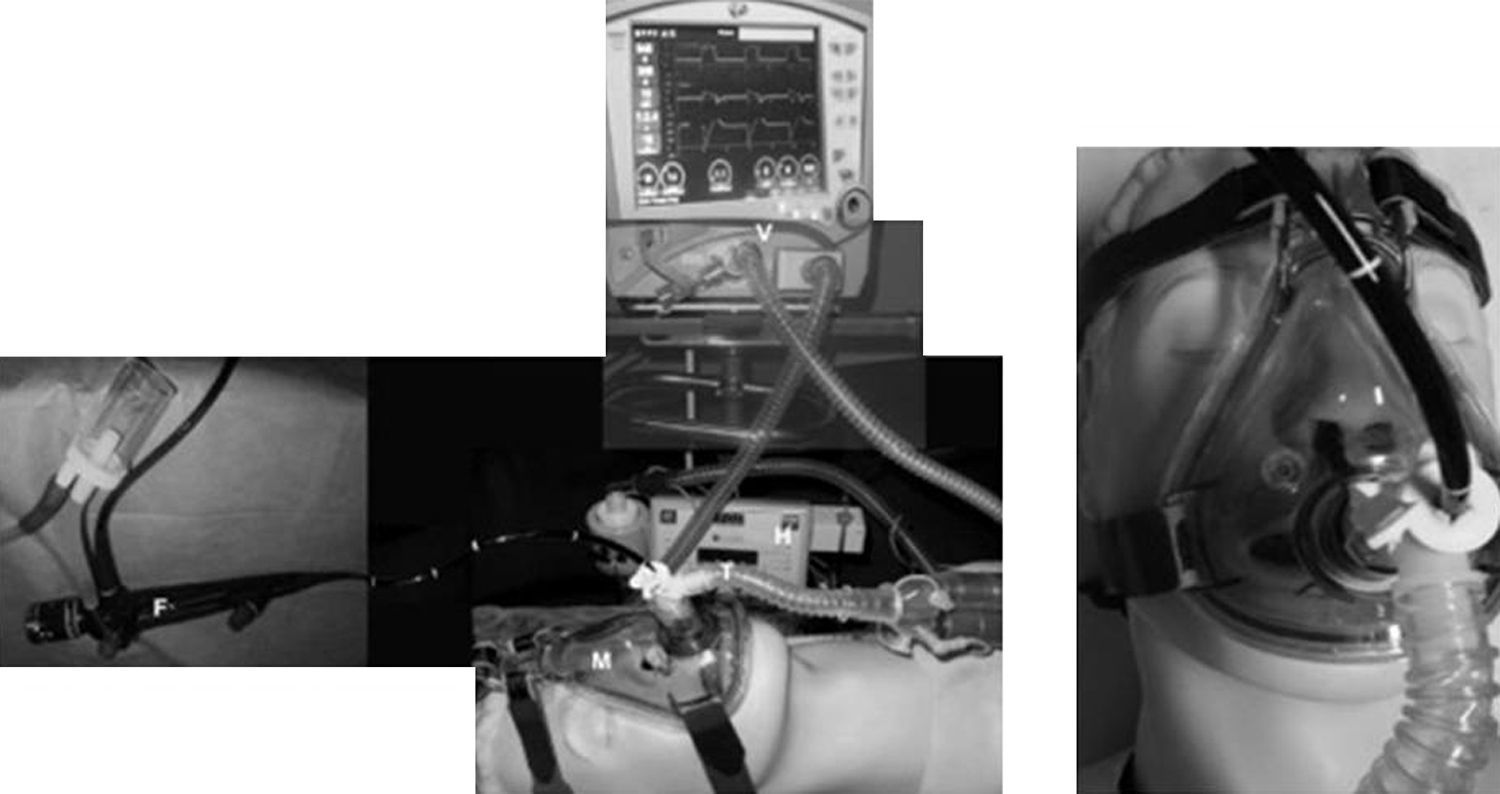
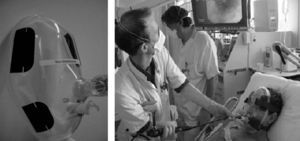
Algunos autores han propuesto modificaciones en las interfases y se basan en la presencia de un segundo orificio con un diafragma de silicona destinado a pasar el fibrobroncoscopio34. También existen conexiones en T universales para el acoplamiento a cualquier mascarilla (fig. 3). Cuando se utiliza una CPAP Boussignac para realizar una FBC, se emplea la máscara facial26. Antonelli describió la posibilidad de realizar FBC con VMNI utilizando una interfase tipo Helmet, que cubre por completo la cabeza del paciente, manteniendo el soporte ventilatorio35 (fig. 4).
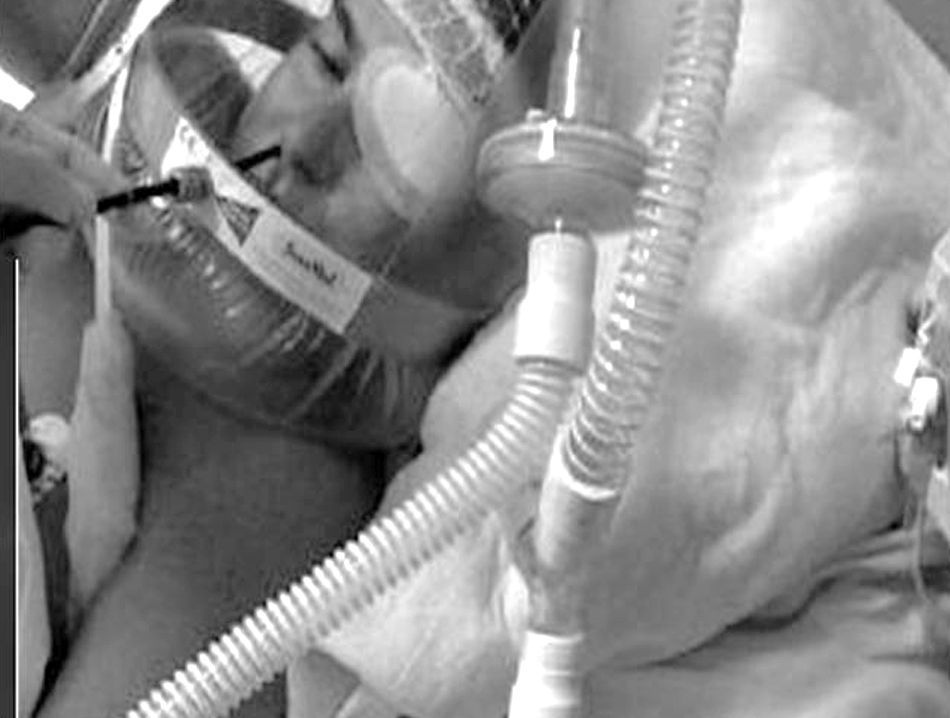
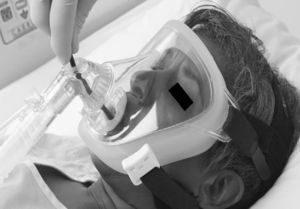
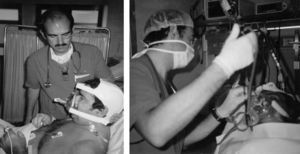
Heunks36 ha diseñado un sistema sobre una máscara facial completa con la inserción de un cilindro de plástico sintético en la máscara para evitar la salida de aire durante la FBC. Sobre 12 pacientes hipoxémicos (PaO2/FiO2: 192±23) se realizaron FBC con LBA sin complicaciones importantes (fig. 5). Un sistema semejante se muestra en la figura 6.
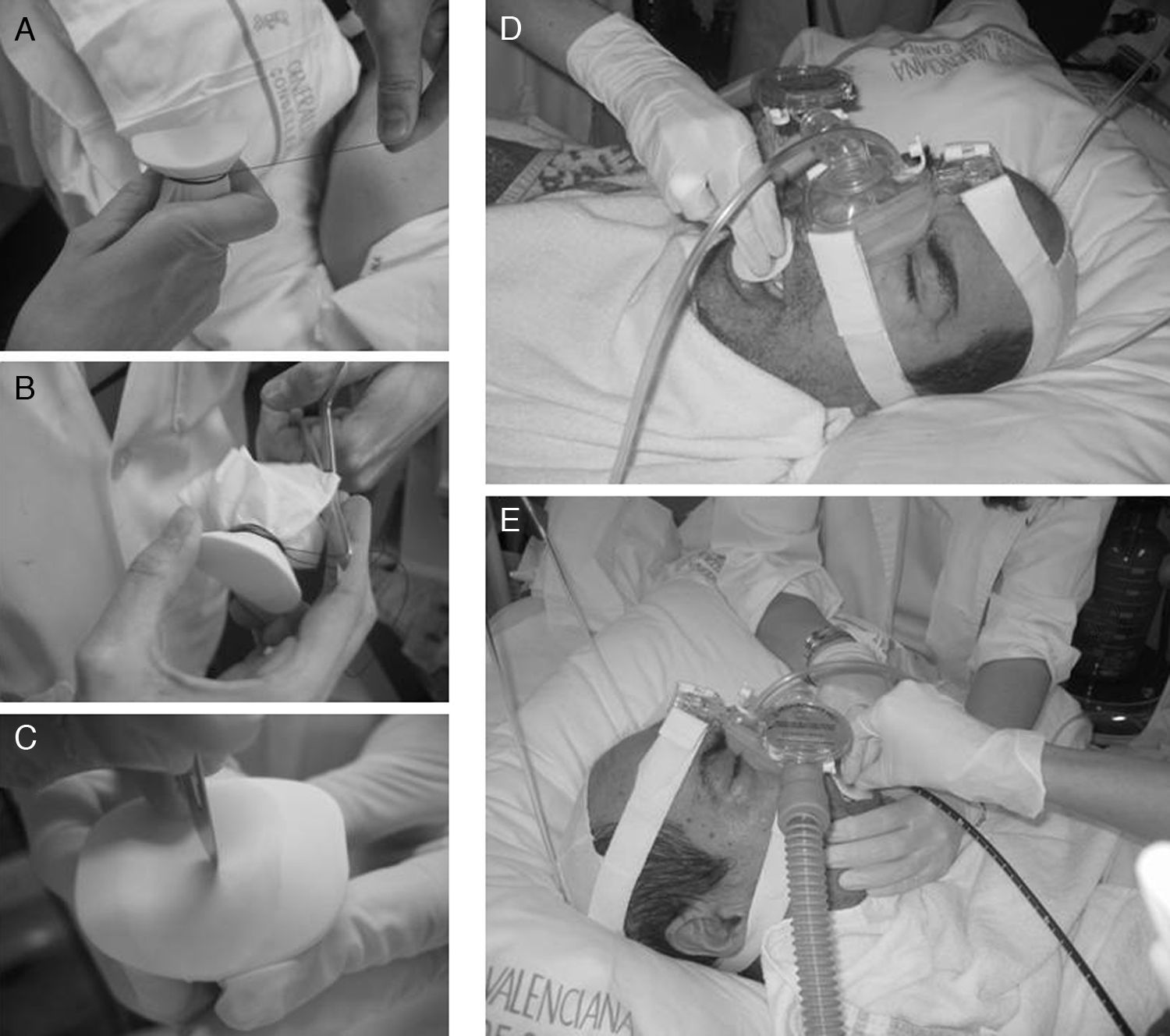
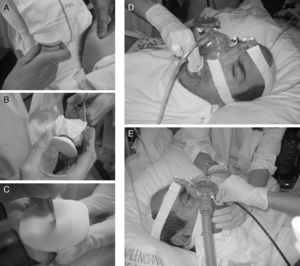
Recientemente, Chiner et al.37 han publicado los resultados de un estudio prospectivo con 35 pacientes, en los que utilizando un sistema artesanal de acoplamiento de una membrana fabricada con un guante de látex a un mordedor bucal sobre el que se realiza una pequeña incisión, se logra la retención de la presión administrada mediante BIPAP a través de una mascarilla nasal, procediendo así a la FBC por vía bucal, con buenos resultados diagnósticos y terapéuticos (fig. 7).
Ventilación mecánica no invasiva practicada con máscara nasal e inserción del fibrobroncoscopio por vía bucal. A) Introducción del mordedor bucal en un guante de látex y sujeción con un hilo de sutura. B) Recorte del material sobrante. C) Mínima incisión en la membrana del mordedor. D) Introducción del mordedor bajo ventilación mecánica no invasiva. E) Inserción del broncoscopio por vía bucal y realización de la técnica con ventilación no invasiva.
La VMNI no implica necesariamente una mayor sedación. De hecho, no se desaconseja, aunque es fundamental disponer de la experiencia necesaria en el manejo de fármacos. Para la anestesia tópica suele emplearse la lidocaína, siguiendo el procedimiento habitual de la FBC. Algunos autores proponen el empleo de propofol para la práctica de la FBC bajo VMNI, lo que permite reducir el malestar de los pacientes sin que presente efectos adversos significativos38.
Posición del pacienteEs recomendable la práctica del procedimiento con el paciente semincorporado, lo que implica la vía anterior para la realización de la FBC. Sin embargo, la propia VMNI ha sido utilizada en decúbito supino para optimizar los parámetros respiratorios en otras exploraciones, como la ecografía transesofágica o la cardiología intervencionista (o en casos de diagnóstico de colapso dinámico de la vía aérea, que precisaron mantener al paciente en esta posición)39–41.
Vía de entradaHay autores que han usado tanto la vía nasal como la oral. En muchos casos está en relación con la interfase utilizada. En aquellos con mascarilla facial, puede emplearse la vía nasal o la oral27,28. La vía oral puede emplearse también con modificaciones y sistemas de acoplamientos a un mordedor bucal, con el empleo concomitante de una mascarilla nasal42. En las exploraciones practicadas con el Helmet, la entrada podría ser nasal u oral, con el paciente incorporado o en decúbito supino35. De igual manera, el uso de CPAP Boussignac permite, al ser un sistema abierto, la entrada por vía oral o nasal26. El control de la pérdida de presión no intencional (interfase) durante la FBC debe ser conocido para poder garantizar la eficacia de la VMNI.
TécnicasLas técnicas empleadas estarán condicionadas por las características de los pacientes. Es habitual el empleo del broncoaspirado, LBA o el catéter protegido para el diagnóstico microbiológico o citológico28,37. Aunque no contraindicada formalmente, algunos autores recomiendan no realizar la biopsia transbronquial mientras el paciente esté sometido a ventilación mecánica, por mayor riesgo de neumotórax y sangrado14,43–45.
DuraciónComo toda intervención en pacientes de riesgo, se recomienda el menor tiempo imprescindible para lograr el propósito de la intervención. Suele variar, aunque la media de duración de una FBC con VMNI en pacientes con neumonía se estableció en torno a 8min28.
Cuidados post-fibrobroncoscopiaSe mantendrá la VMNI con similares parámetros a los previos a la realización de la FBC y un tiempo mínimo entre 15 y 90min después de su finalización12,23,29,41.
ComplicacionesDado que la VMNI ofrece un flujo inspiratorio a presiones positivas, puede presentarse distensión gástrica con incremento del riesgo de broncoaspiración. La presión abdominal generada por la distensión intragástrica puede reducir la capacidad residual funcional y añadir un componente restrictivo46. La VMNI requiere que los pacientes aporten un grado elevado de colaboración, lo que facilita su acople al ventilador, disminuyendo la probabilidad de distensión gástrica y colapso alveolar de tipo restrictivo.
Existen también otras complicaciones propias de la FBC (desaturación, sangrado, mala colaboración, agitación, etc.), para cuya resolución se procederá como en un procedimiento habitual de FBC.
Menos frecuentes son las complicaciones mayores de tipo cardiovascular (arritmias malignas, síndrome coronario agudo, paro cardiaco), que pueden minimizarse por una adecuada selección del paciente y la monitorización durante la FBC.
Los ajustes inmediatos de la VMNI (hipoxemia, hipercapnia, desadaptación, incomodidad) durante la prueba se realizarán según la práctica habitual, que resumimos a continuación:
Se incrementará la EPAP de 2 en 2cmH2O hasta lograr una saturación de O2≥90% si existe hipoxemia. Debe tenerse en cuenta que valores muy altos (mayor de 10) pueden originar un mayor riesgo de distensión gástrica e intolerancia al paciente). En caso de persistir, se incrementaría el flujo o la FiO2.
La hipercapnia se corregiría subiendo la IPAP hasta conseguir buenos márgenes de pH (máximo 25cmH2O) y ajustando la EPAP para evitar rebreathing.
La desadaptación del paciente se objetivará con algunos signos o datos: contracción del esternocleidomastoideo (lo que condicionaría subir la IPAP), contracción abdominal o espiración activa (lo que recomendaría bajar la IPAP), inspiraciones fallidas (que justificarían la subida de la EPAP) y Vt bajo (que obligaría a ajustar la mascarilla, evitar una presión pico mayor de 30cmH2O y permitir fugas si el volumen espirado fuera adecuado)47.
Las lesiones faciales o nasales secundarias al uso de la mascarilla no se incluyen en este apartado, por considerarse que aparecen tras el uso prolongado (horas como mínimo) de la VMNI.
La desaturación persistente del paciente o el deterioro clínico obligarán a la suspensión del procedimiento y a la toma de medidas adicionales, que incluyen la IOT.
Por tanto, es importante subrayar que el procedimiento debe ser evaluado en un ambiente adecuado por personal experto en FBC con VMNI con rápido acceso a la IOT en caso de reanimación cardiopulmonar48.
ContraindicacionesDeben incluirse las propias de la VMNI, como paro cardiaco, encefalopatía grave, sangrado gastrointestinal grave, inestabilidad hemodinámica grave, antecedentes de traumatismo o cirugía facial, incapacidad de ser asegurada una vía aérea permeable o un elevado riesgo de aspiración22. Algunas contraindicaciones relativas son la agitación psicomotora, el fallo respiratorio provocado por causa neurológica o el estado asmático33. No deben olvidarse las relacionadas con las deformidades faciales o intervenciones quirúrgicas faciales, esofágicas o gástricas36. Otras, como la obstrucción de la vía aérea o la incapacidad de expulsar secreciones, pueden llegar a ser indicaciones de broncoscopia con VMNI28. Existen otras contraindicaciones absolutas propias de la FBC, como la falta de colaboración, el ángor inestable, el infarto agudo de miocardio reciente (menos de 20días), arritmias graves, trombopenia inferior a 60.000 o una actividad de protrombina menor del 60% si se prevé la realización de biopsias49. El asma bronquial es una contraindicación relativa con un FEV1 menor del 60%.
Es fundamental recordar que la incapacidad para mantener una saturación de oxígeno superior al 85% a pesar de mantener una elevada FiO2, es indicación de IOT si se plantea la realización de una broncoscopia50 e insistir en la necesidad de contar con una mínima colaboración del paciente. Si ello no fuera posible, se elegiría la IOT o el inicio de tratamiento empírico33.
Situaciones especialesIntubación orotraqueal con fibrobroncoscopia y ventilación mecánica no invasivaLa intubación con FBC se realiza habitualmente de forma urgente en las UCI o de forma programada en los casos de intubación difícil en los servicios de anestesia.
Puede ser peligrosa por el riesgo de hipoxia secundaria tras la apnea inducida por la anestesia general. Se ha empleado la VMNI para asegurar la realización de FBC en pacientes hipoxémicos o hipercápnicos, y podría plantearse su uso para asegurar la intubación traqueal con FBC, incluidas intubaciones previsiblemente difíciles, siempre que se utilice una técnica rigurosa51.
Las mascarillas empleadas serán las faciales con 2 orificios, comentadas previamente. Estas mascarillas permiten una FiO2 de 1 y aseguran una mezcla gaseosa sin fugas. Además, con la ventilación con presión positiva se obtiene una distensión de las estructuras faríngeo-traqueales durante la inspiración y mejora la visualización de la glotis durante la FBC. Al añadir una presión espiratoria positiva al final de la espiración (PEEP), se logra mantener la glotis abierta durante la espiración52.
Muchas intubaciones son nasotraqueales, y en estos casos la técnica consistiría en aplicar la anestesia local de fosas nasales y orofaringe, colocación de la mascarilla endoscópica sobre la cara, conexión al ventilador y, finalmente, introducción del broncoscopio a través del tubo orotraqueal previamente lubrificado progresando hasta llegar a 3cm de la carina principal. Algunos autores administran en este momento midazolam si la saturación con VMNI supera el 94%53. Otros autores prefieren administrarlo una vez visualizada la punta del tubo endotraqueal cuando sobrepasa el extremo distal del broncoscopio. Durante la progresión del tubo endotraqueal utilizando de guía el broncoscopio, este último permanecerá fijo para evitar su salida de la tráquea por la inercia que acompaña a la progresión del tubo endotraqueal sobre el fibrobroncoscopio. En el caso de apreciar una mínima resistencia al deslizamiento del tubo endotraqueal, podría ser útil una mínima retirada del tubo y con una entrada posterior acompañada de una ligera rotación en sentido horario al tiempo que se reintroduce54. Una vez el tubo se encuentra dentro de la tráquea, se hincha el balón del mismo, se retira el broncoscopio, se desconecta la mascarilla y el tubo endotraqueal se conecta al ventilador.
La IOT con fibrobroncoscopio a través de mascarilla facial endoscópica, pero con ventilación manual, es una técnica descrita por algunos grupos. Se trata de una técnica empleada cuando la intubación con laringoscopio no ha sido posible, pero sin antecedentes de empleo previo de la VMNI55.
Ocasionalmente puede realizarse la FBC previa IOT o intubación nasotraqueal con un tubo endotraqueal fino e introduciendo el FBC en paralelo, por fuera del tubo endotraqueal sin hinchar el manguito, lo que permite ventilar simultáneamente al paciente, siempre que el nivel de fuga sea tolerable. Se puede emplear para procedimientos rápidos que impliquen VMI transitoria (mantenimiento del tubo endotraqueal) o VMNI (reversión de sedación y extubación) tras su finalización. Como hemos comentado, estos procedimientos deben ser realizados por equipos con experiencia y en un ambiente de UCI o similar19,48.
Pacientes pediátricosLos pacientes pediátricos tienen un elevado riesgo de sufrir hipoxemia e hipercapnia durante la FBC debido al menor diámetro y a la mayor tendencia al colapso de sus vías aéreas. Además, existe un incremento de la resistencia en las vías creada por el propio broncoscopio56. Cualquier obstrucción por edema, lesión ocupante de espacio o elementos que disminuyan el diámetro transversal con el broncoscopio elevan de manera exponencial la resistencia al flujo de gases (ley de Hagen-Poiseuille), limitando la ventilación por disminuciones significativas en el volumen corriente, la presión pico inspiratoria y el flujo espiratorio57.
La CPAP incrementa la anchura del espacio laríngeo y disminuye la tendencia al colapso de las paredes laterales de la faringe, que son las estructuras más sensibles en la vía aérea superior58. La FBC en pacientes pediátricos con respiración espontánea se ha asociado con una disminución franca del volumen corriente y flujo respiratorio, que puede ser revertida con el uso de CPAP. En pacientes pediátricos con traqueomalacia, donde los volúmenes pulmonares son bajos y la resistencia al flujo espirado es alta, la VMNI mejora los volúmenes pulmonares y el flujo espiratorio59.
Síndrome de apneas-hipopneas del sueño / Síndrome obesidad-hipoventilación / Obesidad mórbidaEn estos pacientes la hipoxemia desencadenada durante la FBC, incrementada en ocasiones por el efecto de la sedación, puede ser verdaderamente importante, hasta el punto de que, aun sin ella, la hipercapnia en vigilia puede empeorar60. La VMNI contrarresta las presiones inspiratorias negativas y la hipotonicidad de los músculos de la vía aérea superior de estos pacientes, aplicando presión positiva sobre la orofaringe33. Además, en este tipo de pacientes se ha descrito que, en condiciones de sedación moderada, el colapso de algunas zonas como la hipofaringe puede limitar la visualización de las estructuras por el broncoscopio61. La presión positiva generada por la VMNI facilita la identificación de las estructuras laríngeas al paso del equipo por la hipofaringe y su introducción a través de las cuerdas. Este aspecto es fundamental en estos casos, que suelen ser considerados como de intubación difícil62.
Broncoscopia rígida y ventilación mecánica no invasivaLas mayores aplicaciones del broncoscopio rígido incluyen la FBC terapéutica (láser, electrocauterio o crioterapia), la colocación de stents traqueobronquiales, la resección de tumores, la dilatación de estenosis traqueobronquial y la extracción de cuerpos extraños, particularmente en niños. Otras indicaciones son el tratamiento de la hemoptisis y la toma de biopsias profundas, obtenidas con la pinza rígida de biopsia, complementada con otras técnicas como la crioterapia bronquial6,63.
La aplicación de presión positiva intermitente y la ventilación en jet son las 2 modalidades ventilatorias habituales que garantizan una ventilación efectiva durante la BR64. Los pacientes también pueden controlarse con una respiración espontánea asistida, pero puede dar lugar a bajos niveles de acidosis respiratoria.
Algunos autores propusieron el uso de la ventilación a presión negativa (VPN), una modalidad de VMNI, como un sistema de ventilación óptima para los procedimientos de BR. Con el objetivo de evaluar la eficacia de VPN mediante sistema de poncho (wrap) durante la aplicación de terapia con láser en lesiones endobronquiales, Vitacca desarrolló un estudio prospectivo aleatorizado y controlado, que confirmó su utilidad en pacientes con apnea, durante el procedimiento de laserterapia bajo anestesia general, evitando el desarrollo de hipercapnia, acidosis respiratoria secundaria y un aumento de las necesidades de aporte de O265. En un estudio posterior, el empleo de la VPN en pacientes sometidos a broncoscopia rígida demostró reducir el uso de opiáceos, el tiempo de recuperación, la posibilidad de reducir la acidosis respiratoria, la necesidad de ventilación manual asistida y la necesidad de O266.
EcobroncoscopiaLa ultrasonografía endobronquial (EBUS) es una técnica diagnóstica mínimamente invasiva que complementa al broncoscopio flexible. Es una herramienta de última generación que combina la videoendoscopia tradicional con la ecografía, que permite obtener imágenes ecográficas de las estructuras que se encuentran fuera de las paredes bronquiales, como son los ganglios linfáticos67. Existen 2 técnicas de EBUS, dependiendo del tipo de transductor: EBUS radial y EBUS lineal.
La técnica se realiza bajo sedación por parte del broncoscopista o anestesia. Tras la colocación a nivel bucal de una cánula orolaríngea, se introduce el ecobroncoscopio por vía oral. Hasta el momento no hay estudios prospectivos publicados sobre la ventaja del uso de la VMNI en la ecobroncoscopia, aunque es probable su empleo en el futuro, probablemente aplicando modalidades de VMNI de alta frecuencia.
Conclusiones y recomendaciones prácticas27,28,48,68,69La VMNI es un procedimiento terapéutico seguro que permite la realización de pruebas complementarias como la FBC, con soporte ventilatorio de eficacia similar a la VMI, aunque debe estar supervisado por personal experto, por lo que se exige ocasionalmente en ambiente de UCI o unidades de cuidados intermedios respiratorios, que cuenten con adecuada monitorización, reconocido manejo en VMNI y preparación por si fuera requerida la IOT y la VMI.
Una vez decidida la realización de la FBC con VMNI, debe haberse iniciado el tratamiento previo con VMNI y comprobado su eficacia en el paciente. Debe contarse con la colaboración del paciente (salvo en niños o en intubaciones programadas).
La FBC debe ser realizada por un broncoscopista con experiencia, que garantice precisión y rapidez en la realización de la prueba. En los casos en los que no se objetive la mejora en el intercambio gaseoso tras un tratamiento previo con VMNI o la incapacidad para mantener una saturación de oxígeno superior al 85% a pesar de mantener una elevada FiO2, se evitará retrasar la IOT, que se programará para ser realizada a la mayor brevedad y en las mejores condiciones posibles.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.