La tuberculosis (TB) es todavía uno de los principales problemas de salud pública a nivel mundial. Las personas con infección tuberculosa latente (ITL) tienen riesgo de desarrollar enfermedad y este está en relación con su estado inmunitario. El desarrollo de TB puede evitarse mediante el tratamiento preventivo (TITL)1. La efectividad del TITL depende de la eficacia de las pautas utilizadas2 y del cumplimiento de estas3.
Nuestro trabajo es un estudio observacional y retrospectivo que tuvo como objetivo evaluar el cumplimiento del TITL y los factores relacionados con el abandono.
Se estudiaron los sujetos con diagnóstico de ITL que iniciaron TITL en la Unidad Clínica de Tuberculosis Vall d’Hebron-Drassanes desde enero de 2011 hasta diciembre de 2016. El diagnóstico de ITL se estableció a partir de la positividad de la prueba de la tuberculina y/o IGRA con estudio radiológico del tórax normal. La pauta de TITL se indicó siguiendo las normativas de la Sociedad Española de Neumología y Cirugía Torácica4.
Se realizó seguimiento clínico/analítico mensual en todos los casos y siempre que el paciente presentara intolerancia. La adherencia se evaluó a través de entrevista y determinación de metabolitos de isoniacida en orina5 y el cumplimiento se definió como la toma de más del 80% de las dosis prescritas.
Se incluyeron 1.113 pacientes consecutivos con una edad media de 29 años, de los que 713 eran varones (64%). Eran inmigrantes 793 (71%), procedentes de más de 50 países (tabla 1). El 70% de los africanos procedían de los países del Magreb (principalmente de Marruecos), el resto eran subsaharianos. El 71,5% de los asiáticos procedían del subcontinente indio (71,5%), siendo Pakistán el país que aportó más pacientes. En el grupo de América Latina destacaron por su aportación Bolivia (23%), Ecuador (21%), Perú (14%), República Dominicana (11%) y Colombia (9%). Y respecto a los incluidos como Europa del Este, Rumanía aportó el 55% del total.
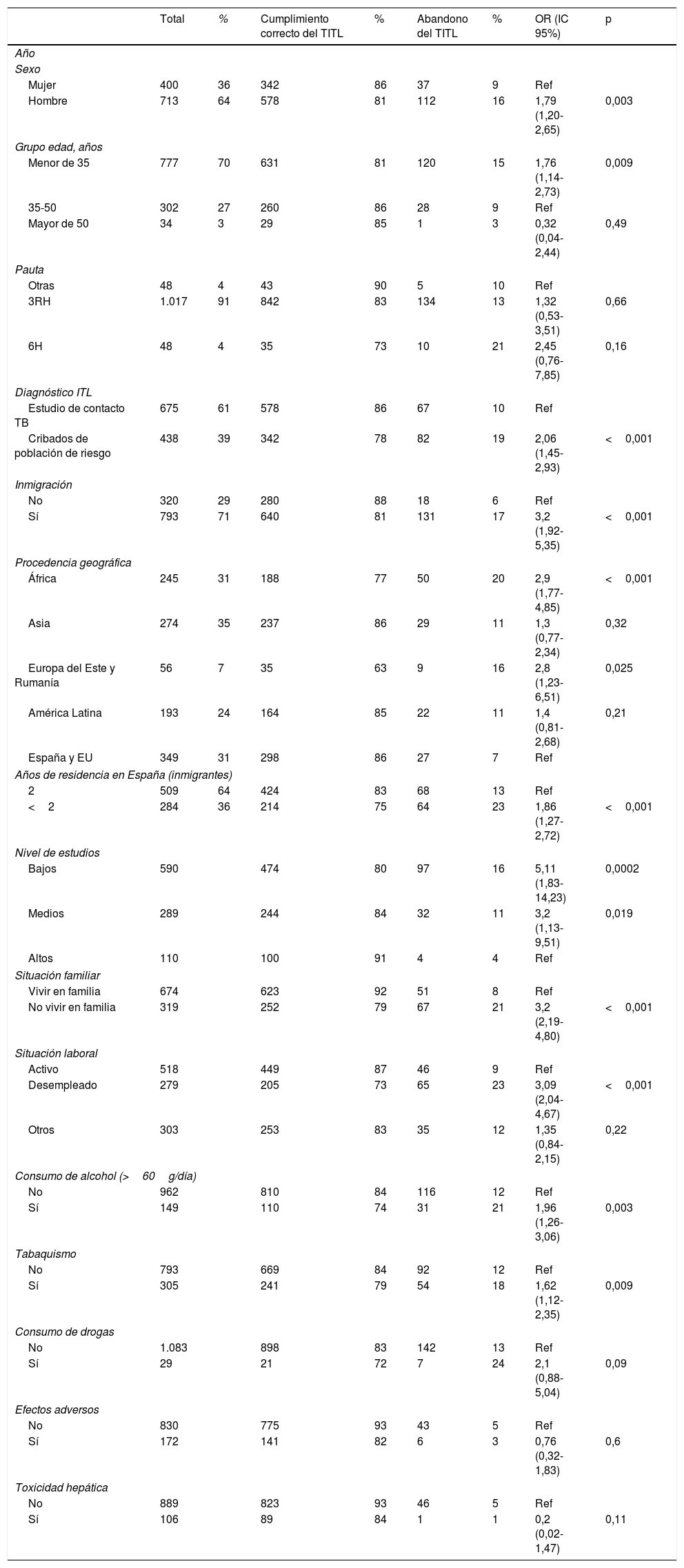
Factores relacionados con el cumplimiento del tratamiento de la infección tuberculosa latente
| Total | % | Cumplimiento correcto del TITL | % | Abandono del TITL | % | OR (IC 95%) | p | |
|---|---|---|---|---|---|---|---|---|
| Año | ||||||||
| Sexo | ||||||||
| Mujer | 400 | 36 | 342 | 86 | 37 | 9 | Ref | |
| Hombre | 713 | 64 | 578 | 81 | 112 | 16 | 1,79 (1,20-2,65) | 0,003 |
| Grupo edad, años | ||||||||
| Menor de 35 | 777 | 70 | 631 | 81 | 120 | 15 | 1,76 (1,14-2,73) | 0,009 |
| 35-50 | 302 | 27 | 260 | 86 | 28 | 9 | Ref | |
| Mayor de 50 | 34 | 3 | 29 | 85 | 1 | 3 | 0,32 (0,04-2,44) | 0,49 |
| Pauta | ||||||||
| Otras | 48 | 4 | 43 | 90 | 5 | 10 | Ref | |
| 3RH | 1.017 | 91 | 842 | 83 | 134 | 13 | 1,32 (0,53-3,51) | 0,66 |
| 6H | 48 | 4 | 35 | 73 | 10 | 21 | 2,45 (0,76-7,85) | 0,16 |
| Diagnóstico ITL | ||||||||
| Estudio de contacto TB | 675 | 61 | 578 | 86 | 67 | 10 | Ref | |
| Cribados de población de riesgo | 438 | 39 | 342 | 78 | 82 | 19 | 2,06 (1,45-2,93) | <0,001 |
| Inmigración | ||||||||
| No | 320 | 29 | 280 | 88 | 18 | 6 | Ref | |
| Sí | 793 | 71 | 640 | 81 | 131 | 17 | 3,2 (1,92-5,35) | <0,001 |
| Procedencia geográfica | ||||||||
| África | 245 | 31 | 188 | 77 | 50 | 20 | 2,9 (1,77-4,85) | <0,001 |
| Asia | 274 | 35 | 237 | 86 | 29 | 11 | 1,3 (0,77-2,34) | 0,32 |
| Europa del Este y Rumanía | 56 | 7 | 35 | 63 | 9 | 16 | 2,8 (1,23-6,51) | 0,025 |
| América Latina | 193 | 24 | 164 | 85 | 22 | 11 | 1,4 (0,81-2,68) | 0,21 |
| España y EU | 349 | 31 | 298 | 86 | 27 | 7 | Ref | |
| Años de residencia en España (inmigrantes) | ||||||||
| 2 | 509 | 64 | 424 | 83 | 68 | 13 | Ref | |
| <2 | 284 | 36 | 214 | 75 | 64 | 23 | 1,86 (1,27-2,72) | <0,001 |
| Nivel de estudios | ||||||||
| Bajos | 590 | 474 | 80 | 97 | 16 | 5,11 (1,83-14,23) | 0,0002 | |
| Medios | 289 | 244 | 84 | 32 | 11 | 3,2 (1,13-9,51) | 0,019 | |
| Altos | 110 | 100 | 91 | 4 | 4 | Ref | ||
| Situación familiar | ||||||||
| Vivir en familia | 674 | 623 | 92 | 51 | 8 | Ref | ||
| No vivir en familia | 319 | 252 | 79 | 67 | 21 | 3,2 (2,19-4,80) | <0,001 | |
| Situación laboral | ||||||||
| Activo | 518 | 449 | 87 | 46 | 9 | Ref | ||
| Desempleado | 279 | 205 | 73 | 65 | 23 | 3,09 (2,04-4,67) | <0,001 | |
| Otros | 303 | 253 | 83 | 35 | 12 | 1,35 (0,84-2,15) | 0,22 | |
| Consumo de alcohol (>60g/día) | ||||||||
| No | 962 | 810 | 84 | 116 | 12 | Ref | ||
| Sí | 149 | 110 | 74 | 31 | 21 | 1,96 (1,26-3,06) | 0,003 | |
| Tabaquismo | ||||||||
| No | 793 | 669 | 84 | 92 | 12 | Ref | ||
| Sí | 305 | 241 | 79 | 54 | 18 | 1,62 (1,12-2,35) | 0,009 | |
| Consumo de drogas | ||||||||
| No | 1.083 | 898 | 83 | 142 | 13 | Ref | ||
| Sí | 29 | 21 | 72 | 7 | 24 | 2,1 (0,88-5,04) | 0,09 | |
| Efectos adversos | ||||||||
| No | 830 | 775 | 93 | 43 | 5 | Ref | ||
| Sí | 172 | 141 | 82 | 6 | 3 | 0,76 (0,32-1,83) | 0,6 | |
| Toxicidad hepática | ||||||||
| No | 889 | 823 | 93 | 46 | 5 | Ref | ||
| Sí | 106 | 89 | 84 | 1 | 1 | 0,2 (0,02-1,47) | 0,11 | |
IC 95%: intervalo de confianza al 95%; OR: odds ratio; TITL: tratamiento de la infección tuberculosa latente; 3RH: rifampicina más isoniacida durante 3 meses; 6H: isoniacida durante 6 meses; Ref: referente.
El motivo de indicación de TITL fue estudio de contacto en 675 (61%) y cribado de población de riesgo en 438 (39%). La pauta TITL de elección fue la combinación de isoniacida y rifampicina durante 3 meses, indicada en 1.017 pacientes (91%). La pauta de isoniacida durante 6 meses se reservó para pacientes en los que se evitó la rifampicina por interacciones con la medicación habitual. La monoterapia con rifampicina durante 4 meses se utilizó en los TITL indicados por contacto con enfermos con TB activa, donde se conocía previamente la existencia de resistencias a la isoniacida y como pauta de rescate cuando se retiró la isoniacida por toxicidad hepática.
Completaron el tratamiento 920 pacientes (83%) y lo abandonaron 150 (13%). Se registraron efectos adversos (EA) en 274 pacientes (24%); el más frecuente fue la elevación de enzimas hepáticas (106; 10%). Únicamente se retiró el TITL en 43 pacientes de los que notificaron EA (4%). En 42 (4%) casos se cambió la pauta inicialmente indicada; de estos, el 98% completaron el TITL.
Las variables relacionadas con el abandono en el análisis de regresión logística fueron: diagnóstico por cribado de población de riesgo (OR 2,06; IC 95% 1,45-2,93), sexo masculino (OR 1,79; IC 95% 1,20-2,65), edad inferior a 35 años (OR 1,76; IC 95% 1,14-2,73), no vivir en familia (OR 3,2; IC 95% 2,19-4,80), bajo nivel educativo (OR 5,11; IC 95% 1,83-14,13), desempleo (OR 3,09; IC 95% 2,04-4,68), tabaquismo (OR 1,62; IC 95% 1,12-2,35), alcoholismo (OR 1,96; IC 95% 1,26-3,06) e inmigración (OR 3,2; IC 95% 1,92-5,35). En el subgrupo de inmigrantes se observa peor cumplimiento en los que llevaban menos de 2 años residiendo en España (OR 1,86; IC 95% 1,27-2,72).
La elección preferente en nuestro centro de la pauta de isoniacida y rifampicina combinadas durante 3 meses se considera fundamental para explicar los resultados de finalización del TITL observados. La utilización de pautas cortas basadas en la rifampicina sola o en combinación con otros fármacos ha demostrado mejorar las tasas de finalización del TITL en comparación con las pautas largas que implican tratamientos de entre 6 y 9 meses, y se consideran una estrategia fundamental para mejorar la adherencia manteniendo la misma eficacia que las pautas tradicionales3,6. En este sentido, en un ensayo clínico controlado realizado por nuestro grupo la utilización de la combinación de isoniacida y rifampicina durante 3 meses demostró una tasa de cumplimiento (72%) significativamente superior que la pauta isoniacida durante 6 meses (52%), sin diferencias respecto a la incidencia de EA, toxicidad hepática ni eficacia7.
El diagnóstico de ITL también es un factor con influencia en el cumplimiento posterior del TITL. Los pacientes en TITL a raíz de un estudio de contacto cumplimentaron mejor el tratamiento (86%) que aquellos a los que se indicó tras cribado de población de riesgo (78%). Un trabajo de revisión publicado recientemente, que recoge tasas de finalización de TITL de 13 estudios prospectivos, muestra que entre los contactos recientes de casos activos de TB el cumplimiento era de un 53 a un 82% y entre las personas procedentes de cribados finalizaron entre un 25 y un 71% de los TITL, atribuyendo este comportamiento a la falta de percepción de riesgo en los sujetos del último grupo8.
En nuestra revisión, los EA y la toxicidad hepática no se asociaron a abandono del TITL, al contrario de lo observado por otros autores9. Durante el seguimiento una cuarta parte de los pacientes notificaron algún tipo de EA, sin embargo, los controles mensuales realizados y el fácil acceso a la Unidad Clínica de Tuberculosis en el momento en que aparece sintomatología facilitó la instauración de medidas para su resolución y evitó el abandono. La elevación de transaminasas ha sido el EA más frecuente, en el 89% de los casos fue asintomática y únicamente en 12 pacientes se catalogó como grave (1%), similar a la objetivada en otros trabajos10,11; en la mayoría de las ocasiones la monitorización analítica, la suspensión temporal del tratamiento y/o el cambio de pauta permitieron completar correctamente el tratamiento.
Respecto a los factores sociodemográficos que se asociaron a incumplimiento, destacan el sexo masculino, ser joven, los pacientes con peor situación social, como era no vivir en familia, un bajo nivel educativo, el desempleo y la inmigración, factores previamente descritos por otros autores como predictores de incumplimiento12,13.
En conclusión, el cumplimiento del TITL observado en nuestro centro fue satisfactorio. A pesar de que la aparición de EA fue muy frecuente, el seguimiento estricto de los pacientes por personal experto y el fácil acceso a consulta facilitó su resolución y la finalización del TITL.