La edición 2017 de la Guía española de la enfermedad pulmonar obstructiva crónica (GesEPOC), con intención de establecer un algoritmo de tratamiento, realiza una estratificación de riesgo de los pacientes en dos niveles: bajo riesgo (BR) y alto riesgo (AR), de acuerdo con tres criterios: función pulmonar, grado de disnea e historial de exacerbaciones1. Dicha estratificación se plantea inicialmente desde un marco teórico como la probabilidad de que el paciente pueda presentar una evolución clínica desfavorable. Tras su publicación, diversos estudios han evaluado su capacidad pronóstica refrendando su utilidad en este aspecto2,3.
Por otro lado, la insuficiencia respiratoria crónica se asocia a una mayor tasa de mortalidad en los pacientes con enfermedad pulmonar obstructiva crónica (EPOC)4. La medición de la saturación de oxígeno periférico mediante oximetría de pulso (SpO2) es fácil de realizar, y valores <92% se correlacionan con la presencia de hipoxemia grave5,6. En base a ello, y con intención de analizar si añadir la medición de SpO2 a los clásicos criterios de riesgo de GesEPOC mejoraría su capacidad pronóstica, realizamos un estudio retrospectivo de pacientes con EPOC estable seguidos en consulta monográfica de neumología. Fueron incluidos pacientes consecutivos diagnosticados de EPOC7 y con historia de tabaquismo (consumo acumulado >10paquetes-año). Se registraron las siguientes variables obtenidas en la primera visita: función pulmonar, índice de masa corporal (IMC), grado de disnea según la escala mMRC, SpO2 basal (realizada por el médico y recogida en situación de estabilidad clínica, respirando aire ambiente, en reposo y previa a la exploración física) e historial de exacerbaciones previo a la inclusión, considerando tanto las exacerbaciones moderadas (que requirieran tratamiento ambulatorio con antibióticos y/o esteroides) como las graves (que requirieran visita a urgencias o ingreso hospitalario). Se clasificó a los enfermos en AR y BR siguiendo los criterios actuales de la guía GesEPOC1 (ante cualquiera de los siguientes criterios el paciente sería categorizado como de AR: FEV1% <50%, disnea ≥2 si está con tratamiento, 2 o más exacerbaciones moderadas o al menos una grave el año anterior), y se comparó con una clasificación en la que los pacientes de AR eran divididos en sujetos con SpO2 <92% (AR-SpO2 <92%) y SpO2 ≥92% (AR-SpO2 ≥92%). Se realizó un análisis de supervivencia mediante regresión de Cox para comparar ambas clasificaciones, obteniéndose el modelo1 con la clasificación tradicional de GesEPOC y el modelo2 incorporando a la clasificación la variable SpO2. Los modelos fueron ajustados por edad y comorbilidad medida con el índice no ajustado de Charlson. Para la comparación de modelos se obtuvo el criterio de información Akaike (AIC). Se obtuvieron curvas de supervivencia ajustadas. La recogida de datos fue aprobada por el comité de ética de la investigación de Santiago-Lugo.
Se incluyeron 710 pacientes, de los cuales 632 eran varones (89%), con una media de edad de 68,3±9,6 años, un FEV1% postBD de 50,5±17,2 y un IMC de 28,3±5,2kg/m2. El 25,9% eran fumadores activos y el índice paquetes-año fue de 59,3±30,7. El índice de comorbilidad de Charlson fue de 1,98±1,41. Eran clasificados de AR 522 pacientes (73,5%) y 188 (26,5%) de BR. La SpO2 media fue de 93,1±4,6%. Ciento sesenta y cuatro (23,1%) presentaban SpO2 <92%, de los cuales 155 eran de AR. El tiempo seguimiento medio fue de 53,9±26,7 meses.
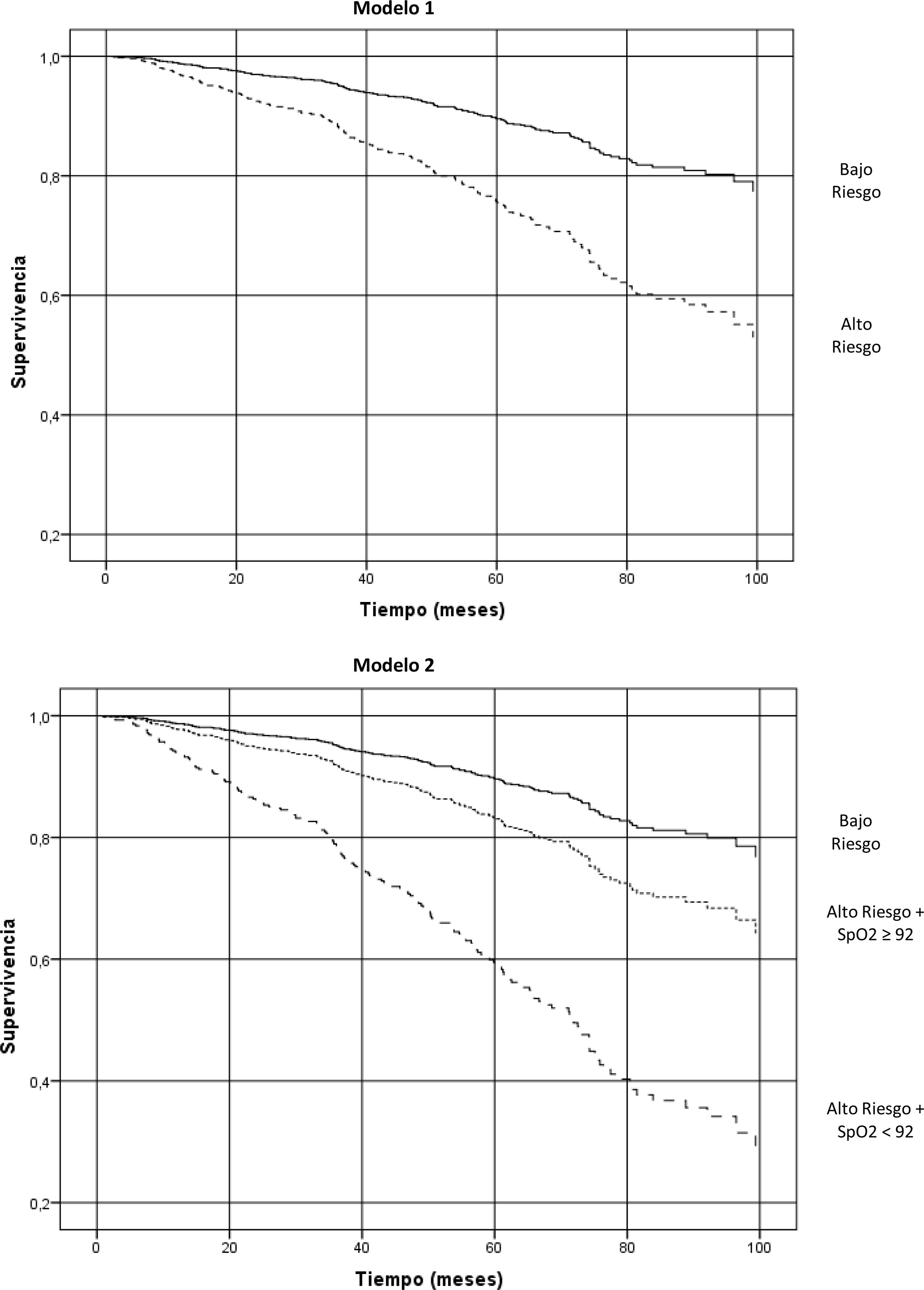
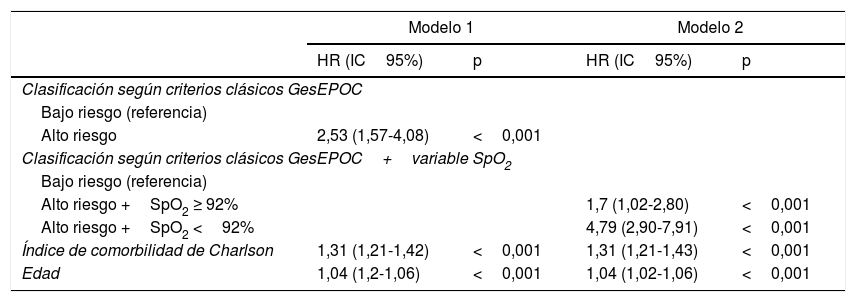
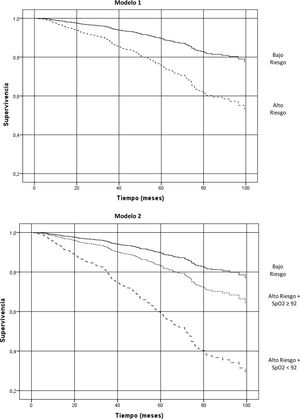
La mortalidad total durante el seguimiento fue del 25,8%, con diferencias significativas entre el grupo BR y el AR (10,1% vs 31,5%: p<0,0001, respectivamente). El grupo AR-SpO2 <92% presentó una mortalidad del 54,2%, frente al 21,9% en el grupo AR-SpO2 ≥92% (p<0,0001). En el análisis de regresión de Cox, en relación con el grupo de BR, los pacientes de AR-SpO2 <92% tienen mayor probabilidad de muerte (HR: 4,79; IC95%: 2,90-7,91; p<0,001) que los de AR-SpO2 ≥92 (HR: 1,7; IC95%: 1,02-2,80; p<0,001) (tabla 1; modelo2) (fig. 1).
Resultados del análisis de regresión logística basados en la clasificación tradicional de GesEPOC (modelo1) o incluyendo la variable saturación basal de oxígeno (modelo2)
| Modelo 1 | Modelo 2 | |||
|---|---|---|---|---|
| HR (IC95%) | p | HR (IC95%) | p | |
| Clasificación según criterios clásicos GesEPOC | ||||
| Bajo riesgo (referencia) | ||||
| Alto riesgo | 2,53 (1,57-4,08) | <0,001 | ||
| Clasificación según criterios clásicos GesEPOC+variable SpO2 | ||||
| Bajo riesgo (referencia) | ||||
| Alto riesgo +SpO2 ≥ 92% | 1,7 (1,02-2,80) | <0,001 | ||
| Alto riesgo +SpO2 <92% | 4,79 (2,90-7,91) | <0,001 | ||
| Índice de comorbilidad de Charlson | 1,31 (1,21-1,42) | <0,001 | 1,31 (1,21-1,43) | <0,001 |
| Edad | 1,04 (1,2-1,06) | <0,001 | 1,04 (1,02-1,06) | <0,001 |
IC 95%: intervalo de confianza del 95%; SpO2: saturación de oxígeno periférico mediante oximetría de pulso.
El modelo1 se ha realizado con la clasificación clásica de GesEPOC de alto y bajo riesgo. En el modelo2 se ha dividido los pacientes de alto riesgo según su valor de SpO2. Ambos modelos han sido ajustados por edad y por índice de comorbilidad de Charlson. El AIC para el modelo1 es de 2.194,44 y para el modelo 2 es de 2.063,95.
En nuestro estudio, al añadir la variable SpO2 a los criterios tradicionales de GesEPOC mejoramos su capacidad pronóstica y permite clasificar a los pacientes de forma más precisa en relación con el riesgo de fallecimiento.
Aspectos como la alteración de la ventilación-perfusión, la desregulación del centro respiratorio o la disfunción de los músculos inspiratorios por la hiperinsuflación pulmonar son factores que contribuyen al desarrollo de hipoxemia en los pacientes con EPOC, lo cual ensombrecerá el pronóstico vital de estos enfermos8-11. Un punto de corte de SpO2 ≥92% permite descartar insuficiencia respiratoria con una alta sensibilidad, y SpO2 ≤88% tiene una alta especificidad para confirmar esta5,6. De forma pragmática y con intención de no excluir a ningún paciente en situación de insuficiencia respiratoria usamos el valor de SpO2 <92%5. En base a ello, no todos cumplirían criterios para iniciar oxigenoterapia crónica domiciliaria (OCD), por lo que una intensa terapia broncodilatadora, la abstención tabáquica mantenida y un precoz inicio de la rehabilitación respiratoria aportaría hipotéticamente una mejora en los valores de SpO2 basal12-15 y, por ende, en su pronóstico vital. Siguiendo el concepto de personalización del tratamiento propuesto por GesEPOC, nuestro planteamiento podría cobrar especial relevancia en aquellos individuos de AR-SpO2 <92% en los que la terapia de inicio recomendada fuera un β2-agonista de acción prolongada-corticoide inhalado, hecho que ocurre en el fenotipo EPOC-asma. Dichos sujetos podrían beneficiarse de un inicio precoz de una doble broncodilatación, al margen del impacto clínico que pudiera alcanzarse con el corticoide inhalado. Por otro lado, sin ser un objetivo del análisis, debemos destacar que en el grupo de BR existían enfermos con SpO2 <92% (9 pacientes). Si bien era un porcentaje muy bajo de pacientes, consideramos que podrían ser necesarios futuros estudios que profundicen en su caracterización para así evaluar su relevancia clínica.
El trabajo actual tiene limitaciones, y sirve esencialmente para generar debate. Es un estudio retrospectivo y está realizado en un único centro. El número de pacientes de BR fue muy bajo, no pudiendo emplear la variable SpO2 en estos sujetos. No podemos descartar que a lo largo del seguimiento a muchos de estos enfermos se le prescribiera OCD, lo que podía haber influido en las cifras de mortalidad descritas. Con intención de no restar potencia estadística, no fue posible estratificar a los pacientes según los rangos de valores de SpO2. A pesar de dichas limitaciones, consideramos que nuestros resultados podrían ser un punto de partida para estudios adecuadamente diseñados que valoren el hecho de añadir la variable SpO2 a los clásicos criterios de AR.
FinanciaciónNo se ha recibido financiación alguna para la realización de este manuscrito.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses relacionado directa o indirectamente con el contenido del manuscrito.