Los grupos de control y tratamiento del tabaquismo de ALAT y SEPAR han colaborado para la realización de este documento en el que se da respuesta, siguiendo metodología PICO, a diferentes interrogantes relacionados con la asistencia sanitaria para ayudar a dejar de fumar a los pacientes con EPOC.
Sus principales recomendaciones son: a)evidencia moderada y recomendación fuerte para realizar espirometría en pacientes con diagnóstico o en fumadores con alto riesgo de padecer EPOC, como instrumento de motivación, en particular evidenciando la edad pulmonar, y con fines diagnósticos y de búsqueda activa de casos; b)evidencia alta y recomendación fuerte para utilizar asesoramiento conductual intenso y específico y tratamiento farmacológico para ayudar a dejar de fumar a fumadores con EPOC; c)evidencia alta y recomendación fuerte para iniciar intervenciones para ayudar a dejar de fumar a fumadores con EPOC mientras se encuentran hospitalizados mejorando al mantener la intervención tras el alta, y d)evidencia alta y recomendación fuerte para la financiación del tratamiento del tabaquismo en fumadores con EPOC por su impacto sobre la salud y la economía de la salud.
The ALAT and SEPAR Treatment and Control of Smoking Groups have collaborated in the preparation of this document which attempts to answer, by way of PICO methodology, different questions on health interventions for helping COPD patients to stop smoking.
The main recommendations are: (i)moderate-quality evidence and strong recommendation for performing spirometry in COPD patients and in smokers with a high risk of developing the disease, as a motivational tool (particularly for showing evidence of lung age), a diagnostic tool, and for active case-finding; (ii)high-quality evidence and strong recommendation for using intensive dedicated behavioral counselling and drug treatment for helping COPD patients to stop smoking; (iii)high-quality evidence and strong recommendation for initiating interventions for helping COPD patients to stop smoking during hospitalization with improvement when the intervention is prolonged after discharge, and (iv)high-quality evidence and strong recommendation for funding treatment of smoking in COPD patients, in view of the impact on health and health economics.
Aproximadamente el 85% de los casos de enfermedad pulmonar obstructiva crónica (EPOC) están causados por el consumo del tabaco. El abandono del tabaquismo es la única medida que se ha mostrado eficaz para detener la progresión de la enfermedad1. Distintos documentos analizan las características de la intervención sanitaria en los fumadores con EPOC para ayudarlos a dejar de fumar2-6. En todos ellos subyacen algunas cuestiones que no han sido respondidas de acuerdo a metodología científica.
Los grupos de control y tratamiento del tabaquismo de la Asociación Latino-Americana del Tórax (ALAT) y de la Sociedad Española de Neumología y Cirugía Torácica (SEPAR) han colaborado para la realización de este documento en el que se da respuesta, siguiendo metodología con preguntas en formato PICO, a diferentes interrogantes relacionados con el tratamiento del tabaquismo a los pacientes con EPOC. El principal objetivo de este documento es proporcionar a los profesionales sanitarios información científica actualizada sobre este asunto.
MetodologíaFormación del grupo colaborador de la guía y formulación de preguntas clínicas. Se formaron cuatro subgrupos de trabajo con la participación de miembros de las dos asociaciones médicas involucradas: ALAT y SEPAR. Estos subgrupos elaboraron una lista de preguntas clínicas y seleccionaron por consenso aquellas que esta guía debía responder. Con la finalidad de concentrar la búsqueda de las evidencias disponibles, todas las preguntas clínicas fueron transformadas al formato PICO o su variante PECO: Paciente (Problema o Población), Intervención o Exposición, Comparación, y Outcome (desenlace relevante)7.
La estrategia de búsqueda bibliográfica se realizó simultáneamente en dos metabuscadores: Tripdatabase y PubMed mediante el uso del MeSH (tabla 1).
Estrategia de búsqueda (palabras clave del Tripdatabase y términos MeSH)
| Pregunta clínica | Pregunta PICO | Estrategia de búsqueda con Términos MeSH |
|---|---|---|
| ¿Es la espirometría un estudio motivador para la cesación tabáquica del paciente fumador con EPOC? | a) P = COPD or Chronic Obstructive Pulmonary Disease I = Smoking Cessation C = Ø O = Lung age | ((((«pulmonary disease, chronic obstructive» [MeSH Terms] OR COPD OR Chronic Obstructive Pulmonary Disease OR COAD OR Chronic Obstructive Airway Disease OR Chronic Obstructive Lung Disease OR Airflow Obstruction, Chronic OR Airflow Obstructions, Chronic OR Chronic Airflow Obstructions OR Chronic Airflow Obstruction))) AND «Smoking Cessation» [MeSH]) AND lung age |
| b) P = COPD or Chronic Obstructive Pulmonary Disease I = Smoking Cessation C = Ø O = («Spirometry» [MeSH] OR Spirometries) | ((((((«pulmonary disease, chronic obstructive» [MeSH Terms] OR COPD OR Chronic Obstructive Pulmonary Disease OR COAD OR Chronic Obstructive Airway Disease OR Chronic Obstructive Lung Disease OR Airflow Obstruction, Chronic OR Airflow Obstructions, Chronic OR Chronic Airflow Obstructions OR Chronic Airflow Obstruction))))) AND ((cessation, smoking OR cessations, smoking OR smoking cessation) OR «Smoking Cessation» [MeSH])) AND («Spirometry» [MeSH] OR Spirometries) | |
| ¿Es diferente el tratamiento del tabaquismo en los fumadores con EPOC que en aquellos sin EPOC? | a) P = COPD or Chronic Obstructive Pulmonary Disease I = Smoking Cessation C = Ø O = Ø | (((((«pulmonary disease, chronic obstructive» [MeSH Terms] OR COPD OR Chronic Obstructive Pulmonary Disease OR COAD OR Chronic Obstructive Airway Disease OR Chronic Obstructive Lung Disease OR Airflow Obstruction, Chronic OR Airflow Obstructions, Chronic OR Chronic Airflow Obstructions OR Chronic Airflow Obstruction))))) AND ((cessation, smoking OR cessations, smoking OR smoking cessation) OR «Smoking Cessation» [MeSH]) by relevance |
| b) P = Smokers with COPD versus Smokers without COPD I = Smoking cessation treatment C = Ø O = Ø | ||
| ¿Es efectiva la intervención para dejar de fumar en fumadores con EPOC ingresados en el hospital? | a) P = COPD or Chronic Obstructive Pulmonary Disease I = Smoking Cessation C = Ø O = Hospitalization | (((((((«pulmonary disease, chronic obstructive» [MeSH Terms] OR COPD OR Chronic Obstructive Pulmonary Disease OR COAD OR Chronic Obstructive Airway Disease OR Chronic Obstructive Lung Disease OR Airflow Obstruction, Chronic OR Airflow Obstructions, Chronic OR Chronic Airflow Obstructions OR Chronic Airflow Obstruction))))) AND ((cessation, smoking OR cessations, smoking OR smoking cessation) OR «Smoking Cessation» [MeSH]))) AND («Hospitalization» [MeSH] OR hospitalizations OR hospitalized) Sort by: Relevance |
| b) P = COPD or Chronic Obstructive Pulmonary Disease I = Smoking Cessation C = Ø O = Exacerbation | ||
| Financiar el tratamiento del tabaquismo en los fumadores con EPOC ¿tendrá impacto sobre la economía de la salud? | P = COPD or Chronic Obstructive Pulmonary Disease I = Smoking Cessation C = Ø O = Financing OR price OR pay OR incentives | ((((((«pulmonary disease, chronic obstructive» [MeSH Terms] OR COPD OR Chronic Obstructive Pulmonary Disease OR COAD OR Chronic Obstructive Airway Disease OR Chronic Obstructive Lung Disease OR Airflow Obstruction, Chronic OR Airflow Obstructions, Chronic OR Chronic Airflow Obstructions OR Chronic Airflow Obstruction))))) AND ((cessation, smoking OR cessations, smoking OR smoking cessation) OR «Smoking Cessation» [MeSH])) AND (financing OR price OR pay OR incentives) |
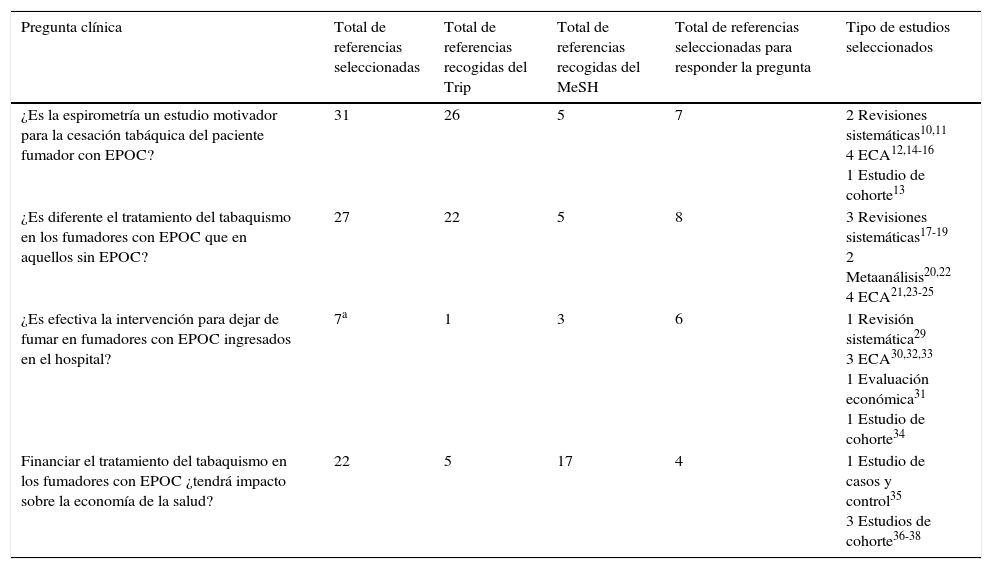
Para los resultados obtenidos de las preguntas PICO se priorizó la selección al nivel más alto de evidencia (ensayos clínicos aleatorizados, metaanálisis y revisiones sistemáticas) que mejor respondiera a la pregunta clínica. Si esto no era posible, se seleccionaron estudios de nivel moderado (estudios observacionales) o bajo (estudios abiertos, serie de casos o consensos) en la jerarquización de evidencias. Se siguió la recomendación de selección algorítmica, principalmente para las preguntas terapéuticas8. Se consideraron publicaciones en idiomas español, portugués e inglés. La fecha de cierre de la última búsqueda fue mayo de 2016 (tabla 2).
Número y tipo de trabajos seleccionados para responder las preguntas clínicas
| Pregunta clínica | Total de referencias seleccionadas | Total de referencias recogidas del Trip | Total de referencias recogidas del MeSH | Total de referencias seleccionadas para responder la pregunta | Tipo de estudios seleccionados |
|---|---|---|---|---|---|
| ¿Es la espirometría un estudio motivador para la cesación tabáquica del paciente fumador con EPOC? | 31 | 26 | 5 | 7 | 2 Revisiones sistemáticas10,11 4 ECA12,14-16 1 Estudio de cohorte13 |
| ¿Es diferente el tratamiento del tabaquismo en los fumadores con EPOC que en aquellos sin EPOC? | 27 | 22 | 5 | 8 | 3 Revisiones sistemáticas17-19 2 Metaanálisis20,22 4 ECA21,23-25 |
| ¿Es efectiva la intervención para dejar de fumar en fumadores con EPOC ingresados en el hospital? | 7a | 1 | 3 | 6 | 1 Revisión sistemática29 3 ECA30,32,33 1 Evaluación económica31 1 Estudio de cohorte34 |
| Financiar el tratamiento del tabaquismo en los fumadores con EPOC ¿tendrá impacto sobre la economía de la salud? | 22 | 5 | 17 | 4 | 1 Estudio de casos y control35 3 Estudios de cohorte36-38 |
Para el análisis crítico de las referencias seleccionadas se usaron las recomendaciones y plantillas propuestas por la red CASPE (www.redcaspe.org). Se utilizó el ACCP grading system, que clasifica las recomendaciones en fuerte1 o débil2 de acuerdo con el balance entre riesgo, beneficio, carga y, en ocasiones, costo. La calidad de la evidencia fue clasificada en alta (A), moderada (B) o baja (C) según el diseño del estudio, consistencia de los resultados y claridad de la evidencia para responder a la pregunta PICO9.
Los autores propusieron dos revisores externos con experiencia en el campo de EPOC y tabaquismo.
Pregunta PICO¿Es la espirometría un estudio motivador para la cesación tabáquica del paciente fumador con EPOC?
JustificaciónSe han hecho esfuerzos importantes para aumentar la tasa de cesación tabáquica utilizando elementos o mediciones motivadoras como la espirometría, la cooximetría y el cálculo de la edad pulmonar. Es de interés conocer las investigaciones clínicas actuales dirigidas a responder esta cuestión.
Selección de búsquedaSe recogieron 31 referencias (MeSH: 5; Tripdatabase: 26), seleccionando 7 estudios para responder la pregunta (2 revisiones sistemáticas, 4 ECA y un estudio de cohorte).
Resumen de la evidenciaUna revisión sistemática encontró beneficios limitados del uso de la espirometría como método motivador para aumentar la cesación tabáquica10, y otra11 evaluó la eficacia de la utilización de instrumentos biomédicos para incrementar la motivación en la cesación tabáquica. Ambas incluyeron 15 ECA, en 2 de los cuales se utilizó la espirometría en atención primaria como instrumento motivador. No encontraron beneficios estadísticamente significativos en la tasa de cesación tabáquica cuando se empleó la espirometría. En el análisis no se evaluó el efecto motivador de la espirometría cuando el resultado era anormal. En este sentido, más recientemente, un ECA12 demostró que la obstrucción bronquial fue el predictor más significativo de cesación tabáquica (OR: 4,215; IC95%: 2,215-7,865). En la misma dirección, otro estudio13 sobre 4.494 fumadores seleccionados de 100.000 sujetos con espirometría obstructiva, fueron llamados para notificarles sobre la EPOC y un consejo breve de cesación tabáquica. Los resultados mostraron una tasa de cesación de 16,3% en los pacientes con obstrucción contra el 12% en aquellos con espirometría normal (p=0,0003). Un ECA14, en el que aleatorizaron a pacientes con EPOC contra fumadores con espirometrías normales y seguimiento de 3años e intervenciones farmacológicas, encontró mayor tasa de abandono en los fumadores con diagnóstico de la EPOC a los 3años de seguimiento (29% versus 14%; p=0,003).
En relación al efecto motivador de explicarle al paciente la edad pulmonar calculada con la espirometría, un ECA15, mostró una tasa de cesación tabáquica a los 12meses del 13,6%, contra el 6,4% en el grupo control (p=0,05; NNT=14).
Un ECA16 no demostró efectividad en confrontar con la espirometría a los fumadores sin diagnóstico previo de la EPOC, a pesar de que la tasa de abstinencia fue del doble en comparación al grupo control (OR: 2,02; IC95%: 0,63-6,46).
Conclusiones y recomendaciones.Evidencia moderada de la espirometría para incentivar el abandono del tabaco en pacientes con EPOC o en fumadores con riesgo de padecerla.
Recomendación fuerte para realizar espirometría en pacientes con diagnóstico o en fumadores sintomáticos, como instrumento de motivación y con fines diagnósticos en la búsqueda activa de casos.
Grado de recomendación: 1B.
Pregunta PICO¿Es diferente el tratamiento del tabaquismo en los fumadores con EPOC que en aquellos sin EPOC?
JustificaciónLas conclusiones de los estudios que analizan el tratamiento del tabaquismo en los fumadores con EPOC sugieren que el tratamiento más eficaz es aquel que combina el asesoramiento psicológico y el tratamiento farmacológico2,17-19.
En cuanto al asesoramiento psicológico, parece claro que cuando la intensidad de este es leve, la eficacia, para este grupo de fumadores, es muy reducida o inexistente. En los fumadores con EPOC el asesoramiento psicológico debe ser intenso tanto en número de sesiones como en tiempo dedicado a cada sesión. Es imprescindible que sea ofertado con empatía, respeto y comprensión para el paciente. Se debe explicar claramente al paciente la íntima relación que existe entre el consumo del tabaco y la EPOC, mostrándole que el único tratamiento que se ha identificado capaz de controlar la evolución crónica de la enfermedad es dejar de fumar. Igualmente, haciendo hincapié en que el abandono del consumo del tabaco en la EPOC contribuye de manera definitiva a controlar los cuatro síntomas cardinales de la EPOC: tos, expectoración, disnea y opresión torácica2,17-19.
Tres tipos de fármacos han sido utilizados en estudios clínicos: Terapia sustitutiva con nicotina (TSN), vareniclina y bupropión. Todos han mostrado que la asociación entre fármaco activo y asesoramiento psicológico es más eficaz que la asociación entre asesoramiento y placebo. TSN y vareniclina han mostrado ser eficaces a los 6 y a los 12meses de seguimiento, en tanto que bupropión solo se mostró eficaz a los 6meses2,17-19.
Algún estudio ha encontrado que las tasas de eficacia en estos pacientes son más altas cuando, además del asesoramiento psicológico, se añade tratamiento farmacológico intenso (durante más de 3meses o en combinación de varios fármacos o utilizando altas dosis de fármaco)3,4.
Es importante determinar cuáles son los componentes imprescindibles que tiene que tener el asesoramiento psicológico en estos fumadores para que sea más eficaz. Además, también es relevante determinar cómo conseguir un tratamiento farmacológico de mayor eficacia.
Selección de búsquedaSe recogieron 31 referencias (MeSH: 5; Tripdatabase: 22), seleccionando 8 estudios para responder la pregunta (3 revisiones sistemáticas, 2 metaanálisis, 2 ECA y un estudio de corte transversal).
Resumen de la evidenciaUna de las primeras revisiones sobre tratamiento del tabaquismo en fumadores con EPOC mostró que la combinación de asesoramiento conductual y tratamiento farmacológico era superior a la no utilización de tratamiento (RR: 4,0; IC95%: 3,25-4,93) o a la utilización de solo asesoramiento conductual (RR: 4,19; IC95%: 3,41-5,15)17.
Otro metaanálisis evaluó a 7.332 pacientes con EPOC que recibieron diferentes tratamientos para dejar de fumar, encontrando que la combinación de asesoramiento conductual más TSN fue el tipo de intervención más eficaz (OR: 5,08; p<0,0001) frente a solo asesoramiento conductual (OR: 2,8; p=0,001) y frente a asesoramiento conductual en combinación con un antidepresivo (OR: 3,32; p=0,002). El asesoramiento conductual solo rozó la eficacia cuando se comparó con los cuidados usuales (OR: 1,81; p=0,07)20.
Otro estudio comparó la eficacia de un programa de tratamiento del tabaquismo de alta intensidad en fumadores con EPOC con la de los cuidados habituales. El programa de alta intensidad consistió en la combinación de tratamiento farmacológico más hospitalización durante 2semanas recibiendo asesoramiento conductual intenso; además se programaban contactos telefónicos y seguimiento continuo durante un período de 1 a 3años. Las cifras de abstinencia en el grupo que recibió el tratamiento intenso fueron del 52 y del 38% al año y a los 3años de seguimiento, en tanto que las cifras en el grupo que recibió los cuidados usuales fueron del 7 y del 10%, respectivamente21.
Probablemente uno de los estudios más clarificadores ha sido el de Hoogendoon et al.18, quienes realizaron una revisión sistemática de los diferentes ensayos clínicos en pacientes fumadores con EPOC. Las diferentes intervenciones fueron agrupadas en cuatro categorías: cuidados usuales, intervención mínima, asesoramiento conductual intenso y asesoramiento conductual intenso más tratamiento farmacológico. Las cifras de abstinencia al año de seguimiento para cada una de las categorías fueron: 1,4, 2,6, 6 y 12,3%, respectivamente. Comparado con el tratamiento usual, el coste por año de vida ganado ajustado a calidad para la intervención mínima fue de 16.900euros, para el asesoramiento conductual intenso de 8.200euros y para el asesoramiento conductual intenso más el tratamiento farmacológico de 2.400euros. Los autores concluyen que la combinación de asesoramiento conductual intenso más tratamiento farmacológico es la forma de tratamiento del tabaquismo en la EPOC más eficaz y con mejor relación coste/efectividad
Bartlett et al.22 evaluaron 17 ensayos aleatorizados para saber qué tipo de asesoramiento conductual para dejar de fumar es más eficaz en fumadores con EPOC. Los datos de este estudio muestran que hay cinco técnicas de asesoramiento que se asocian significativamente con los mejores resultados: 1)la planificación de acciones; 2)el registro de la evolución de los síntomas, logros y fracasos; 3)el control del peso; 4)el apoyo social, y 5)explicar claramente la relación entre EPOC y tabaquismo.
Dos ensayos clínicos han analizado la eficacia y la seguridad de uso de bupropión. Uno de ellos encontró que bupropión fue más eficaz que placebo en obtener abstinencia continua a los 6 meses de seguimiento (16 vs 9%; p<0,05)23. El otro mostró similares resultados, también a los 6meses de seguimiento (diferencia del 18,9% [IC95%: 3,6-34,2%]; p=0,0224.
Un ECA ha analizado la eficacia y la seguridad de uso de vareniclina, demostrando que vareniclina fue más eficaz que placebo para ayudar a dejar de fumar al tercer, sexto y duodécimo mes de seguimiento. Al cabo del año las cifras fueron del 18,6% vs 5,6% (OR: 4,04 [IC95%: 2,13-7,67]; p<0.0001)25.
Recientemente una revisión que analiza 16 estudios que incluyeron más de 13.000 pacientes ha llegado a conclusiones similares a las aquí comentadas26.
Conclusiones y recomendacionesLa evidencia disponible nos indica que la intervención más eficaz para ayudar a dejar de fumar en los sujetos con EPOC es la combinación de asesoramiento conductual intenso más tratamiento farmacológico. Esta intervención resulta altamente coste-efectiva.
El asesoramiento conductual debe ser intenso y duradero; a mayor intensidad y a mayor duración del mismo, se obtiene una más alta eficacia.
Como tratamiento farmacológico se pueden utilizar cualquiera de estos tres fármacos: TSN, bupropión y vareniclina. Bupropión mostró eficacia solo a 6meses de seguimiento. TSN y vareniclina han mostrado ser eficaces a los 6 y a los 12meses de seguimiento.
Evidencia alta y recomendación fuerte para utilizar asesoramiento conductual intenso y tratamiento farmacológico (TSN y vareniclina mejor que bupropión) para ayudar a dejar de fumar a fumadores con EPOC.
Grado de recomendación: 1A.
Pregunta PICO¿Es efectiva la intervención para dejar de fumar en fumadores con EPOC ingresados en el hospital?
JustificaciónAlrededor del 25-35% de los pacientes con EPOC que ingresan en un hospital son fumadores. La hospitalización es una situación idónea para ayudar a los fumadores a dejar de serlo. Teniendo en cuenta estas premisas, sería importante que la hospitalización de un sujeto con EPOC fuese utilizada para comprobar su estado con respecto al consumo del tabaco y para intervenir de forma decisiva sobre esa situación27,28.
Selección de búsquedaSe recogieron 7 referencias (MeSH: 3; Tripdatabase: 1 y mediante Snow-balling: 3), seleccionando 6 estudios para responder la pregunta (3 ECA, una revisión sistemática, una evaluación económica y un estudio de cohorte).
Resumen de la evidenciaEn una revisión sistemática se encontró que las intervenciones conductuales intensivas que comienzan en el hospital y continúan durante, al menos, un mes tras el alta aumentan las tasas de abstinencia (RR: 1,37; IC95%: 1,27-1,48)29. Un estudio encontró que la combinación de intervención intensiva más TSN incrementaba las tasas de abstinencia en comparación con intervención intensiva sola (RR: 1,54; IC95%: 1,34-1,79). Pero en otros dos estudios no se pudo comprobar que añadir vareniclina o bupropión aumentase las tasas de abstinencia. Los mismos resultados se encontraron en un subgrupo de fumadores que fueron ingresados por enfermedades cardiovasculares; en este subgrupo una intervención intensiva seguida de soporte posterior incrementó las tasas de abstinencia (RR: 1,42; IC95%: 1,29-1,56) al compararla con una intervención no intensiva.
Un ensayo clínico comparó las tasas de abstinencia en dos grupos de fumadores30. Un grupo recibió intervención intensiva (tratamiento farmacológico gratuito durante 90días, llamadas telefónicas periódicas y refuerzo conductual) y el grupo control solo recibió recomendaciones sobre el uso de la medicación en el momento del alta. La abstinencia puntual a los 6meses fue significativamente más alta en el grupo intervención (26% vs. 15%; RR: 1,71; IC95%: 1,14-2,56; p=0,009; NNT: 9,4; IC95%: 6,4-35,5). Lo mismo ocurrió con las tasas de abstinencia continua a los 6meses (27% vs. 16%; RR: 1,70; IC95%: 1,15-2,51).
Un estudio fármaco-económico analizó el coste-efectividad del modelo Otawa para dejar de fumar en pacientes hospitalizados (OMSC) por diversas patologías, EPOC entre ellas31. El modelo Otawa incluye asesoramiento psicológico y tratamiento farmacológico. Los autores encontraron que el programa OMSC era muy coste-efectivo (1 año de coste por QALY ganado $C1.386; coste de vida ganado por QALY $C68). El estudio mostraba que aplicar el modelo Otawa a 15.326 fumadores ingresados aporta un total de 4.689 abstinentes en un año y prevendría 116 re-hospitalizaciones, 923 estancias y 119 muertes en el conjunto de estas enfermedades crónicas.
Un ensayo clínico llevado a cabo por Borglykke et al.32 comparó las tasas de abstinencia en dos grupos de fumadores con EPOC que acudían al servicio de urgencias de un hospital. Un grupo era aleatorizado a recibir intervención intensa y otro grupo era el control. Los pacientes fueron seguidos al año y a los tres años después de la intervención. Los resultados mostraron que al año de seguimiento la tasa de abstinencia en el grupo de intervención fue significativamente más alta que en el control (30% vs. 13%; OR: 2,83; IC95%: 1,40-5,74). Además, no se encontraron diferencias significativas en cuanto a la cantidad de flemas ni en la supervivencia (50,4% vs. 43,1%; HR: 0,80; IC95%: 0,55-1,16). No obstante, a los 3años de seguimiento se encontró que el grupo de intervención estuvo de forma significativa un menor número días ingresado por EPOC o por otras causas.
Un ensayo clínico33 aleatorizó a 172 pacientes a dos grupos. El grupo de intervención consistió en asesoramiento médico para dejar de fumar, cribado de reflujo gastroesofágico, depresión y/o ansiedad, además de educación de manejo de inhaladores. En comparación con el grupo control, los resultados no mostraron diferencias en cuanto a reingresos o consultas a 30días tras el alta, ni en la tasa de reingresos a 90días.
Otro estudio de una cohorte de pacientes con EPOC ingresados por exacerbación34 examinó la eficacia de la utilización de consejo breve antitabaco mientras los pacientes se encontraban ingresados, y el uso de medicación para ayudar a dejar de fumar una vez que eran dados de alta. Se incluyeron un total de 1.334 pacientes: el 19,8% declararon haber dejado de fumar a los 6 y 12meses de seguimiento, el 17,5% no declararon su estatus, y el 63,7% continuaron fumando. Es de destacar que solo el 33,7% de los pacientes utilizaron medicación para dejar de fumar. Los resultados no encontraron mayores tasas de abstinencia entre los que recibieron medicación para dejar de fumar. Tampoco se encontró asociación entre el consejo para dejar de fumar al alta y la abstinencia, ni entre los que recibieron medicación en las 48h tras el alta o en los que habían sido tratados en el año anterior. Los que recibieron vareniclina presentaron de forma significativa mayores tasas de abstinencia (OR: 2,44; IC95%: 1,48-4,05), y en cambio los que recibieron TSN en monoterapia presentaron los peores resultados (OR: 0,66; IC95%: 0,51-0,85). Los que recibieron bupropión o combinaciones no tuvieron mayores probabilidades de reportar abstinencia.
Conclusiones y recomendacionesLa evidencia disponible nos indica que una intervención intensiva para ayudar a dejar de fumar iniciada mientras el paciente está ingresado y que incluya, al menos, un mes de seguimiento tras el alta hospitalaria consigue mayores tasas de abstinencia al compararlo con fumadores a los que se les realizó el tratamiento habitual. La eficacia se incrementa significativamente cuando al asesoramiento psicológico se añade tratamiento con TSN o vareniclina. Esta intervención resulta altamente coste-efectiva.
Evidencia alta y recomendación fuerte para realizar intervenciones para ayudar a dejar de fumar a pacientes con EPOC iniciadas mientras se encuentran hospitalizados.
Grado de recomendación: 1A.
Pregunta PICOFinanciar el tratamiento del tabaquismo en los fumadores con EPOC ¿tendrá impacto sobre la economía de la salud?
JustificaciónLa EPOC es responsable de un elevado gasto sanitario para los sistemas públicos de salud. En España supone un coste de 3.000 millones de euros anuales. También se conoce que el coste sanitario en el que incurre un fumador con EPOC es aproximadamente 3.700euros/año, y en el que incurre un sujeto con EPOC que ha dejado de fumar es 2.000euros/año. Luego se puede calcular que cuando un paciente con EPOC que fuma deja de hacerlo, ello ocasiona un ahorro para el Sistema Nacional de Salud de alrededor 1.300euros/año35.
Selección de búsquedaSe recogieron 22 referencias (MeSH: 17; Tripdatabase: 5), seleccionando 4 estudios para responder la pregunta (3 estudios de cohorte y uno de casos y control).
Resumen de la evidenciaEn un estudio de casos y controles realizado en España, en el que se estudió comparativamente el gasto ocasionado por el paciente EPOC fumador frente al EPOC ex fumador en un período de 12meses, se comprobó que los fumadores EPOC tuvieron un mayor consumo de recursos sanitarios frente a los exfumadores e independientemente del estadio de severidad de su EPOC35.
Tres estudios de cohortes simulados en el Reino Unido, España y Francia han analizado el escenario de la financiación del tratamiento del tabaquismo en pacientes con EPOC utilizando un modelo de Markov: 1)En el caso de los pacientes con EPOC en el Reino Unido36, el ICER (razón de coste incremental) correspondiente fue de 22.686£ por AVAC con datos de rentabilidad a 10años en cualquier paciente, independientemente de la severidad de su EPOC y porcentaje de éxito de la intervención aplicada. 2)En España37 y para un horizonte temporal de 5años y utilizando los tres fármacos de primera línea aprobados (vareniclina, bupropión y TSN) el modelo estima que 17.756 pacientes con EPOC podrían dejar de fumar si se dispusiera de financiación del tratamiento, en comparación con 1.303 pacientes, sin reembolso38. En el escenario de reembolso, el ahorro acumulado sería de 4,3 millones de euros. 3)En Francia, utilizando un estudio de coste-efectividad en pacientes con EPOC, cáncer y enfermedad cardiovascular, los autores concluyen que para un horizonte de 5años habría un ahorro de costes que podría variar de 15 a 215 millones de euros con un ICER de 11.187€ por AVAC.
Conclusiones y recomendacionesLos estudios que analizan el impacto de la financiación del tratamiento del tabaquismo en pacientes con EPOC indican las siguientes conclusiones: a)los pacientes EPOC que continúan fumando utilizan más recursos sanitarios y tienen un mayor coste social y económico, y b)la financiación del tratamiento del tabaquismo en fumadores con EPOC es una medida altamente eficaz y coste-efectiva.
Evidencia moderada y recomendación fuerte para la financiación del tratamiento del tabaquismo en fumadores con EPOC por su impacto sobre la salud y economía de la salud.
Grado de recomendación: 1B.
Conflicto de interesesEl Dr. Carlos A. Jiménez Ruiz ha colaborado con GSK y Pfizer industrias farmacéuticas con interés en el campo del tratamiento del tabaquismo.
El Dr. Daniel Buljubasich no tiene conflicto de intereses.
El Dr. Juan A. Riesco Miranda ha colaborado con GSK, Pfizer, Novartis, Boehringer Ingelheim y Astra-Zeneca en actividades de formación e investigación clínica.
El Dr. Agustín Acuña Izcaray ha recibido honorarios por impartir conferencias y/o asesoría científica de Astra-Zeneca, Novartis y Pfizer.
El Dr. Jose Ignacio de Granda Orive no tiene conflicto de intereses.
El Dr. José Miguel Chatkin no tiene conflicto de intereses.
El Dr. Gustavo Zabert declara haber recibido honorarios para realizar acciones educativas con Global Bridges e Interamerican Heart Foundation y como ponente de Astra-Zeneca, Novartis, Boehringer Ingelheim y Pfizer.
El Dr. Alfredo Guerreros Benavides no tiene conflicto de intereses.
El Dr. Nelson Paez Espinel no tiene conflicto de intereses.
La Lda. Valeri Noe no tiene conflicto de intereses.
El Dr. Efraín Sánchez-Angarita ha recibido honorarios por charlas en congresos y actividades educativas relacionadas con tratamiento de la EPOC por Novartis, Boehringer Ingelheim, Takeda y Pfizer.
La Dra. Ingrid Núñez-Sánchez no tiene conflicto de intereses.
El Dr. Raúl H. Sansores no tiene conflicto de intereses.
El Dr. Alejandro Casas no tiene conflicto de intereses.
El Dr. Andrés Palomar Lever ha recibo honorarios por impartir conferencias para Novartis y Actelion.
La Dra. Inmaculada Alfageme Michavila no tiene conflicto de intereses.
Agradecemos a la Dra. Ángela Ramos Pinedo (Hospital Fundación Alcorcón, Madrid, España) y a la Dra. Susana Luhning (Profesora del Departamento de Medicina Interna/Neumología, Facultad de Medicina, Universidad de Córdoba, Argentina), quienes fueron las revisoras externas de este documento.