Músculo esquelético y fibra muscular
El movimiento es esencial para la vida del ser humano y la de los animales. Ejemplos de movimiento nos los ofrecen actividades como caminar, hablar, mirar o respirar. Todos ellos implican siempre la existencia de contracciones musculares diversas que a su vez originan diferentes tamaños y formas de músculos. Las diferencias existentes entre los músculos respiratorios y los músculos esqueléticos de las extremidades están directamente relacionadas con la función que deben ejercer. En este sentido, los músculos ventilatorios están diseñados para vencer cargas resistivas y elásticas, que están sujetas tanto a un control voluntario como involuntario. Además, la longitud de reposo de los músculos respiratorios se establece por el equilibrio existente entre las fuerzas de retracción elástica pulmonar y las de expansión de la caja torácica1,2. Cabe añadir que su función es esencial para la vida ya que han de contraerse rítmicamente y generar las presiones necesarias para la ventilación durante toda la existencia del individuo3. Por último, y basado en sus acciones mecánicas, los músculos ventilatorios se clasifican en general en inspiratorios y espiratorios. Estas acciones pueden realizarlas varios grupos de músculos con el fin de asegurar los medios por los cuales el aire puede ser movido eficazmente en cualquier situación fisiológica o fisiopatológica4. Por otro lado, los músculos de las extremidades son los que nos permiten tener una vida de relación, mediante la deambulación.
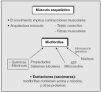
Todos los músculos esqueléticos están compuestos por fibras, cuya característica principal es la presencia de estriaciones claras y oscuras alternadas (fig. 1). Las fibras musculares son células multinucleadas, cuyos núcleos se encuentran en condiciones normales dispersos a lo largo de la superficie interior del plasmalema. Aparte de los núcleos y otros organelos, las mitocondrias representan las estructuras principales del citoplasma de las fibras. Estos organelos son los encargados de sintetizar el adenosintrifosfato (ATP) (fig. 1) procedente tanto de los gránulos de glucógeno como de las gotitas lipídicas, que a su vez están también presentes en el citoplasma de la fibra muscular5.
Fig. 1. Representación esquemática de la composición y estructura del músculo. ATP: adenosintrifosfato.
Los diferentes tipos de miosinas determinan la diversidad fenotípica fibrilar de los músculos, especialmente el componente de las isoformas de las cadenas pesadas de miosina (MHC). Según predomine un tipo u otro de isoforma de MHC, las fibras "puras" se clasifican en fibras lentas tipo I compuestas por la isoforma MHCIß por un lado, y por otro en fibras rápidas de tipo IIA, IIB, IID y IIX, compuestas por MHCIIa, MHCIIb, MHCIId y MHCIIx, respectivamente (la MHCIId y las fibras IID se consideran equivalentes a la MHCIIx y a las fibras IIX, respectivamente). La coexpresión de parejas de estos tipos de isoformas de MHC constituye las fibras híbridas. Los programas específicos de expresión genética que definen los distintos tipos de fibras no sólo se limitan a regular las isoformas de MHC, sino que también pueden modular la expresión de otras proteínas como la tropomiosina, las tres subunidades de troponina, alfa-actinina y otras proteínas musculares dependientes del calcio. Esa regulación no sólo es cualitativa, sino que diversas proteínas del músculo pueden encontrarse en mayor o menor medida en unos tipos de fibras, o incluso estar sólo presente en otras. Además, las fibras musculares son estructuras dinámicas con capacidad para modificar su fenotipo en respuesta a cambios en la actividad neuromuscular, modificaciones de la carga mecánica, alteraciones hormonales (tiroideas) y la edad. Los cambios producidos en las isoformas de las MHC siguen un esquema de transiciones secuenciales y reversibles que va desde isoformas rápidas hasta isoformas lentas y viceversa.
Músculos respiratorios en condiciones de normalidad
La respiración es un fenómeno bifásico, en que se distingue una parte activa, la inspiración, y otra gene-ralmente pasiva, o espiración. Esto implica que suele considerarse como más importante la función de los músculos inspiratorios, pues su contracción es imprescindible para conseguir la entrada de aire en los pulmones. Entre los músculos inspiratorios, el más importante es el diafragma6. Éste tiene forma de cúpula y está situado entre la caja torácica y la cavidad abdominal. En circunstancias normales, el diafragma es el músculo que desempeña el papel más relevante en generar el flujo de aire inspiratorio. Se halla dividido en dos porciones, cuyos orígenes y funciones son tan diferenciados que se ha llegado a proponer que se consideren como músculos distintos. Por un lado, el diafragma costal (anterior y lateral), que actúa como un émbolo y es el responsable directo de generar el gradiente de presión respiratoria. Por otro, el diafragma crural (localización posterior), que fundamentalmente fija las diferentes estructuras para permitir la óptima función de los demás músculos respiratorios7. Sin embargo, existen otros músculos que actúan auxiliando al diafragma en la función inspiratoria, los intercostales externos y un grupo especial de intercostales internos, denominado paraesternales8. Además hay toda una serie de músculos inspiratorios secundarios, como los escalenos, dorsal ancho y esternocleidomastoideo, que auxilian a los antes mencionados. Cuando el esfuerzo inspiratorio es mayor (enfermedades pulmonares, ejercicio, respiración bajo cargas), los músculos auxiliares desempeñan un papel progresivamente mayor.
Cuando los músculos inspiratorios se contraen, tienden a aumentar el volumen de la caja torácica. Dado que la presión de retracción elástica pulmonar actúa en dirección contraria, se genera un gradiente de presión negativa en el espacio pleural. Esta presión se transmite al espacio alveolar, donde llega algo atenuada (es decir, menos negativa) debido a la resistencia del propio parénquima pulmonar a la transmisión de la presión (la diferencia se conoce como presión transpulmonar)9. Sin embargo, aun es lo suficientemente negativa como para que exista un claro gradiente con la atmósfera (o "nivel cero"), por lo que se produce la entrada de aire en los pulmones. Naturalmente, ese flujo de aire deberá superar todavía una serie de resistencias en las vías aéreas y en el propio parénquima pulmonar.
Poco después, los músculos inspiratorios se relajan y se inicia pasivamente la espiración. En realidad, a pesar de la relajación, sigue existiendo una presión ligeramente negativa en el espacio pleural, ya que continúa presente la retracción elástica del pulmón. Sin embargo, esa negatividad es tan pequeña que, al disminuir aún más debido al parénquima pulmonar interpuesto (la antes mencionada presión transpulmonar), ya no llega al alvéolo. Allí, la presión es ahora algo más positiva que en la atmósfera, y se produce la salida del aire9.
Sin embargo, existen circunstancias en que es necesario facilitar la salida de aire (esfuerzo, enfermedad pulmonar, tos). En ese momento, el organismo puede recurrir a la contracción de los llamados músculos espiratorios. Fundamentalmente, los de la llamada prensa abdominal (oblicuo externo, oblicuo interno, transverso y recto del abdomen) y los intercostales internos, con excepción de los paraesternales.
Músculos no respiratorios en condiciones de normalidad
Nos referiremos fundamentalmente aquí a los llamados músculos periféricos o de las extremidades. Se trata de un grupo muscular con importantes implicaciones en las enfermedades respiratorias. Los músculos de las extremidades inferiores permiten, como hemos visto, la deambulación. Es decir, son fundamentales para la vida de relación del individuo pues facilitan su desplazamiento, tanto en circunstancias normales (marcha) como en situaciones más extremas (p. ej., el ejercicio). Los músculos de las extremidades superiores, a su vez, condicionan los movimientos de éstas, y por tanto actividades tan diversas e imprescindibles como la alimentación, los autocuidados o el manejo de instrumentos. Es fácil entender pues que el mal funcionamiento de los músculos periféricos tenga un impacto muy relevante en la calidad de vida del individuo.
Disfunción de los músculos respiratorios en la EPOC
Inspiratorios
Estudios sobre la fuerza y resistencia del diafragma. La fuerza del diafragma está disminuida en los pacientes con una EPOC si se compara con la de individuos sanos10,11. La hiperinsuflación pulmonar hace que el diafragma se aplane, alejándose de su longitud óptima12 (fig. 2). Este concepto ha sido ampliamente difundido y aceptado, pero también se ha postulado que la disfunción diafragmática puede tener una base estructural en el propio músculo. En esta línea, diversos estudios han puesto de manifiesto un menor tamaño de las fibras del diafragma en los pacientes con EPOC13,14. Este hecho nos lleva a pensar que el contenido del diafragma en proteínas contráctiles (miosina y actina) sea probablemente también menor, y puede explicar en parte su disminución para generar fuerza.
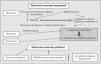
Fig. 2. Representación esquemática de las características más importantes y de los factores implicados en la disfunción muscular respiratoria y la periférica en los pacientes con enfermedad pulmonar obstructiva crónica.
Por otro lado, Similowski et al12 demostraron que la fuerza del diafragma estaba preservada, o podía ser incluso mayor a la de individuos sanos si se comparaban ambos grupos a volúmenes pulmonares equivalentes. En este sentido, un estudio de nuestro grupo puso de manifiesto la existencia de cambios adaptativos estructurales, a nivel de la sarcómera, en el diafragma de pacientes con una EPOC moderada15. Además, se ha demostrado que la capacidad aeróbica del músculo estaba incrementada con un mayor contenido en mitocondrias16,17 y capilares18,19. En cuanto a la composición fibrilar del diafragma de los pacientes con EPOC grave, Levine et al20 demostraron que este músculo tenía un mayor porcentaje de fibras tipo I (aeróbicas, lentas y resistentes a la fatiga) que el de los sujetos control. Datos de nuestro grupo corroboraron también este hallazgo21. Levine et al22 también sugirieron en otro estudio la existencia de una disfunción intrínseca de las fibras del diafragma en los pacientes con una EPOC grave. En este sentido, un trabajo reciente de nuestro grupo21 también puso de manifiesto un aumento significativo de los niveles de estrés oxidativo (proteínas oxidadas) en el diafragma de pacientes con EPOC grave, que a su vez correlacionó negativamente con la función de los músculos respiratorios y con la del diafragma. En ese estudio, concluimos que el desarrollo de estrés oxidativo (aumento de los niveles de oxidantes superior a los neutralizados por los antioxidantes musculares) podría ser uno de los factores implicados en la disfunción intrínseca del diafragma de los pacientes con una EPOC grave. En resumen, todavía desconocemos si los cambios adaptativos del diafragma son suficientes para aumentar la eficiencia de este músculo, y poder vencer así las cargas a las que se ve sometido en la EPOC grave. Tampoco conocemos con exactitud si la disfunción de los músculos respiratorios obedece exclusivamente a la incorrecta configuración de la geometría de la caja torácica en la EPOC grave o si, por el contrario, la disfunción muscular intrínseca del diafragma sería el factor predominante.
Estudios de los músculos intercostales externos. Estos músculos constituyen uno de los principales grupos musculares inspiratorios23.. Sin embargo, a diferencia del diafragma, no es posible evaluar específicamente su fuerza o resistencia de forma aislada. Estudios de nuestro grupo han mostrado que las fibras de los músculos intercostales externos tienen un diámetro similar en los pacientes con EPOC y en los individuos sanos24. Sin embargo, existen cambios moleculares muy relevantes en la expresión de las proteínas contráctiles. Así se ha podido demostrar que la expresión de la MHC tipo II está aumentada en la EPOC, correlacionada directamente con la gravedad de la enfermedad25. Esto sugiere que la modalidad y frecuencia de activación de este grupo de músculos son diferentes de las del diafragma. Una posible explicación para ello sería el reclutamiento intermitente y de alta intensidad de estos músculos, asociado a la tos o a incrementos ventilatorios durante el ejercicio25.
Espiratorios
Convencionalmente, la fuerza de los músculos espiratorios se ha evaluado mediante la medición de la presión espiratoria máxima en boca (PEM). Miembros de nuestro grupo describieron un nuevo método específico para evaluar la resistencia de los músculos espiratorios, con aceptable reproducibilidad y tolerancia26. En otro estudio pudimos demostrar que los pacientes con EPOC presentan una verdadera disfunción de los músculos espiratorios, expresada como menor fuerza, y sobre todo como menor resistencia27. A su vez, la resistencia disminuida de los músculos espiratorios en estos pacientes se correlacionó con la gravedad de su enfermedad, medida por el grado de obstrucción de la vía aérea27. De hecho, diversos estudios han mostrado que los músculos espiratorios son activos en los pacientes con EPOC, tanto en reposo como en ejercicio28,29. Además se sabe que estos músculos son también reclutados en situación de sobrecarga ventilatoria y broncospasmo30,31, y son esenciales para la tos y la limpieza de la vía aérea. Sin embargo, estas acciones no parecen resultar en un efecto entrenamiento en los pacientes con EPOC, tal y como sucede en los músculos inspiratorios.
Desde el punto de vista estructural, datos procedentes de nuestro grupo muestran que las fibras del músculo oblicuo externo (uno de los principales músculos espiratorios) tienen tamaños similares a los observados en los músculos de los sujeto control32.
Afectación muscular periférica en la EPOC
Son numerosos los estudios que han puesto de manifiesto cambios importantes, tanto funcionales, estructurales y moleculares, en los músculos periféricos de los pacientes con EPOC. La mayoría de estos estudios se ha centrado exclusivamente en los músculos de las piernas, ya que este grupo muscular parece ser el más determinante en la limitación funcional ante el esfuerzo de estos pacientes (fig. 2).
Cuádriceps. Los cuádriceps de pacientes con EPOC muestran una menor masa muscular33,34, un mayor número de capilares35, contenido mitocondrial normal35, una menor concentración de mioglobina35,36, una atrofia de fibras tipo I y II35,36, una disminución del porcentaje de fibras tipo I37-39, y un incremento de isoformas de miosina tipo IIb39. Desde el punto de vista de su capacidad metabólica, la concentración de las enzimas aeróbicas (citrato-sintetasa, succinil-deshidrogenasa, hidroxiacetil CoA) disminuye, mientras que la mayoría de las enzimas anaeróbicas (especialmente LDH y HK) no se modifica38,40. La fosfofructocinasa, sin embargo, parece incrementarse moderadamente41. También se ha demostrado que la concentración de la enzima citocromo-oxidasa, el último eslabón de la fosforilación oxidativa, está aumentada en estos pacientes, al parecer como un fenómeno compensatorio ante una probable hipoxia celular crónica o recurrente42.
Bíceps. Son pocos los estudios estructurales que se han realizado en este músculo en la EPOC. Parece ser que el porcentaje de fibras no se modifica43, y hay una atrofia de éstas (tipos I y II), que a su vez se asoció con la pérdida de peso y con el grado de obstrucción de los pacientes43.
Deltoides. Estudios de nuestro grupo han demostrado que las fibras del deltoides de pacientes con EPOC tienen tamaños y proporciones similares a las de los sujetos control, que enzimas de la vía glucolítica y oxidativa estaban preservadas y que el contenido en proteínas contráctiles fue también similar44.
Etiología de la disfunción muscular en la EPOC
La disfunción muscular periférica es una de las manifestaciones sistémicas más importantes de los pacientes con EPOC, por el deterioro en la capacidad de ejercicio y las consecuentes implicaciones en su calidad de vida. Se trata de una entidad multifactorial; de esos factores, la inflamación y el estrés oxidativo han sido objeto de numerosos estudios en la última década (fig. 3).
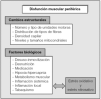
Fig. 3. Representación esquemática de los factores implicados en la etiología de la disfunción muscular de los pacientes con enfermedad pulmonar obstructiva crónica, así como de las alteraciones estructurales más frecuentes.
Hipoxia crónica. Deteriora la función muscular mediante la disminución de los depósitos intracelulares de energía (p. ej., glucógeno y glucosa) y de la glucosa-6-fosfato-deshidrogenasa, por lo que aumenta los niveles de hexocinasa y puede afectar a la síntesis intramitocondrial de otras proteínas45. Por otro lado, los niveles de estrés oxidativo estaban más aumentados en los cuádriceps de pacientes con EPOC e hipoxemia respecto de un grupo de pacientes de idéntica gravedad y sin hipoxemia46.
Hipercapnia crónica. La hipercapnia aguda o crónica es frecuente en los pacientes con EPOC e insuficiencia respiratoria aguda o crónica. Los estudios en humanos han puesto de manifiesto la existencia de una alteración metabólica celular en situación de fracaso ventilatorio agudo, en forma de un descenso en el contenido de ATP y fosfocreatina47. Parece ser que estos cambios metabólicos son temporales y reversibles tras una intervención terapéutica47.
Inflamación y estrés oxidativo. La inflamación local o sistémica es común en los pacientes con EPOC. Estos mediadores incrementan el estrés oxidativo. El músculo estriado posee numerosas vías metabólicas normales por las cuales se producen radicales oxigenados y óxido nítrico que, por otra parte, son esenciales para una óptima función contráctil48,49. Es por ello que existen unos sistemas antioxidantes constitutivos representados por el glutatión reducido y enzimas como las superóxido dismutasas y la catalasa. Si la homeostasis de este sistema redox se altera por los mediadores inflamatorios, se produce un desequilibrio entre oxidantes y antioxidantes que se conoce como estrés oxidativo. Trabajos de nuestro grupo50,51 han demostrado que el músculo cuádriceps de pacientes con EPOC de diversos grados de gravedad tienen niveles aumentados de estrés oxidativo y nitrosativo, así como de la enzima Mn-superóxido dismutasa respecto de una población control50. A su vez, las proteínas que estaban más intensamente oxidadas en los músculos de los pacientes con EPOC resultaron ser la actina muscular, la anhidrasa carbónica y la creatincinasa, cuya actividad se correlacionó inversamente con su nivel de oxidación51. En otro estudio52, se demostró que los niveles de estrés oxidativo, y no los de estrés nitrosativo, estaban aumentados en los diafragmas de pacientes con EPOC grave respecto del grupo control. Además, aquéllos se correlacionaron con la gravedad de la función pulmonar y con la disfunción muscular respiratoria52.
Desnutrición y pérdida de masa muscular. La desnutrición prolongada se asocia a un descenso proporcional en la masa muscular de los pacientes que la sufren. A su vez las repercusiones (atrofia) en las fibras tipo II son de mayor magnitud que en las de tipo I. De esta manera, la masa muscular restante estará compuesta fundamentalmente por fibras resistentes a la fatiga (tipo I)53. También se sabe que la desnutrición y el bajo peso en los pacientes con EPOC se relacionan con una menor supervivencia. Recientemente, se ha podido demostrar que el contenido de masa magra, y no sólo el peso corporal, es un factor independiente de predicción de mortalidad en la EPOC54. Estos resultados sugieren que la composición corporal debería incluirse siempre en la evaluación sistemática de este tipo de pacientes.
Comorbilidad. Entre ellas están las alteraciones electrolíticas crónicas, el fallo cardíaco crónico, la diabetes o la hipertensión arterial. Otras condiciones asociadas, como la edad avanzada y el desacondicionamiento por sedentarismo e inactividad física, también se han postulado como posibles factores contribuyentes.
Corticoides. En los pacientes con EPOC, se ha puesto de manifiesto la existencia de asociaciones directas entre la dosis y la duración de la corticoterapia y el grado de debilidad de las piernas55, y entre el incremento de las concentraciones séricas de LDH38 y la atrofia o necrosis de las fibras del cuádriceps en los pacientes con EPOC56. Por otro lado, se ha reportado que la supervivencia es menor en los pacientes con EPOC y miopatía esteroidea que en los pacientes que no la padecen56.
Implicaciones funcionales de la disfunción muscular en la tolerancia al ejercicio
La disnea, una capacidad de esfuerzo disminuida y una menor calidad de vida son manifestaciones comunes de los pacientes con EPOC. Diversos estudios han puesto de manifiesto que esas manifestaciones no son sólo la consecuencia del deterioro en la función pulmonar que estos pacientes sufren. En este sentido, la medicación consigue mejorar significativamente la función pulmonar, pero no queda claro su papel en la capacidad de esfuerzo de los pacientes. Siguiendo esta línea de razonamiento, el trasplante pulmonar, que tiene claros efectos en la función pulmonar, tan sólo logra mejorar la tolerancia al ejercicio de forma parcial57. Además, no se encontraron diferencias significativas en cuanto a la capacidad de esfuerzo postrasplante de los pacientes, entre los sometidos a trasplante único y doble57.
La relevancia clínica de la disfunción muscular periférica en la disminución de la capacidad de ejercicio de los pacientes con EPOC fue descrita por primera vez por Killian et al58. En su estudio se reportó que la fatiga de las piernas limitó la tolerancia al ejercicio, tanto de los sujetos control como de los pacientes con EPOC58. Las relaciones entre la disfunción muscular periférica y la capacidad de esfuerzo de los pacientes con EPOC se describen a continuación.
Fuerza de los músculos periféricos en la EPOC. Diversos estudios han demostrado consistentemente que la fuerza de las piernas está disminuida en los pacientes con EPOC59-61. La disfunción muscular periférica se asocia directamente a la distancia recorrida en la prueba de marcha de 6 min, con la gravedad de los síntomas durante una prueba de esfuerzo incremental60 y con la capacidad máxima de consumo de oxígeno59,61. En este sentido, existen estudios intervencionistas que demuestran que el entrenamiento de tipo fuerza de las piernas de pacientes con EPOC se asocia a una mejoría, tanto de su capacidad de ejercicio62 como de su calidad de vida63. Por otro lado, se ha mostrado la existencia de una relación entre una menor distancia de la prueba de marcha y un menor contenido de masa magra en pacientes con EPOC y bajo peso64.
Resistencia de los músculos periféricos en la EPOC. Los hallazgos procedentes de la literatura médica al respecto de la resistencia de los músculos de las extremidades inferiores en estos pacientes son, en algunos casos, contradictorios. Por un lado, ese parámetro resultó ser normal en pacientes con EPOC e hipoxemia65, mientras que estaba disminuido en otros estudios66,67; además mostraron una asociación directa con el desarrollo temprano de fatiga, independientemente de la gravedad de la EPOC67. Desde un punto de vista molecular, en diversos estudios se ha evaluado la resistencia de los músculos periféricos como la expresión de cambios moleculares subyacentes en la cadena respiratoria mitocondrial o a través de productos derivados del metabolismo muscular durante el ejercicio. En este sentido, diversos estudios han demostrado que durante el ejercicio los pacientes con EPOC desarrollan precozmente un metabolismo muscular anaeróbico, hecho que a su vez contribuye a la limitación funcional ante un esfuerzo incremental41,68.
Las alteraciones en el metabolismo oxidativo muscular de pacientes con EPOC guardan una relación directa con el consumo de oxígeno. En este sentido, Maltais et al40 demostraron la existencia de una asociación entre la concentración de enzimas aeróbicas en los músculos de las piernas y la capacidad de consumo de oxígeno de sus pacientes. Otro aspecto a tener en cuenta en la resistencia del cuádriceps de pacientes con EPOC es su composición fibrilar. Diversos estudios muestran que los cuádriceps de pacientes con EPOC grave presentan una disminución de las fibras tipo I con un incremento proporcional de las de tipo II, fundamentalmente las IIb38,39. También se ha valorado el impacto de la resistencia muscular periférica en la limitación al ejercicio físico mediante el estudio de los cambios metabólicos tras el entrenamiento. Así, el entrenamiento muscular indujo un aumento de la actividad de las enzimas oxidativas en el cuádriceps de pacientes con EPOC, mejorando a su vez su capacidad de ejercicio69. En otros estudios se puso de manifiesto que la mejoría de la capacidad aeróbica en los pacientes se asoció a concentraciones más bajas de lactato y menores requerimientos ventilatorios, para una misma intensidad de ejercicio68-70. En este sentido, Clark et al71 demostraron que tanto la resistencia de las piernas como la capacidad de esfuerzo de pacientes con EPOC mejoraron tras un entrenamiento de baja intensidad. Estos resultados ponen de manifiesto que la función muscular del cuádriceps, sus modificaciones estructurales y/o moleculares, así como la capacidad de esfuerzo de los pacientes con EPOC, guardan una estrecha relación.
Disfunción de los músculos de las extremidades superiores frente a inferiores. Los músculos de las extremidades superiores están claramente implicados en actividades de la vida diaria, que están a menudo limitadas en los pacientes con EPOC. Ello obedece a diversas causas. En primer lugar, los músculos de las extremidades superiores participan en la ventilación, y el ejercicio de brazos se asocia a asincronía respiratoria en los pacientes con EPOC72. En segundo lugar, se ha demostrado que ciertas posiciones de los brazos permiten incrementar la ventilación53. En tercer lugar, para idénticas intensidades de trabajo, se ha demostrado que tanto la ventilación como el consumo de oxígeno son superiores en los brazos que en las piernas, probablemente debido a la aparición temprana de metabolismo anaeróbico en los brazos que en las extremidades inferiores53. Por último, existen diferencias en el grado de disfunción de los músculos de las extremidades inferiores y superiores. En este sentido, la fuerza del cuádriceps es menor que la de la mano, sugiriendo que las actividades derivadas del movimiento de las extremidades inferiores se verían mayormente afectadas que las de los miembros superiores53.
Entrenamiento en la EPOC
Los programas de rehabilitación pulmonar en la EPOC grave persiguen como objetivos fundamentales la mejoría de la capacidad de esfuerzo para las actividades cotidianas de los pacientes, así como una mejoría de su calidad de vida y supervivencia (fig. 4). Los programas de rehabilitación pulmonar son, en general, de carácter multidisciplinario y flexibles, con el fin de poder adaptarse a las necesidades particulares de cada paciente. Dado que la intolerancia al ejercicio es uno de los problemas de mayor relevancia de los pacientes con EPOC, en un programa de rehabilitación pulmonar el entrenamiento general para el ejercicio aparece como uno de los componentes esenciales.
Fig. 4. Representación esquemática de los beneficios de la rehabilitación pulmonar y entrenamiento en los pacientes con enfermedad pulmonar obstructiva crónica.
Diversos estudios aleatorizados y controlados han demostrado mejorías en la capacidad máxima de esfuerzo, resistencia y distancia recorrida en la prueba de marcha, así como una reducción de la mortalidad en pacientes con EPOC tras un programa de rehabilitación pulmonar73. Si bien todos estos programas eran de naturaleza multidisciplinaria, todos los autores concluyeron que el entrenamiento general constituía una parte esencial de la rehabilitación pulmonar, sobre todo en lo que a la mejoría de la capacidad de esfuerzo de los pacientes se refiere.
La eficacia del entrenamiento general está basada en los principios básicos de la fisiología del ejercicio. En los sujetos sanos, el establecimiento de la intensidad del entrenamiento se basa en la frecuencia cardíaca máxima (60-90% de la frecuencia cardíaca máxima predicha) o en el consumo máximo de oxígeno (50-80% del predicho) alcanzados durante el entrenamiento. La intensidad debería mantenerse durante 20-45 min, en períodos de 3-5 veces/semana. En estas condiciones, en individuos sanos, la capacidad de esfuerzo máxima aumenta, los músculos periféricos se adaptan y la función cardíaca mejora. En el caso de los pacientes con EPOC, esto no es necesariamente así. Por ejemplo, diversos estudios han apuntado que estos pacientes desarrollan acidosis láctica precozmente en respuesta al ejercicio68, y que las mejorías en la capacidad máxima de ejercicio sólo se alcanzan tras entrenamientos de alta intensidad (70% de la carga máxima), por encima del umbral anaeróbico, comparado con entrenamientos de baja intensidad (30% de la carga máxima). Actualmente se acepta que un entrenamiento general de alta intensidad es necesario para conseguir mejorar la función muscular y el transporte de oxígeno, reducir las concentraciones de lactato y aumentar la capacidad oxidativa mitocondrial en los pacientes con una EPOC moderada y grave73. La mayor parte de los programas de rehabilitación incluye entrenamientos de tipo resistencia, con períodos de cargas sostenidas durante 20-30 min. Sin embargo, en algunos pacientes muy graves con hipoxemia e hipercapnia, el entrenamiento de tipo resistencia de alta intensidad suele ser mal tolerado, por lo que el entrenamiento de tipo intervalo, donde alternan períodos de entrenamiento de alta intensidad con períodos equivalentes sin carga, aparece como una alternativa interesante para estos enfermos.
Tipos de entrenamiento
La especificidad del entrenamiento se basa en el hecho de que el beneficio depende de las actividades entrenadas. Si bien difícil en la práctica clínica, ello implica que la carga administrada durante el entrenamiento debería tener como objetivo primario la mejoría de las actividades de la vida diaria de los pacientes con EPOC.
Entrenamiento de las extremidades superiores. En los pacientes con EPOC, los músculos de la cintura escapular y el dorsal ancho actúan como músculos accesorios de los respiratorios. Cuando participan en las actividades de la vida cotidiana, su contribución en la ventilación es menor y, por tanto, el diafragma ha de trabajar más. Estudios sobre el entrenamiento de los brazos han mostrado efectos beneficiosos en ejercicios de resistencia específicos de éstos, así como una disminución de los requerimientos metabólicos durante sus actividades53. A pesar de la falta de estudios concluyentes al respecto de si el entrenamiento de brazos mejora el estado funcional de los pacientes, en general se recomienda su inclusión en los programas de rehabilitación de los pacientes con EPOC53.
Entrenamiento de las extremidades inferiores. Como ya se ha mencionado anteriormente, la disfunción muscular periférica es uno de los factores más implicados en la disminución de la capacidad de ejercicio de los pacientes con EPOC. Las estrategias más comúnmente utilizadas en el entrenamiento de las piernas en los pacientes con EPOC son ejercicios como caminar, andar sobre cinta rodante y pedaleo en bicicleta distribuidos en 3-5 sesiones/semana durante períodos de 6-12 semanas53. Diversos estudios han puesto de manifiesto la adaptación de los músculos de las piernas en forma de un aumento de su capacidad aeróbica tras un programa de entrenamiento de resistencia. Por ejemplo, se ha demostrado una menor producción de ácido láctico y de CO2 en respuesta al ejercicio53. En otros estudios se ha demostrado tras entrenamiento de resistencia de alta intensidad de 6-15 semanas de duración53, un aumento en la proporción de fibras tipo I con una reducción recíproca de las de tipo IIb, al igual que el paso de un fenotipo rápido a lento de las proteínas contráctiles musculares. Otros trabajos también han puesto de manifiesto el incremento del tamaño de las fibras tipo I y del número de mitocondrias, así como un aumento de la actividad de diversas enzimas mitocondriales53 tras este tipo de entrenamiento. Por otro lado, también se ha visto la existencia de un aumento de los valores de mioglobina y de capilares, facilitando así el aporte y extracción de oxígeno en el músculo53. Todos estos cambios se acompañan de un menor aumento en la concentración de ácido láctico en sangre y en el músculo para un mismo grado de ejercicio intenso, reflejando, por tanto, un incremento en la capacidad oxidativa de los músculos entrenados53. Se sabe además que la adaptación muscular inducida por un entrenamiento de resistencia se caracteriza por un incremento de la masa y fuerza musculares, de las fibras tipo IIa, y por un descenso de las fibras de tipo IIb, y finalmente por una hipertrofia de ambos tipos de fibras53. En resumen, los cambios a nivel funcional, molecular y estructural tendrán lugar en el músculo entrenado en la medida en que el estímulo sobre ese músculo sea aplicado adecuadamente en términos de frecuencia, intensidad y duración.
Entrenamiento de los músculos respiratorios. La función de los músculos respiratorios, sobre todo la de los inspiratorios, está comprometida en los pacientes con EPOC, lo que contribuye a la aparición de disnea, a su limitación al ejercicio y al desarrollo de hipercapnia. En este tipo de entrenamientos, la función de los músculos inspiratorios mejora en la medida en que la intensidad del entrenamiento sea mantenida y supere el 30% de la presión inspiratoria máxima. En diversos estudios, se ha podido demostrar que el entrenamiento de los músculos inspiratorios añadido a un entrenamiento general resultó en una mejoría de la capacidad de esfuerzo en pacientes con una limitación ventilatoria al ejercicio74,75. En un estudio de nuestro grupo, se pudo demostrar también un aumento en la fuerza y resistencia de los músculos respiratorios en pacientes con EPOC grave sometidos a un entrenamiento inspiratorio de tipo umbral de 5 semanas de duración, y cargas superiores al 40% de la presión inspiratoria máxima76. A su vez, esa mejoría funcional se asoció a un aumento en la proporción de las fibras tipo I y en el tamaño de las de tipo II del músculo intercostal externo76, sin mostrar cambios en el músculos control (cuádriceps) no entrenado. En otro trabajo muy reciente de nuestro grupo77, también se ha podido poner de manifiesto una mejoría en la capacidad de ejercicio, la sintomatología clínica y la calidad de vida de pacientes con EPOC grave sometidos a un programa de entrenamiento específico de los músculos espiratorios de tipo umbral de 5 semanas de duración, y cargas del 50% de la presión espiratoria máxima de los pacientes. Estudios futuros permitirán conocer las modificaciones estructurales de los músculos espiratorios sometidos a un programa de entrenamiento específico.
Conclusiones
A pesar de los esfuerzos realizados en la última década, que nos han permitido avanzar en el conocimiento de la etiología y el diagnóstico de la disfunción muscular de los pacientes con EPOC, todavía son muchos los interrogantes que quedan por resolver. La respuesta a éstos debería ir encaminada hacia un mejor manejo clínico, diagnóstico y terapéutico de estos pacientes. Cabe esperar que estudios en curso y otros que se pondrán en marcha en un futuro inmediato puedan arrojar más luz sobre los mecanismos fisiopatológicos de la disfunción muscular en la EPOC.
Correspondencia: Dra. E. Barreiro Portela.
Unidad de Investigación en Músculo y Aparato Respiratorio, IMIM, PRBB.
Doctor Aiguader, 88. 08003 Barcelona. España.
Correo electrónico: ebarreiro@imim.es