El objetivo fundamental del aparato cardiorrespiratorio es el suministro de oxígeno y sustratos a las células, y la eliminación de los productos del metabolismo de éstas1. Este oxígeno, necesario para el metabolismo tisular, lo aportan los glóbulos rojos, que ejercen el papel de contenedores de hemoglobina, la cual es la principal molécula transportadora de oxígeno. Cualquier disminución de la concentración de hemoglobina se acompaña del correspondiente descenso de la capacidad de transporte de oxígeno en la sangre (hipoxia anémica). La presión parcial de oxígeno puede permanecer normal, pero la cantidad absoluta de oxígeno transportado por unidad de volumen de sangre disminuye. Por este motivo, la manera más sensible para establecer el diagnóstico de anemia en un paciente sería realizar una medición directa de la cantidad de oxígeno aportado a los tejidos periféricos2. Dado que esto no es posible, debemos basarnos en un diagnóstico funcional a partir de las modificaciones observadas en el proceso normal de la eritropoyesis: producción, maduración, supervivencia y morfología de los hematíes, y estudio del hierro.
La Organización Mundial de la Salud define la anemia como una cifra de hemoglobina inferior a 13 g/dl en varones y a 12 g/dl en mujeres3. Para el correcto funcionamiento de la eritropoyesis basal, las células peritubulares del riñón secretan diariamente cantidades bajas de eritropoyetina (Epo), hormona que actúa inhibiendo la apoptosis de los hematíes y estimulando su proliferación y diferenciación en normoblastos en los tejidos hematológicos4. Cuando los valores de hemoglobina disminuyen por debajo de 10,5 g/dl, se movilizan nuevas células y se incrementan de forma logarítmica los títulos de Epo. El estímulo fundamental para su producción es la disponibilidad de oxígeno en los tejidos y su transcripción genética está mediada por el factor inducible de la hipoxia. Por este motivo uno de los mecanismos de compensación de la hipoxia prolongada es la denominada eritrocitosis secundaria debida al incremento de la Epo. Este fenómeno se ha descrito tanto en situaciones en que la concentración de oxígeno es baja (permanencia en grandes altitudes) como en enfermedades de origen cardiopulmonar que cursan con hipoxemia1. El criterio más ampliamente aceptado para su diagnóstico es el valor aumentado del hematócrito por encima del 54%.
El aporte de hierro también desempeña un papel fundamental en la hematopoyesis. La mayor parte del hierro procede del que contienen los hematíes viejos, el cual es reciclado por el sistema reticuloendotelial. Este hierro lo transporta en el plasma la transferrina. La mayoría de estas moléculas de transferrina cargadas de hierro están destinadas a unirse a unos receptores específicos situados en la superficie de los precursores eritroides (receptor soluble de transferrina) para su internalización en la célula. A continuación este hierro se libera y el complejo transferrina-receptor regresa a la superficie de la célula, donde las moléculas de transferrina quedan libres para volver de nuevo a la circulación. El hierro liberado intracelularmente se utiliza para sintetizar la hemoglobina, y todo exceso de este metal se deposita en forma de ferritina5.
La anemia en la enfermedad pulmonar obstructiva crónica
La prevalencia de anemia en la población general aumenta con la edad, y la llamada "anemia inflamatoria o de trastornos crónicos" (ATC) se presenta en múltiples entidades (neoplasias, artritis reumatoide, entre otras). Si prestamos atención a estas premisas, podemos inferir que los pacientes con EPOC cumplen estos requisitos: ésta es una enfermedad crónica e inflamatoria, que afecta a una población envejecida. No obstante, no podemos olvidar que las causas de anemia en los ancianos suelen ser de origen multifactorial y que, concretamente en la EPOC, también pudiera ser la suma de diversos factores, como los trastornos nutricionales, las pérdidas sanguíneas ocultas, la administración de ciertos fármacos como la teofilina o los inhibidores de la enzima de conversión de la angiotensina, o la propia oxigenoterapia6.
Uno de los primeros trabajos publicados sobre la anemia en pacientes con EPOC fue el realizado por Tassiopoulos et al7 en 2001. Inicialmente su objetivo era estudiar las características de la anemia y la respuesta eritropoyética compensadora en pacientes diagnosticados de fibrosis pulmonar idiopática y EPOC, con insuficiencia respiratoria crónica establecida, asumiendo el hecho de que estas 2 enfermedades se comportaban de manera inversa desde el punto de vista hematológico y que el fenómeno de la eritrocitosis secundaria estaría conservado en la EPOC ante la hipoxemia crónica. Sin embargo, observaron que un subgrupo de pacientes con EPOC mostraba una respuesta de aumento de la masa globular inconsistente, presentando valores de hemoglobina normales o subóptimos, a pesar de que las concentraciones de Epo en plasma era elevadas, lo que apuntaba al papel de la inflamación como una probable causa de la misma. Estos hallazgos se han confirmado en un estudio reciente con 101 pacientes con EPOC, donde se estimó una prevalencia de anemia del 13%8. En el grupo de pacientes que cumplían el criterio de anemia se objetivó una concentración más elevada de Epo y de algunos parámetros de la inflamación como la interleucina (IL) 6 y la proteína C reactiva, en comparación con el grupo de EPOC sin anemia. Asimismo, encontraron una relación inversa entre la hemoglobina y la Epo, lo que permitía conjeturar que había cierta resistencia a la acción de esta hormona. Estos resultados, aunados al hecho de que no se observó una relación entre la anemia y las alteraciones nutricionales presentes en estos pacientes (pérdida de peso y caquexia), llevaron a los autores a concluir que el desarrollo de la anemia en la EPOC cumple los criterios de ATC, como se ha reseñado anteriormente. En este contexto, esta afirmación puede fundamentarse de manera razonable, con la suficiente evidencia científica disponible acerca de la complejidad de la respuesta inflamatoria y del estrés oxidativo que se genera en la EPOC, donde participan diversos tipos de células (neutrófilos, macrófagos y linfocitos T) y una gran variedad de mediadores proinflamatorios factor de necrosis tumoral alfa (TNF-a) y sus receptores, leucotrieno B4, IL-1, IL-6, IL-8, proteína C reactiva, fibrinógeno, entre otros9,10 que se han hallado elevados tanto en sangre periférica como en el esputo de estos pacientes, y cuyas concentraciones se incrementan durante las exacerbaciones5,9-11. Hasta ahora no se ha dilucidado la interrelación entre ellos y la secuencia de eventos. Sin embargo, sí se sabe que la intensidad de esta inflamación sistémica es directamente proporcional a la gravedad de la enfermedad12,13.
Anemia de trastornos crónicos o "anemia inflamatoria"
La ATC es un trastorno inmunitario que se ha descrito en varias enfermedades con componente inflamatorio asociado, en el que las citocinas inflamatorias ejercen diversos efectos que desempeñan un papel determinante en la patogenia de este tipo de anemia y finalmente interfieren en los mecanismos normales de la eritropoyesis. Se han propuesto varios mecanismos:
1. Alteración de la regulación de la homeostasis de hierro, por su incremento y retención dentro de las células del sistema reticuloendotelial, con la consiguiente disminución de su disponibilidad para su utilización por parte de las células progenitoras. En animales de experimentación se ha demostrado que la administración de IL-1 y de TNF-α conduce al desarrollo de hipoferrinemia14.
2. Alteración de la proliferación de precursores eritroides. El inhibidor más potente es el interferón gamma, aunque también causan este efecto los radicales libres provenientes del estrés oxidativo. Este fenómeno puede producir aumento de apoptosis de estas células o disminución de la expresión de Epo en sus receptores.
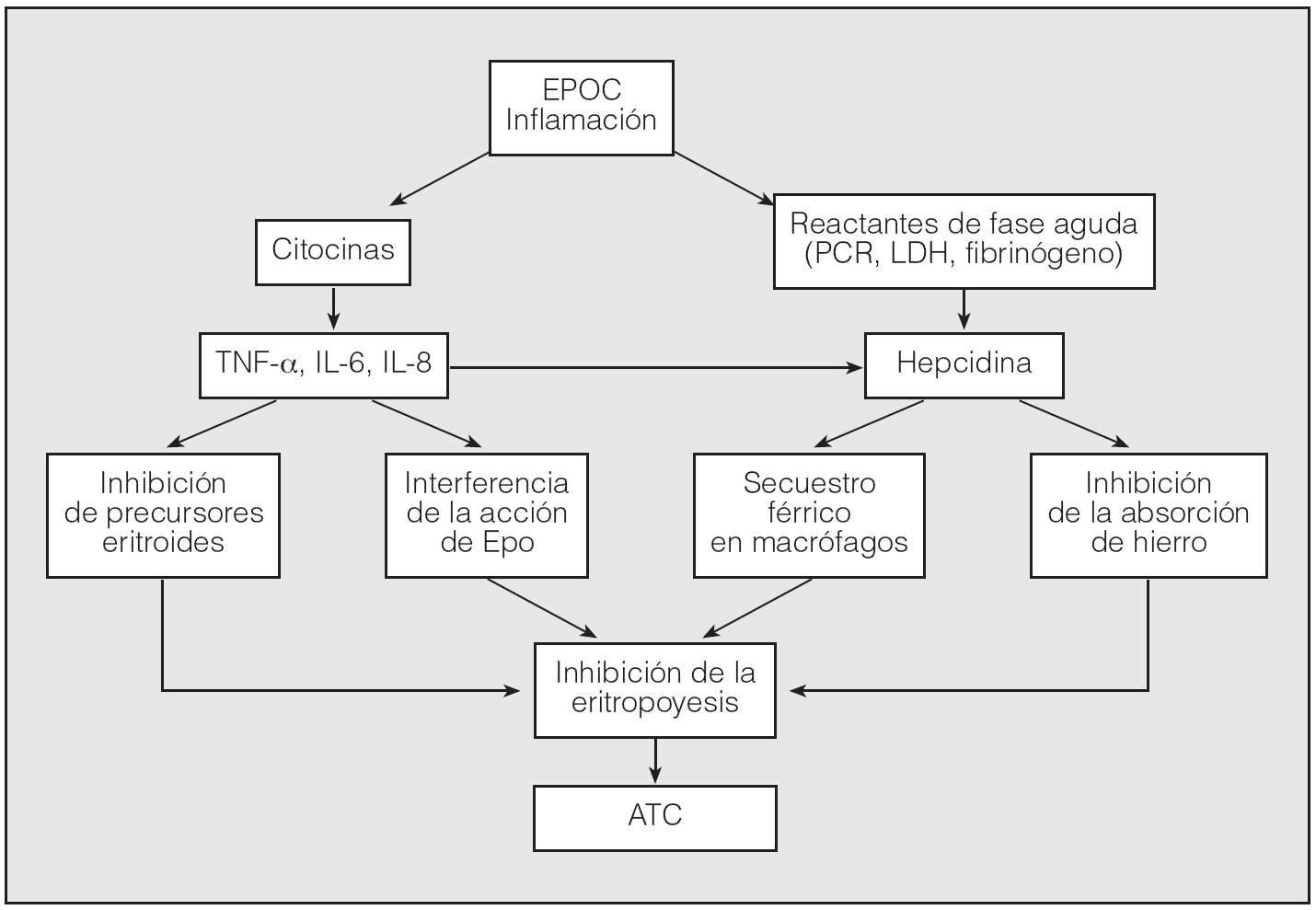
3. Alteración de la respuesta a la Epo por parte de la médula ósea por efecto directo de las citocinas. La IL-1 y el TNF-α inhiben la expresión de esta hormona in vitro. Por último, la activación de estos mediadores estimularía la producción de hepcidina, un polipéptido recientemente conocido, que se sintetiza en el hígado, participa en la absorción del hierro y se considera clave en el desarrollo de la ATC (fig. 1)14.
Fig. 1. Posible mecanismo de la anemia inflamatoria o de trastornos crónicos (ATC) en la enfermedad pulmonar obstructiva crónica (EPOC). Epo: eritropoyetina; IL: interleucina; LDH: lactatodeshidrogenasa; PCR: proteína C reactiva; TNF-α: factor de necrosis tumoral alfa.
Alteraciones de la hematopoyesis en la enfermedad pulmonar obstructiva crónica
Macrocitosis
El aumento del volumen corpuscular medio (VCM) es un hallazgo que se ha descrito en pacientes con EPOC, a pesar de que su causa todavía no está clara. Para aproximarse a este fenómeno Tsantes et al15 realizaron un estudio con 32 pacientes con EPOC e hipoxemia, en fase estable, y 34 voluntarios sanos, evaluando los siguientes parámetros: hemograma, porcentaje de células F (góbulos rojos con hemoglobina fetal), gases arteriales y valores de Epo. La macrocitosis (definida como VCM > 94 fl) se encontró en casi la mitad de los pacientes con EPOC (43,75%), mientras que un 37% tenía eritocitosis. La respuesta de la Epo no se relacionó con el grado de hipoxemia, y tampoco con la eritocitosis ni con la macrocitosis hallada, ocurriendo en algunos casos el fenómeno de manera independiente. El porcentaje de células F fue significativamente más elevado en los pacientes con EPOC y esta elevación se asoció a los valores del VCM. A partir de estos datos los investigadores postulan que en la EPOC hay un estrés eritropoyético que se produce repetidamente como resultado de las exacerbaciones y de la desaturación nocturna e inducida por el ejercicio, hecho que provoca la liberación de formas inmaduras en la médula ósea como mecanismo compensador para optimizar la capacidad transportadora de oxígeno. Los valores de hemoglobina que presentan estos pacientes pueden resultar subóptimos, aun cumpliendo el rango de normalidad, dado su grado de hipoxemia basal. Se reafirma el hecho de que el fenómeno de eritrocitosis secundaria no se observa de manera consistente en todos los pacientes con EPOC y que el aumento del hematócrito y de la masa globular a menudo no es tan alto en comparación con el de individuos que viven en grandes alturas.
En un trabajo publicado recientemente por García-Pachón y Padilla-Navas16 se analiza también esta observación, esta vez en pacientes con EPOC sin hipoxemia, y se plantea su posible relación con otros parámetros funcionales. La prevalencia de macrocitosis en su muestra de estudio (n = 58) fue del 29%. No hubo relación entre el VCM y la saturación arterial de oxígeno, resultado similar a los descritos previamente. Sin embargo, el hallazgo más interesante de este estudio fue que en un subgrupo de exfumadores (9/36%) se encontró una relación significativa con la disnea y con el volumen espiratorio forzado en el primer segundo, lo cual sugeriría que el grado de macrocitosis quizá esté asociado a una peor situación clínica.
Alteración del sistema renina-angiotensina-aldosterona
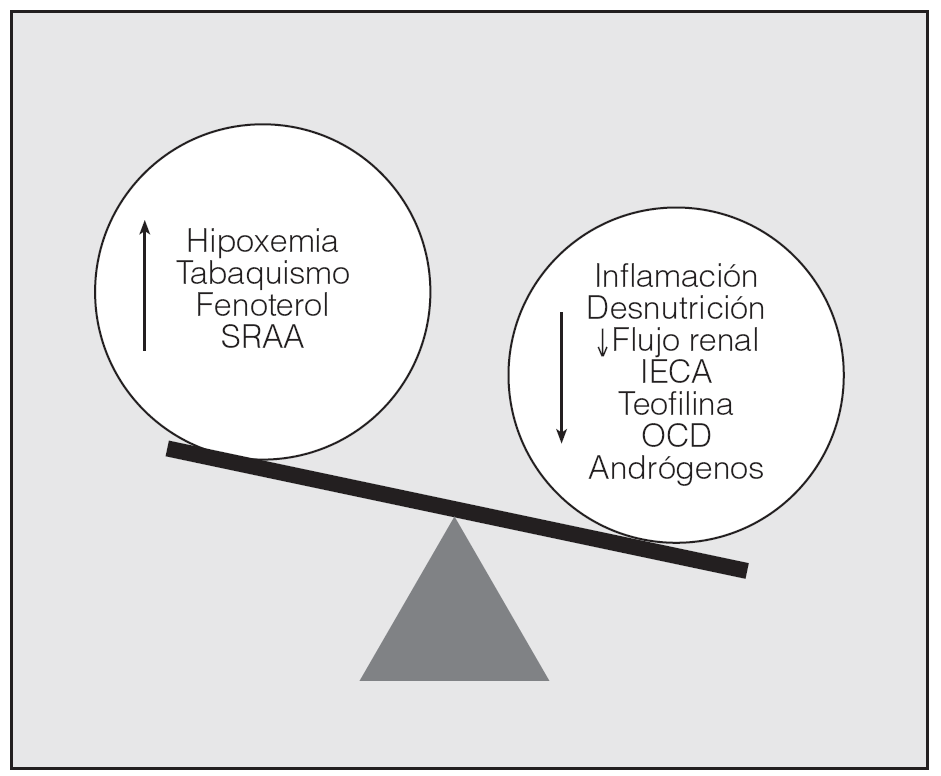
Varias observaciones clínicas y experimentales demuestran que la EPOC causa una activación neurohumoral, la cual presumiblemente contribuye a perpetuar el círculo vicioso de su patogenia y se relaciona con los efectos sistémicos de la enfermedad17. Se ha contemplado que la alteración en la activación del sistema renina-angiotensina-aldosterona (SRAA) pudiera ayudar a explicar en parte las divergencias encontradas en cuanto a la presencia de eritocitosis en los pacientes con EPOC (fig. 2). Hay una posible asociación entre la activación de este sistema y la policitemia en ciertas condiciones clínicas como la insuficiencia cardíaca grave, el trasplante renal, la hemodiálisis crónica y la hipertensión arterial renovascular18. En el estudio de Vlahakos et al19 incluso se observó el aumento de secreción de Epo después de la administración de renina o angiotensina II en animales de experimentación; por ende, la administración de inhibidores de la enzima de conversión de la angiotensina se acompaña del descenso de los valores de Epo y de hematócrito. Dichos autores se propusieron estudiar en qué medida la activación de este sistema se relacionaba con el desarrollo de la eritrocitosis compensadora en pacientes con EPOC e hipoxemia. Las concentraciones de renina y aldosterona fueron 3 veces mayores en los pacientes con eritrocitosis que en el grupo control, que estaba formado por pacientes con EPOC e hipoxemia pero sin eritrocitosis. No se observaron diferencias en los valores séricos de Epo entre los grupos, mientras que la renina y la presión parcial de oxígeno fueron las únicas variables asociadas con el hematócrito. Esta falta de relación entre la Epo y el hematócrito indica la presencia de otro mecanismo implicado en el desarrollo de la poliglobulia, como, por ejemplo, la acción directa de la angiotensina II, que induciría una secreción mantenida de Epo o bien actuaría sobre los precursores eritroides favoreciendo su proliferación, ya que esta molécula tiene un reconocido papel como factor de crecimiento de varios tipos celulares. En función de los datos obtenidos, los autores apuntan que la variabilidad de los parámetros relacionados con la masa globular encontrada en pacientes con EPOC que presentan el mismo grado de hipoxemia puede depender de alguna forma de la integridad del SRAA19.
Fig. 2. Factores relacionados con la eritrocitosis en la EPOC. IECA: inhibidores de la enzima de conversión de la angiotensina; OCD: oxigenoterapia crónica domiciliaria; SRAA: sistema renina-angiotensina-aldosterona.
Otros factores
Flujo renal. Dado que el riñón es el principal órgano implicado en la secreción de Epo, la alteración en la hemodinámica renal, descrita también en la EPOC como consecuencia de la disminución del flujo sanguíneo, ocasiona un desequilibrio en la relación entre la demanda y el consumo de oxígeno que influye en la producción de esta hormona por posible afectación del sensor de oxígeno20.
Fármacos. Se ha visto que, además de los inhibidores de la enzima de conversión de la angiotensina, que producen una reducción del hematócrito por los fenómenos antes descritos, la teofilina causa una disminución de la producción de hematíes. El mecanismo de supresión es complejo y en principio puede derivar de la inhibición directa de la eritropoyesis a través de la apopotosis inducida por este fármaco, más que de un efecto sobre la Epo21. Por el contrario, el fenoterol, un agente betamimético empleado en el tratamiento de la EPOC, actúa sobre el SRAA estimulando directamente la secreción de esta hormona18.
Andrógenos. Los andrógenos pueden promover la eritropoyesis, también por estimulación directa de los progenitores eritroides o indirectamente a través de la activación del SRAA18; de hecho, la anemia es un hallazgo frecuente en varones con hipogonadismo o que reciben tratamiento antiandrogénico. Además, los títulos de testosterona disminuyen con la edad. Actualmente hay evidencia de que en los varones con EPOC las concentraciones de testosterona son bajas22. Entre los factores que predisponen a ello se han planteado los siguientes: la hipoxia, el tratamiento corticoide y la naturaleza crónica de la enfermedad. Un estudio publicado recientemente con una muestra de 905 pacientes mayores de 65 años concluye que los títulos bajos de testosterona se asocian a un mayor riesgo de presentar anemia23.
Exacerbaciones. Las exacerbaciones representan un acontecimiento adverso, frecuente en la historia natural de los pacientes con EPOC. Como se ha señalado antes, durante ellas se produce un incremento de los marcadores inflamatorios, que podrían interferir en el proceso hematopoyético. De igual modo, las exacerbaciones que requieren ingreso pueden alterar el valor de la hemoglobina basal, ya que se ha descrito su disminución por diversos factores durante las hospitalizaciones.
Relación de otras enfermedades cardiopulmonares con la anemia
Insuficiencia cardíaca
Numerosos estudios que han evaluado la relación entre la anemia y la insuficiencia cardíaca han determinado que la presencia de anemia como comorbilidad asociada incrementa el número de hospitalizaciones y reingresos24, actúa como factor independiente de mortalidad y su tratamiento mejora la calidad de vida, la capacidad funcional y el pronóstico de estos pacientes25,26. En este sentido, John et al27 compararon en un estudio retrospectivo en pacientes hospitalizados la prevalencia de anemia en pacientes con EPOC con respecto a otras enfermedades pulmonares, como el asma y a otras enfermedades crónicas asociadas tradicionalmente a esta entidad, como la insuficiencia renal crónica, el cáncer y la insuficiencia cardíaca. Establecieron una prevalencia de anemia en pacientes con EPOC del 23%, porcentaje similar al que se observó en la insuficiencia cardíaca, pero mayor que en el asma y menor que en pacientes afectados de cáncer o insuficiencia renal crónica. En los pacientes diagnosticados de EPOC la anemia no estuvo asociada a la edad ni al hábito tabáquico. Este estudio presenta algunas limitaciones: no puede determinarse la influencia de ciertos fármacos en el valor de hemoglobina ni cuantificarse el efecto que la hospitalización produce sobre los valores hematimétricos. Sin embargo, no cabe duda de su valiosa aportación al concluir que la anemia no se presenta como un fenómeno excepcional en la EPOC y que podría ser otra diana terapéutica que mejore el pronóstico.
Fibrosis pulmonar
La fibrosis pulmonar idiopática (FPI) es una entidad clinicopatológica compleja de etiología desconocida, que produce destrucción irreversible de las unidades alevolares. Al igual que en la EPOC, se ha descrito que las concentraciones de citocinas inflamatorias están elevadas y que cursa en fases avanzadas con insuficiencia respiratoria progresiva. Además del estudio de Tassiopoulos et al7 descrito en párrafos anteriores, otro trabajo realizado por el mismo equipo de investigación analiza la respuesta eritopoyética alterada que se ha observado en esta enfermedad y su relación con la inflamación. El primero7 incluyó a 9 pacientes diagnosticados de FPI con hipoxemia y a 34 voluntarios sanos como grupo control, en quienes se evaluó, además de los valores hematológicos, de Epo y citocinas séricas, el desarrollo de unidades formadoras de colonias de eritrocitos (CFU-e) mediante el cultivo de las células mononucleares de los sujetos incluidos en varias condiciones experimentales. A estos cultivos se añadieron suero inactivado y suero proveniente de cada grupo. Se encontraron los siguientes resultados: los valores de hemoglobina y Epo fueron similares en ambos grupos, a pesar de la hipoxemia que presentaban los pacientes con FPI. En este grupo, las concentraciones de TNF-α, IL-6 e IL-8 estuvieron significativamente más elevadas que en el grupo control. El suero extraído de los pacientes con FPI produjo menor crecimiento de CFU-e en los cultivos de ambos grupos, comparados con los cultivos que contenían suero inactivado (p < 0,05). Por último, se observó un incremento de las CFU-e en el cultivo de pacientes con FPI en presencia de suero inactivado. Estos resultados indican que en la FPI se produce una proliferación de precursores eritroides como mecanismo compensador ante la hipoxemia, que sin embargo falla en el proceso de diferenciación y maduración, con la consiguiente eritropoyesis ineficaz, junto con los valores subóptimos de Epo; cabe presumir que todos estos fenómenos están propiciados en parte por la inflamación intrínseca de la enfermedad.
El segundo ensayo clínico vuelve a tomar la EPOC como enfermedad de referencia28. Se propuso investigar las diferencias en la eritropoyesis entre la FPI y la EPOC repitiendo el experimento anterior, es decir, comparando los valores hematológicos, la Epo y el comportamiento de las de CFU-e proveniente de ambos grupos y un grupo control, en presencia tanto de suero obtenido de la muestra en estudio como de suero inactivado. Los resultados confirmaron los hallazgos observados en el estudio anterior con respecto a la FPI: valores significativamente inferiores de hemoglobina y Epo en comparación con los pacientes con EPOC, a pesar de que el grado de hipoxemia era equiparable. El aumento de las CFU-e de los cultivos de los pacientes con FPI con suero inactivado y la inhibición de su crecimiento ante la presencia de suero de FPI no se observaron en el grupo con EPOC28. En conclusión, este trabajo reafirma el hallazgo de la Epo elevada en la EPOC, comunicado en otros estudios, hecho que puede apoyar la hipótesis de la resistencia a la acción de esta hormona en un subgrupo de pacientes. Por otro lado, la importancia de este estudio radica en que es el primero en investigar de manera experimental uno de los mecanismos propuestos para describir la influencia de la inflamación de la EPOC en el comportamiento de las células de la serie roja; es decir, no sólo contribuye a tratar de discernir la patogenia de la anemia en la FPI, sino que también invita a seguir indagando sobre aspectos alternativos o sinérgicos que produzcan la anemia en la EPOC.
Fibrosis quística
Considerada hasta hace poco una enfermedad exclusivamente pediátrica, la fibrosis quística es ahora también una enfermedad de adultos debido al aumento de la supervivencia que se ha conseguido en los últimos años. En estos pacientes se ha descrito la síntesis de diversos mediadores de la inflamación (IL-1, IL-8 y TNF-α), incluso antes de que se produzca la colonización por Pseudomonas aeruginosa29, lo que podría ser la base para la aparición de anemia30,31. No obstante, los factores nutricionales también entrarían en juego, aunque tendrían menos protagonismo debido a su adecuado manejo en el tratamiento integral de estos pacientes, como plantean O'Connor et al29 en un estudio de casos y controles llevado a cabo en 15 pacientes con fibrosis quística. Estos últimos presentaron valores inferiores de saturación de oxígeno tanto en reposo como durante el ejercicio respecto a los voluntarios sanos (p < 0,0001); sin embargo, los valores de hemoglobina y hematócrito no difirieron de manera significativa entre ambos grupos. No fue el caso de algunos parámetros funcionales relacionados con la cinética del hierro, que sí se encontraron más disminuidos en el grupo con fibrosis quística (sideremia, transferrina y capacidad total de fijación de hierro; p < 0,05). Se trataría, pues, de una enfermedad pulmonar que cursa con "anemia relativa", término utilizado para describir que los valores de hemoglobina alcanzados no guardan relación con la hipoxemia presente. Estas interesantes observaciones merecen ser respaldadas por más estudios controlados.
Efectos de la anemia en la enfermedad pulmonar obstructiva crónica
Es conocido que la anemia es una causa per se de disnea y, por otro lado, que contribuye a la limitación funcional de quienes la presentan. Sin embargo, hasta la fecha no hay trabajos prospectivos que relacionen esta entidad con parámetros como la tolerancia al ejercicio, la propia disnea o el impacto en la calidad de vida en pacientes con EPOC. No obstante, no es anecdótico el hecho de que las concentraciones bajas de hemoglobina pueden provocar un efecto nocivo en algunas variables respiratorias y que éstas mejoran con su corrección mediante estrategias de tratamiento. En concreto, Schonhofer et al32,33 han publicado los 2 únicos estudios disponibles en la literatura médica sobre este tema en el ámbito de una unidad de cuidados intensivos. Su intervención terapéutica se fundamentó en transfundir a un grupo de 20 pacientes diagnosticados de EPOC grave y anemia, con lo que se observó una reducción estadísticamente significativa de la ventilación-minuto y del trabajo respiratorio, con descarga de los músculos respiratorios. Previamente habían publicado una serie de 5 pacientes con EPOC que habían requerido ventilación invasiva y en los que la retirada de ésta (weaning) era dificultosa. El aumento de los valores de hemoglobina hasta un valor superior a 12 g/dl tras la hemotransfusión consiguió la extubación de manera satisfactoria.
Por lo que se refiere a un aspecto de gran trascendencia, como el efecto de la anemia sobre los costes sanitarios y, aún más importante, su relación con la mortalidad en la EPOC, es ineludible mencionar el estudio de Celli et al34 sobre el índice BODE (índice de masa corporal, obstrucción al flujo aéreo, disnea y capacidad de ejercicio) como artículo de referencia. En dicho estudio los pacientes que murieron presentaban un hematócrito significativamente menor que los supervivientes. Un año más tarde, el estudio observacional ANTADIR35, efectuado sobre una población de 2.524 pacientes con EPOC y oxigenoterapia domiciliaria (con una prevalencia de anemia del 12,6% en varones y del 8,2% en mujeres), demostró mediante un análisis multivariante que el hematócrito disminuido era un gran predictor de supervivencia y que además se asociaba a mayor número de hospitalizaciones y mayor duración de la estancia media. En concreto, los marcadores de supervivencia de esta cohorte fueron, en orden descendente: edad, hematócrito, índice de masa corporal, presión parcial de oxígeno, sexo y volumen espiratorio forzado en el primer segundo. Por último, vale la pena destacar el trabajo llevado a cabo por Martínez et al36 sobre los predictores de mortalidad en pacientes con enfisema y obstrucción grave del flujo aéreo, que tomó como población de estudio a los pacientes aleatorizados a recibir tratamiento médico en el National Emphysema Treatment Trial (NETT). Dichos autores observaron que la hemoglobina disminuida actuaba como factor independiente de mortalidad, junto con otras variables como, por ejemplo, la edad, el uso de oxigenoterapia, un mayor volumen residual y un índice BODE mayor, entre otros.
Conclusiones
Asumir casi como un dogma que los pacientes diagnosticados de EPOC con hipoxemia están "protegidos" de las consecuencias fisiopatológicas de la anemia a través del mecanismo de eritrocitosis secundaria puede entorpecer su adecuado manejo, ya que, como se ha señalado a lo largo del artículo, este fenómeno no acontece en la totalidad de estos pacientes, lo cual no sólo demuestra una vez más la heterogeneidad de esta enfermedad, sino que también pone de manifiesto los diversos y complejos factores implicados en ella que pueden alterar la hematopoyesis. Concretamente en la EPOC se puede hablar de un desequilibrio en la hemoglobinemia debido a que hay factores que estimulan la eritropoyesis (el aumento de la Epo ante la hipoxemia, la desaturación arterial nocturna, el tabaquismo, un adecuado funcionamiento del SRAA) y factores que la disminuyen (mediadores inflamatorios, fármacos, desnutrición y oxigenoterapia).
El hecho de que importantes publicaciones hayan documentado que la anemia se presenta como un factor de supervivencia en la EPOC es un paso de gigante para abordar el tema e intentar, mediante trabajos controlados, indagar sobre aspectos tan relevantes como su verdadera prevalencia, sus mecanismos patogénicos, su relación con los síntomas de la enfermedad y su influencia sobre la capacidad funcional o la calidad de vida de estos pacientes. Debemos tener en cuenta esta entidad en la práctica clínica diaria para poder identificarla y tratarla, si fuera el caso. No obstante, antes de plantear un enfoque terapéutico es preciso valorar de forma adecuada su extensión, sus causas y los factores que predisponen a ella. La evidencia científica actual pone de manifiesto que las alteraciones extrapulmonares cobran cada vez más importancia en esta enfermedad y que si dirigimos nuestras intervenciones hacia ellas podríamos influir en la mortalidad global de la EPOC37.
Correspondencia: Dra. K. Portillo Carroz.
Servicio de Neumología. Consorcio Sanitario Integral. Hospital Dos de Maig.
Dos de Maig, 301. 08025 Barcelona. España.
Correo electrónico: karisoe@yahoo.es
Recibido: 29-8-2006; aceptado para su publicación: 19-9-2006.