En la literatura científica se han publicado resultados contradictorios sobre el valor pronóstico de la pérdida de la expresión del antígeno de grupo sanguíneo A (GSA) en el cáncer de pulmón, por lo que analizamos retrospectivamente este hecho en nuestra serie quirúrgica.
Pacientes y métodosEn un estudio multicéntrico de 402 pacientes con carcinoma no microcítico de pulmón (CNMP) en estadio I patológico según la nueva clasificación TNM-2009 se analizó la influencia pronóstica de la pérdida de la expresión del antígeno del GSA en los 209 pacientes con grupos sanguíneos A o AB.
ResultadosLa supervivencia a los 5 años de los pacientes en estadio I patológico que mantenían la expresión del antígeno del GSA fue del 73%, frente a una supervivencia del 53% en los pacientes que habían perdido la expresión del mismo (p=0,03). Cuando se analizó la supervivencia subdividiendo la muestra en estadios IA y IB, solo se alcanzó la significación estadística en el estadio IA (p=0,038). Al analizar la supervivencia según el tipo histológico, los pacientes con adenocarcinoma que perdían la expresión del antígeno del GSA tenían una menor supervivencia, con una p estadísticamente muy significativa (p=0,003). El análisis multivariable mostró que la edad, el género y la expresión del antígeno del GSA eran factores pronósticos independientes
ConclusionesLa pérdida de la expresión del antígeno del grupo sanguíneo A tiene una influencia pronóstica negativa en el CNMP estadio I patológico, sobre todo en el tipo histológico adenocarcinoma.
In the scientific literature, contradictory results has been published on the prognostic value of the loss of expression of blood group antigen A (BAA) in lung cancer. The objective of our study was to analyze this fact in our surgical series.
Patients and methodsIn a multicenter study, 402 non-small-cell lung cancer (NSCLC) patients were included. All were classified as stage-I according to the last 2009-TNM classification. We analyzed the prognostic influence of the loss of expression of BAA in the 209 patients expressing blood group A or AB.
ResultsThe 5-year cumulative survival was 73% for patients expressing BAA vs 53% for patients with loss of expression (P=.03). When patients were grouped into stages IA and IB, statistical significance was only observed in stage I-A (P=.038). When we analyzed the survival according to histologic type, those patients with adenocarcinoma and loss of expression of BAA had a lower survival rate that was statistically very significant (P=.003). The multivariate analysis showed that age, gender and expression of BAA were independent prognostic factors.
ConclusionsThe loss of expression of blood group antigen A has a negative prognostic impact in stage I NSCLC, especially in patients with adenocarcinoma.
El cáncer de pulmón es la primera causa de mortalidad por enfermedad neoplásica1, y su pronóstico sigue siendo muy pobre a pesar de los avances de la medicina en las últimas décadas2.
En 2009 se publicó la nueva clasificación TNM del cáncer de pulmón3,4, la cual ha introducido importantes modificaciones, ampliamente validadas5, en el sistema de estadificación.
El 80% aproximadamente de todos los cánceres de pulmón pertenecen al grupo de los carcinomas no microcíticos de pulmón (CNMP). El factor pronóstico más importante en el CNMP es el estadio tumoral. Otros factores que empeoran el pronóstico son el género masculino y la edad avanzada6. La resección quirúrgica completa es el tratamiento de elección de los estadios iniciales del CNMP, aunque los métodos y abordajes quirúrgicos están evolucionando7. Aproximadamente el 30% de los pacientes con CNMP en estadio I a los que se les ha practicado una resección completa recidivan y fallecen antes de los 5 años, fundamentalmente por la presencia de enfermedad micrometastásica en el momento de la resección8, aunque no se conocen los mecanismos ni en qué pacientes se van a producir estas recurrencias.
Los antígenos del grupo sanguíneo ABH se describieron originalmente en la membrana de los glóbulos rojos, pero posteriormente se han encontrado en la mayoría de los epitelios, endotelios y secreciones del organismo9. Consisten en una variedad de glucolípidos y glucoproteínas cuya especificidad antigénica viene determinada por la variación en los constituyentes de sus cadenas de hidratos de carbono10. Desde hace varias décadas se conoce la existencia en los tumores de cambios en los patrones de glucosilación de los glucolípidos y glucoproteínas de la superficie celular. Estudios recientes parecen indicar que dichas alteraciones son el resultado de una transformación oncogénica inicial y un elemento clave en la inducción de la invasión tumoral y en el desarrollo de metástasis11. En algunos tumores, la elevada expresión de ciertos antígenos glucosilados promueve la invasión y las metástasis, mientras que la expresión de otros antígenos glucosilados suprime la progresión tumoral. El mecanismo de expresión de estos antígenos, en lo que se refiere al estado de los genes de sus respectivas glucosiltransferasas, se he estudiado ampliamente. Sin embargo, se sabe muy poco sobre los mecanismos a través de los cuales los antígenos glucosilados inducen fenotipos invasivos y metastáticos en las células tumorales12. Los determinantes antigénicos del grupo sanguíneo ABH se localizan en la porción terminal de las cadenas de los hidratos de carbono de los glucolípidos y glucoproteínas de la membrana celular y su grado de expresión depende del tipo de diferenciación del epitelio y del grado de maduración de la célula dentro del mismo13. La pérdida de la expresión de los antígenos del grupo sanguíneo ABH está causada por la pérdida de la actividad de las glucosiltransferasas específicas, secundaria a la deleción o la pérdida de heterocigosidad en el brazo largo del cromosoma 9 (uno de los cromosomas más intensamente implicados en la carcinogénesis) donde se localizan sus alelos o a la hipermetilación del ADN de su región promotora, que impide que se pueda realizar de la transcripción14. La pérdida de la expresión de los antígenos del grupo sanguíneo ABH se describió por primera vez en el cáncer gástrico15. Desde entonces, este fenómeno y su relación con el pronóstico se han descrito en carcinomas de cabeza y cuello, pulmón, tracto gastrointestinal, ovario, vejiga y mama14. En el caso del cáncer de pulmón se han publicado muy pocos artículos en este sentido. Concretamente, los primeros que en el cáncer de pulmón relacionaron la pérdida de la expresión del antígeno del grupo sanguíneo A (GSA) con el pronóstico fueron Lee et al.16. Sin embargo, en otros artículos no se ha podido demostrar esa relación pronóstica17,18.
Debido a la controversia existente en la literatura, el objetivo de este estudio ha sido realizar un amplio estudio multicéntrico para analizar la influencia pronóstica de la pérdida de la expresión del GSA en el CNMP en estadio I patológico, según el nuevo sistema de estadificación TNM-2009.
Pacientes y métodosPacientesNuestra serie quirúrgica, de la que en septiembre de 2011 se ha publicado un estudio de supervivencia y factores pronósticos en esta revista19, estaba compuesta por pacientes intervenidos por CNMP en los servicios de cirugía torácica del Hospital General Universitario Gregorio Marañón (entre los años 1991 y 2005), del Complejo Hospitalario Xeral-Cies de Vigo (entre los años 2000 y 2004) y del Complejo Hospitalario Universitario de Albacete (entre los años 2001 y 2006), en estadio I patológico mediante resección pulmonar completa y que no habían recibido tratamiento adyuvante o de inducción. Se consideró que se había practicado una resección completa cuando los límites quirúrgicos estaban libres de tumor y no había metástasis en los ganglios analizados tras realizar una linfadenectomía mediastínica sistemática. Se excluyeron los pacientes que fallecieron en los primeros 30 días después de la cirugía y en los que se pudo realizar un seguimiento postoperatorio. Se recogieron las siguientes variables: edad, sexo, tipo de resección practicada, estirpe histológica, grado de diferenciación, tamaño tumoral y estadio (IA y IB) según la nueva clasificación TNM del cáncer de pulmón de 20093. En el seguimiento postoperatorio en consultas externas se registraron las recidivas y las causas de los fallecimientos. Se consideró que se había producido una recidiva locorregional o a distancia cuando la evidencia de criterios clínicos, analíticos, radiológicos (fundamentalmente hallazgos compatibles en la tomografía computarizada), histológicos o una combinación de ellos sostenía la existencia de dicha afectación secundaria. Debido a que se trata de un estudio con carácter retrospectivo de pacientes intervenidos por cáncer de pulmón, todos ellos firmaron previamente a la cirugía el documento de consentimiento informado en el que se refleja que autorizan la utilización de sus datos con fines de investigación, por lo que para el comité ético de investigación no fue necesaria la firma de un nuevo documento de consentimiento informado específico para este estudio.
Estudio inmunohistoquímicoLos bloques tumorales en parafina más representativos de los pacientes del Complejo Hospitalario Xeral-Cies de Vigo y del Complejo Hospitalario Universitario de Albacete se enviaron al departamento de anatomía patológica del Hospital General Universitario Gregorio Marañón, donde las muestras histológicas fueron analizadas por dos patólogos para confirmar el tipo histológico y se realizó el estudio inmunohistoquímico. Se utilizó la vigente clasificación de la OMS de los tumores de pulmón publicada en 200420.
Tras realizar el estudio inmunohistoquímico que se detalla a continuación, los pacientes que en los tejidos broncopulmonares normales expresaban el antígeno del GSA se identificaron como pertenecientes a los grupos sanguíneos A o AB. En este subgrupo de pacientes es en el que se estudió el valor pronóstico de la pérdida de la expresión del antígeno del GSA.
El anticuerpo que se utilizó fue el BG-2 (clon T36), que es válido para tejidos incluidos en parafina y corresponde a un tipo de IgG3 que posee especificidad para las cadenas tipo 1 y tipo 2 del GSA (GeneTex Inc., Irvine, California, EE. UU.).
La técnica de inmunotinción utilizada fue el sistema ABC (Complejo Avidina-Biotina), que consta de los siguientes pasos: desparafinado de los cortes con xileno, etanol y alcohol de 96°; hidratación; bloqueo de la peroxidasa endógena mediante inmersión en una solución de agua oxigenada en metanol al 5% durante 5min; lavado en solución tampón (PBS); incubación con suero bloqueador; incubación con el anticuerpo primario; lavado en tampón PBS; incubación con el anticuerpo secundario biotinado; lavado en tampón PBS; incubación con el complejo avidina-peroxidasa-biotina; lavado en tampón PBS; incubación con la solución cromógena reveladora de diaminobencidina: lavado en agua destilada; ligera tinción de contraste con hematoxilina de Carazzi; lavado breve en agua corriente, deshidratación, aclarado y montaje en medio permanente.
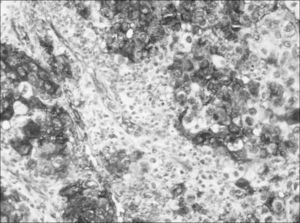
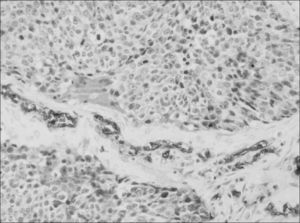
Al igual que en la gran mayoría de los artículos publicados sobre el valor pronóstico de la pérdida de la expresión tumoral en el cáncer de pulmón16-18,21,22, en nuestro estudio la expresión en el tejido tumoral del antígeno del GSA en los pacientes con grupos sanguíneos A o AB se consideró positiva cuando el porcentaje de células teñidas era mayor del 5%. El resultado se consideró negativo cuando las células demostraron no teñirse en relación con los adecuados controles internos (epitelio bronquial, glándulas bronquiales, endotelio vascular y eritrocitos). Cuando las células se teñían entre un 1 y un 5%, el resultado se consideró equívoco y, para el análisis estadístico, se agruparon con los casos negativos (figs. 1 y 2).
El análisis estadístico se realizó mediante el programa informático SPSS 15.0 para Windows. La normalidad de las variables cuantitativas se demostró con el test de Kolmogorov-Smirnov. La comparación de variables cuantitativas independientes se realizó: si la variable seguía una distribución normal, mediante el test de la t de Student, y si la variable seguía una distribución no normal, mediante la prueba de la U de Mann-Whitney o el test de Kruskal-Wallis. La relación existente entre dos variables categóricas se estudió mediante el test de la Chi-cuadrado. El análisis de supervivencia se realizó mediante el método de Kaplan-Meier, y para comparar las curvas de supervivencia se empleó la prueba de logaritmo de rango (log-rank). Para el análisis multivariable se construyó un modelo de regresión múltiple de riesgos proporcionales de Cox (método «enter»). De este modo se calculó el riesgo de muerte de cada variable, controlando la presencia o no del resto de variables incluidas en el modelo. Se consideró que se alcanzó la significación estadística cuando p<0,05.
ResultadosLa muestra seleccionada para el estudio consistió en 402 pacientes19, de los cuales 180 fueron intervenidos en el Hospital General Universitario Gregorio Marañón, 135 en el Complejo Hospitalario Xeral-Cies de Vigo y 87 en el Complejo Hospitalario Universitario de Albacete. Tras realizar el estudio inmunohistoquímico, 209 pacientes (52%) expresaban el antígeno del GSA en tejidos broncopulmonares normales, por lo que fueron identificados como pertenecientes a los grupos sanguíneos A o AB.
De los 209 pacientes con grupos sanguíneos A o AB, 126 (60%) mantenían la expresión en el tumor del antígeno del GSA y 83 (40%) la habían perdido. Ciento ochenta y dos (87%) eran varones y 58 (28%) tenían más de 70 años. La resección más frecuente fue la lobectomía (70%). La distribución por tipos histológicos, grados de diferenciación y estadios se describe en la tabla 1.
Datos relativos al tumor pulmonar de los pacientes con grupos sanguíneos A o AB
| N=209 | N.° de pacientes | % |
| Datos del tumor pulmonar | ||
| Tipo histológico | ||
| Epidermoide | 100 | 48% |
| Adenocarcinoma | 102 | 49% |
| Células grandes | 7 | 3% |
| Grado de diferenciación | ||
| Bueno | 38 | 18% |
| Moderado | 94 | 45% |
| Pobre | 77 | 37% |
| Estadio | ||
| IA | 77 | 37% |
| IB | 132 | 63% |
Después de un seguimiento medio de 70,18 meses (rango: 1,8-218,07), 98 pacientes (47%) se encontraban vivos y libres de enfermedad, 8 pacientes (4%) estaban vivos con recidiva tumoral, 71 pacientes (34%) habían fallecido por recidiva tumoral y 32 pacientes (15%) habían fallecido por otras causas.
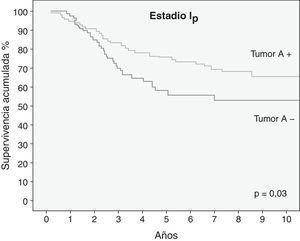
No se alcanzó la mediana de supervivencia. La supervivencia a los 5 años de los pacientes con grupos sanguíneos A o AB y CNMP en estadio I patológico que mantenían la expresión en el tumor del antígeno del GSA fue del 73%, frente a una supervivencia del 53% de los pacientes que habían perdido la expresión del mismo. La diferencia encontrada fue estadísticamente significativa, como se muestra en la figura 3.
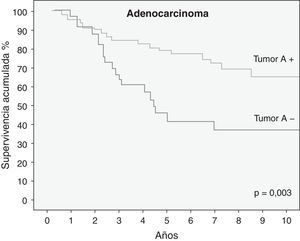
También se analizó la supervivencia en función de la expresión tumoral del antígeno del GSA estratificando por estadios. Tanto en el estadio IA como en el IB se apreció una influencia clínica relevante, pero solo se alcanzó la significación estadística en el estadio IA (tabla 2). Por último, se analizó la supervivencia en función de la expresión tumoral del antígeno del GSA estratificando según el tipo histológico (tabla 2). Los pacientes con adenocarcinoma que habían perdido la expresión del antígeno del GSA tenían una menor supervivencia (fig. 4), con una p estadísticamente muy significativa (p=0,003). Esta diferencia no se encontró en el carcinoma epidermoide (p=0,58). No se estudió esta relación en el carcinoma de células grandes por el escaso número de pacientes de este grupo (7 pacientes).
Resultados de supervivencia a los 5 años de los pacientes con grupos sanguíneos A o AB en función de la expresión del antígeno del GSA estratificando según el estadio y el tipo histológico
| Expresión del antígeno del GSA | |||
| Negativan-Sv% | Positivan-Sv% | p | |
| Supervivencia global a los 5 años | |||
| Estadio | |||
| IA | 31-63% | 46-86% | 0,038 |
| IB | 52-51% | 80-60% | 0,20 |
| Tipo histológico | |||
| Epidermoide | 45-65% | 55-67% | 0,58 |
| Adenocarcinoma | 36-36% | 66-65% | 0,003 |
GSA: grupo sanguíneo A; n: número de pacientes; Sv%: supervivencia global a los 5 años, en porcentaje.
En el análisis multivariable realizado mediante la regresión de Cox se incluyeron las mismas variables que en nuestro estudio previo sobre factores pronósticos en el CNMP en estadio I patológico19: edad (>70 años vs. ≤70 años), género, tipo histológico, tipo de resección, estadio patológico (IB vs. IA), junto con la variable «expresión del antígeno del GSA». El análisis multivariable mostró que la edad, el género y la expresión del antígeno del GSA eran factores pronósticos independientes (tabla 3).
Análisis multivariable según el modelo de riesgos proporcionales de Cox de los pacientes con grupos sanguíneos A o AB
| Análisis multivariable de supervivencia | |||
| p | HR | IC 95% de HR | |
| Edad (>70 vs. <70) | 0,035 | 1,033 | 1,002-1,065 |
| Género (varón vs. mujer) | 0,040 | 2,936 | 1,052-8,190 |
| Tipo histológico | 0,184 | – | – |
| *Epidermoide vs. adenocarcinoma | 0,071 | 1,596 | 0,961-2,650 |
| *Epidermoide vs. carcinoma de células grandes | 0,987 | 1,012 | 0,238-4,291 |
| Tipo de resección | 0,799 | – | – |
| *Resección atípica vs. lobectomía | 0,795 | 1,092 | 0,564-2,111 |
| *Resección atípica vs. neumonectomía | 0,517 | 1,354 | 0,541-3,384 |
| Estadio (IB vs. IA) | 0,068 | 1,657 | 0,964-2,849 |
| Expresión del antígeno del GSA (no vs. sí) | 0,045 | 1,628 | 1,010-2,626 |
GSA: grupo sanguíneo A; HR: hazard ratio; IC: intervalo de confianza; vs.: versus.
En nuestra serie de 209 pacientes con grupos sanguíneos A o AB y CNMP en estadio I patológico según la 7.ª edición de la clasificación TNM de 2009 se demuestra que la pérdida de la expresión del antígeno del GSA es un factor pronóstico desfavorable (p=0,03), fundamentalmente en el tipo histológico adenocarcinoma (p=0,003).
Los primeros en proponer esta asociación pronóstica fueron Lee et al.16 en 1991, en un estudio de 164 pacientes. Sin embargo, en su estudio solo había 27 pacientes en estadio I con grupos sanguíneos A o AB.
En 1997, Graziano et al.23 realizaron un estudio con una serie de 260 pacientes, de los que 70 se encontraban en estadio I, obteniendo que los 29 pacientes que habían perdido la expresión del antígeno del GSA tenían una mediana de supervivencia de 41 meses, frente a los 41 pacientes que conservaban la expresión del antígeno del GSA que tenían una mediana de supervivencia de 98 meses (p<0,01).
Resultados similares obtuvieron Ulger et al.21 en 2002, en su serie de 92 pacientes con carcinoma de pulmón en cualquier estadio y tipo histológico (incluido el microcítico).
Por el contrario, otros artículos, como el de Gwin et al.22, publicado en 1994, y los de Rice et al.18 y Dresler et al.17, publicados en 1995, no encontraron relación entre el pronóstico y la pérdida de expresión del antígeno del GSA.
Matsumoto et al.24 encontraron que la pérdida de la expresión de los antígenos del grupo sanguíneo ABH en el cáncer de pulmón se correlacionaba con un mayor potencial metastásico, fundamentalmente con la recurrencia por metástasis hematógenas a distancia. Ichikawa et al.25,26, en estudios experimentales con líneas celulares de carcinoma de colon humano, encontraron una menor movilidad de las células que expresan dichos antígenos (fundamentalmente el antígeno A), lo que podría explicar la mayor capacidad metastásica de las células que han perdido la expresión de los mismos.
Nuestro estudio se ha centrado en determinar el valor pronóstico de la pérdida de la expresión del antígeno del GSA en pacientes con CNMP en estadio I patológico, debido a que en un estudio de determinación de factores pronósticos los estadios iniciales son los que menos están influidos por otros elementos cuya repercusión sobre la supervivencia es de sobra conocida (afectación ganglionar, metástasis a distancia, etc.). Además, se han reestadificado los pacientes según la nueva clasificación TNM de 2009 de la UICC y el AJCC3,4, que es más restrictiva en la definición del estadio I, ya que se eliminan los pacientes con tumores mayores de 5cm. Por otro lado, solo se han incluido pacientes con CNMP, y ello por el hecho de que el carcinoma microcítico tiene un comportamiento biológico y un pronóstico muy diferente. Por último, se han excluido los pacientes que recibieron tratamiento adyuvante o de inducción, con el fin de evitar la influencia sobre la supervivencia que el tratamiento complementario conlleva y que podría añadir un factor de confusión a nuestros resultados y conclusiones.
El haber realizado un estudio retrospectivo, multicéntrico, con amplios periodos de recogida de datos diferentes entre los 3 hospitales participantes y del que se han excluido los casos perdidos, podría limitar en cierta medida la validez de nuestros resultados si los comparáramos con los de un hipotético estudio prospectivo y aleatorizado. Sin embargo, los estrictos criterios de selección de la muestra descritos anteriormente nos han permitido identificar un grupo homogéneo de pacientes con escasa variabilidad en los principales factores pronósticos clínicos y anatómicos. De este modo, el análisis del valor pronóstico de la pérdida de la expresión del histoantígeno del grupo sanguíneo A en los CNMP en estadio I patológico no se ha visto alterado por otros factores con influencia conocida sobre la supervivencia. Por otro lado, el hecho de realizar un estudio multicéntrico nos ha servido para conseguir la serie de pacientes más amplia y con el mayor seguimiento medio (>70 meses) publicada en la literatura sobre el valor pronóstico de la pérdida de la expresión del antígeno del GSA en el cáncer de pulmón, lo que da una gran consistencia a nuestros resultados estadísticos.
Al analizar la supervivencia a los 5 años en función de la pérdida de la expresión tumoral del antígeno del GSA estratificando según el estadio solo se alcanzó la significación estadística en el caso del estadio IA (p=0,038), probablemente por las sucesivas subdivisiones de la muestra.
El hecho más relevante se encontró al analizar la supervivencia a los 5 años en función de la expresión tumoral del antígeno del GSA estratificando según el tipo histológico, ya que los pacientes con adenocarcinoma que perdían la expresión del antígeno del GSA tenían un pronóstico peor, con una p estadísticamente muy significativa (p=0,003). Después de haber realizado una búsqueda bibliográfica en PubMed, encontramos que este hecho únicamente había sido descrito por Moldvay et al.27. Estos autores, en su estudio sobre factores pronósticos del CNMP resecado quirúrgicamente, hallaron que en los adenocarcinomas eran frecuentes las deleciones del cromosoma 9, donde se localizan los alelos A y B, lo que provoca la acumulación de sus precursores fucosilados que sirven como presentadores de ligandos a receptores de adhesión como la E-selectina. Todo esto promueve la capacidad de las células tumorales de interactuar con plaquetas activadas, leucocitos y células endoteliales y, por tanto, facilita su diseminación metastásica.
El análisis multivariable mostró que la pérdida de la expresión tumoral del antígeno del GSA es un factor pronóstico desfavorable. Al igual que otros autores6 y que los resultados publicados recientemente por nuestro grupo en esta revista19, en el análisis multivariable también encontramos que el sexo masculino y la edad mayor de 70 años eran factores pronósticos adversos.
En resumen, nuestro trabajo representa el estudio multicéntrico con el mayor número de pacientes descrito en la literatura sobre la función protectora que supone mantener la expresión del antígeno del GSA en el CNMP en estadio I patológico, fundamentalmente en el tipo histológico adenocarcinoma. Esto podría estar relacionado con el menor potencial metastásico de las células tumorales que mantienen la expresión del antígeno del GSA por inhibición de su motilidad, aunque todavía se desconocen los mecanismos biomoleculares responsables.
Conflicto de interesesLos autores comunicamos la inexistencia de cualquier relación con personas o entidades públicas o privadas susceptible de generar un potencial conflicto de intereses, ya sea en relación a intereses económicos concretos como a implicaciones laborales, personales o profesionales tales como labores de contratación, consultoría, inversión, financiación de la investigación, relación familiar, etc., pasadas o presentes, según las normas del Comité Internacional de Editores de Revistas Médicas.