El Ying Yang 1 (YY1) es un factor de transcripción represor que inhibe la expresión génica muscular y la miogénesis. Este factor no se ha investigado previamente este factor no se ha investigado en el músculo esquelético de pacientes con enfermedad pulmonar obstructiva crónica (EPOC). Los objetivos del presente estudio fueron investigar la expresión de YY1 y su localización en el músculo cuádriceps de pacientes con EPOC, comparado con individuos control sanos, emparejados por edad, y examinar la relación entre la expresión y localización de YY1 en las áreas transversales (AT) de las fibras musculares del cuádriceps en pacientes con EPOC.
Pacientes y métodosSe sometió a 15 pacientes con EPOC y a 8 individuos de control, emparejados por edad, a valoraciones de la función pulmonar y del cuádriceps y a una biopsia percutánea de este músculo. Mediante inmunofluorescencia se determinó el AT de las fibras musculares del cuádriceps las proporciones de fibras y localización de YY1. YY1 se inmunoprecipitó a partir del músculo y sus niveles se evaluaron mediante inmunotransferencia.
ResultadosLos niveles de YY1 se correlacionaron inversamente con el AT de las fibras de tipo IIx y de tipo I en pacientes e individuos de control, aunque los niveles de YY1 no fueron significativamente diferentes entre ambos grupos. En los pacientes, pero no en los individuos control, se demostró la localización nuclear de YY1.
ConclusiónLa expresión de YY1 se asocia a un AT más pequeña de las fibras del cuádriceps en pacientes con EPOC, en cuyo músculo también se observa una localización nuclear del factor, a diferencia de los individuos control. La regulación de YY1 parece alterada en la EPOC y podría estar implicada en la atrofia muscular relacionada con la enfermedad.
Yin Yang 1 (YY1) is a transcriptional repressor that inhibits muscle gene expression and myogenesis. YY1 has not previously been investigated in the skeletal muscle of patients with COPD. The aims of this study were to investigate YY1 expression and localisation in the quadriceps muscle of COPD patients compared to healthy age-matched controls, and examine the relationship between YY1 expression and localisation and quadriceps muscle fibre cross-sectional area (CSA) in COPD patients.
Patients and methods15 COPD patients and 8 age-matched controls underwent lung and quadriceps function assessments and a percutaneous quadriceps biopsy. Quadriceps muscle fibre CSA and fibre proportions and YY1 localisation were determined by immunofluorescence. YY1 was immunoprecipitated from muscle and YY1 levels assessed by western blotting.
ResultsYY1 levels were inversely correlated with type IIx and type I fibre CSA in patients and controls, though YY1 levels were not significantly different between the groups. Nuclear localisation of YY1 was demonstrated in the patients but not in controls.
ConclusionYY1 expression is associated with smaller quadriceps fibre CSA in COPD and nuclear localisation of YY1 was found in muscle of patients but not controls. Regulation of YY1 appears altered in COPD and may be implicated in COPD-related muscle atrophy.
La atrofia y debilidad de los músculos periféricos son factores pronósticos negativos en la enfermedad pulmonar obstructiva crónica (EPOC)1,2. Para mantener la masa muscular, es necesaria una regeneración del músculo esquelético3 y, a partir de modelos animales de EPOC, hay pruebas de que la regeneración muscular esquelética puede estar deteriorada como consecuencia de la inflamación sistémica, lo que contribuye a la atrofia muscular4. No se conocen por completo los mecanismos moleculares que pueden traducirse en un deterioro de la miogénesis en la EPOC.
Ying Yang 1 (YY1) es un factor de transcripción que reprime la miogénesis y que previamente no se ha investigado en el músculo de pacientes con EPOC ni, hasta lo que conocen los autores, en el músculo esquelético de adultos sanos. No obstante, es conocido que su expresión aumenta en el tejido pulmonar de pacientes con EPOC, comparado con individuos control5. YY1 suprime la diferenciación muscular y la transcripción génica del músculo esquelético, como la alfa actina esquelética6 y la creatincinasa muscular7, uniéndose a los promotores pertinentes y bloqueando la unión de un activador transcripcional, el factor de respuesta sérica8. Por ejemplo, la activación de la vía del factor nuclear kappa B (NF-κB) por el factor alfa de necrosis tumoral (TNF-α), puede inhibir la regeneración muscular3 a través de un aumento de la expresión de YY19. La localización de YY1, al igual que su expresión, afecta a su actividad. Cuando YY1 se limita al citoplasma de las células musculares, es inactivo, lo que permite que se produzcan la diferenciación y síntesis de las proteínas contráctiles. YY1 se activa por el transporte hasta el núcleo, por ejemplo como respuesta a la presencia de actina despolimerizada8.
Hay como mínimo dos mecanismos por los que en la EPOC podría aumentar la actividad de YY1 en el músculo. En primer lugar, los pacientes con EPOC y consunción muscular pueden presentar un aumento de la unión de ADN-NF-κB en el músculo10 y, por lo tanto, una mayor expresión de YY19. La activación de NF-κB en el cuádriceps de pacientes con EPOC podría ser consecuencia de la estimulación secundaria al aumento de TNF-α en sangre11 o en el músculo, aunque, en pacientes, comparado con individuos control, se ha descrito una disminución de los valores de TNF-α en el músculo cuádriceps12, en comparación con los hallazgos en los músculos intercostales13. Dado que el TNF-α también puede estimular la activación de células satélite a través de la activación del factor de respuesta sérico14, su disminución en músculo podría inhibir la regeneración muscular independientemente de YY1. En segundo lugar, en el músculo de pacientes con EPOC, la actividad de YY1 podría incrementarse por el aumento del transporte nuclear de YY1, en presencia de un aumento de la actina despolimerizada como consecuencia de la degradación acelerada de proteínas a través de la vía ubicuitina-proteasoma8,15. Por lo tanto, la hipótesis del presente estudio fue que la disregulación de la señalización YY1 está implicada en la atrofia del cuádriceps de pacientes con EPOC. Investigamos la expresión y localización de YY1 en el músculo cuádriceps de un pequeño grupo de pacientes con EPOC y de individuos de control, emparejados para la edad, y examinamos la relación entre la expresión y localización de YY1 y el AT de las fibras del cuádriceps.
Individuos y métodosIndividuosA partir del servicio respiratorio se incluyeron 15 pacientes con EPOC (estadio de la iniciativa Global Initiative for Chronic Obstructive Lung Disease [GOLD] II [n=4], III [n=4] y IV [n=7]). Los criterios de exclusión fueron insuficiencia cardíaca, renal o hepática o una enfermedad inflamatoria sistémica, metabólica o neuromuscular o una exacerbación moderada/grave (es decir, con necesidad de antibióticos, esteroides orales u hospitalización) en las 4 semanas previas. Mediante un anuncio se reclutaron 8 individuos control, sanos. Los individuos dieron su consentimiento informado y el estudio fue aprobado por el comité de investigación del Royal Brompton y Harefield NHS Trust y el Ealing and West London Mental Health Trust.
Determinaciones fisiológicas y biopsia del cuádricepsDe acuerdo con las guías de la American Thoracic/European Respiratory Society, se determinaron la espirometría posbroncodilatador16, los volúmenes pulmonares con pletismografía17, la capacidad de difusión del monóxido de carbono18 y la gasometría arterial se examinó en una muestra de sangre arterializada, obtenida del lóbulo de la oreja. La masa magra se determinó mediante impedancia bioeléctrica (dispositivo Bodystat® 1500, Bodystat, Reino Unido)19 y se corrigió para la estatura para derivar el índice de masa magra. La actividad física se determinó con un acelerómetro triaxial Dynaport® ADL3; McRoberts BV, Países Bajos), que los pacientes utilizaron durante 2 días, 12 horas cada día, durante una actividad normal. El tiempo de locomoción media se calculó como se ha descrito previamente20. La fuerza del cuádriceps (pierna derecha) se evaluó con la contracción voluntaria máxima isométrica, en decúbito supino, basada en el método de Edwards21. La biopsia percutánea con aguja en el músculo vasto lateral derecho se efectuó con anestesia local utilizando la técnica de Bergstrom22. Las muestras para el análisis de ácido ribonucleico y proteínas se congelaron de inmediato en nitrógeno líquido, al mismo tiempo que las muestras para histología se introdujeron en isopentano preenfriado durante 15 seg antes de congelarse en nitrógeno líquido, y acto seguido, se almacenaron a –80°C.
Análisis de la biopsia muscularNo se dispuso de tejido suficiente a partir de todos los individuos para efectuar los análisis y por esta razón para cada análisis se usó un subgrupo de muestras.
Detección inmunofluorescente de Yin Yang 1Los cortes congelados de 10 μm de 10 pacientes y 8 individuos de control se fijaron en una solución de formaldehído al 10%, se lavaron en Triton X-100 al 0,1% en una solución salina neutralizada con fosfato (PBS) y se bloquearon con albúmina de suero bovino (BSA) al 5% en PBS, antes de incubación con un anticuerpo de conejo anti-YY1 (dilución 1:400, sc-281; Santa Cruz Biotechnology, Estados Unidos) y un anticuerpo murino anti-cadena pesada de la miosina de contracción rápida (MYSN02, dilución 1:200, Abcam, Reino Unido) en BSA al 3% en PBS durante toda la noche a 4°C. Tras una incubación de 1 h a temperatura ambiente en la oscuridad con anticuerpos secundarios marcados con fluorescencia (A11008 Invitrogen y A11005 Invitrogen, dilución 1:250 en PBS), los cortes se trataron con diaminodifenilindol (DAPI). Las imágenes (dos campos por muestra, dos cortes por individuo) se obtuvieron utilizando un microscopio de campo ancho Zeiss Axiovert con una lente de 10× y un programa informático Improvision Volocity. Mediante un microscopio Leica SP2 se obtuvieron imágenes confocales con una lente de inmersión en aceite 63x y se analizaron con un programa informático LCS Lite (Leica Microsystems, Alemania).
Cuantificación de la proteína Yin Yang 1YY1 no es abundante en el músculo esquelético de adultos y, por consiguiente, antes de la inmunotransferencia fue necesaria la inmunoprecipitación. A partir de nueve pacientes y siete individuos control, para este análisis estuvieron disponibles 3-6 mg de proteína.
Inmunoprecipitación de Yin Yang 1Se incubaron 3-6 mg de proteína homogeneizada en solución con Nonidet P40, cócteles de inhibidor de la proteasa y de inhibidor de la fosfatasa (Sigma, Poole Dorset, Reino Unido) en hielo durante 30 min con 30 μl de cuentas Protein G-Sephorose. Después de 2 min de centrifugación (8.000 rpm), el sobrenadante se incubó durante 1 h en hielo con 1 μg de anticuerpo de conejo anti-YY1 (sc-281, Santa Cruz Biotechnologies, Estados Unidos). Para cada muestra se añadieron otros 30 μl de cuentas de Protein G-Sephorose y se reincubaron en hielo durante 1 h. Las muestras se centrifugaron de nuevo y se desechó el sobrenadante. Las cuentas se lavaron en Nonidet P40 y se hirvieron con 30 μl del tampón de la muestra (tampón de carga y 2-mercaptoetanol) durante 5 min a 100°C. Este proceso se optimizó para garantizar que el sobrenadante no contendría una cantidad detectable de YY1 en la inmunotransferencia.
Análisis de inmunotransferenciaLas muestras se analizaron utilizando electroforesis en gel de poliacrilamida con dodecilsulfato (SDS/PAGE) (gel al 10%) y una técnica de inmunotransferencia semiseca (LKB). Tras el bloqueo (BSA al 5% en PBS), las membranas se incubaron con un anticuerpo de ratón anti-YY1 (ab58066, dilución 1:200, Abcam, Reino Unido) en BSA al 3% en PBS durante toda la noche a 4°C, y acto seguido, con un anticuerpo IgG murino unido a peroxidasa de rábano picante (ab 6728, Abcam, Reino Unido, 1:5.000 en BSA al 3% en PBS) durante 1 h a temperatura ambiente. Las proteínas se visualizaron mediante Supersignal (Pierce, Rockford, IL, Estados Unidos), determinándose la densidad de la banda con un análisis de densitometría 1D (AIDA, Raytek, Sheffield, Reino Unido) y se normalizaron para la cantidad de proteínas usadas en la inmunoprecipitación.
Determinación del área transversal de las fibras muscularesA partir de todos los individuos, los cortes musculares transversales congelados de 10 μm se incubaron con anticuerpos primarios para la miosina tipo I, miosina tipo IIa y laminina (A4.840 y N2.261 Developmental Studies Hybridoma Bank, University of Iowa, Estados Unidos, y L-9393 Sigma, Zwijndrecht, Países Bajos, respectivamente) seguido de anticuerpos secundarios marcados con fluorescencia (A-21121, A-21426 y A-11069, Invitrogen)23. La señal de epifluorescencia se registró utilizando un filtro de excitación Texas Red (540-580 nm) para la miosina tipo I, un filtro de excitación FITC (465-495 nm) para la miosina de tipo IIa y un filtro de excitación UV DAPI (340-380 nm) para la laminina utilizando un microscopio Nikon Eclipse 800. Las fibras se clasificaron en tipo I, IIa, IIx (sin tinción) e híbridas I/IIa (tinción dual) y se utilizó el borde de laminina de las fibras para calcular el AT de cada fibra (y a partir de ésta, el AT mediana para cada tipo de fibra) y las proporciones de fibras utilizando el programa estadístico Lucia 4.81 (Nikon, Japón)24. Para cada individuo se analizó una mediana de 207 fibras con un mínimo de 103 fibras.
Cuantificación de los niveles de ARNm de factor de necrosis tumoral αLos transcritos de ARNm de TNF-α se determinaron mediante reacción en cadena de la polimerasa cuantitativa, en tiempo real, utilizando SYBR® Green PCR Master Mix (Applied Biosystems) en un 7900HT Fast Real-Time PCR System (Applied Biosystems). Los transcritos se normalizaron hasta un factor geNorm derivado de dos genes internos, la fosfoproteína ribosómica ácida (RPLPO) y la microglobulina beta-2 (β2M), según lo descrito previamente25. Más adelante se muestran las secuencias de los cebadores (iniciadores):
Análisis estadísticoLos datos no tenían una distribución normal (de acuerdo con el histograma y la prueba de la simetría), por lo que se describen como medianas (percentil 25 y percentil 75). Las diferencias de grupo en las variables continuas se analizaron con la prueba de la U de Mann Whitney, mientras que se usó la prueba exacta de Fisher para probar las diferencias de grupo en las variables categóricas. Se calculó el coeficiente de correlación de rangos de Spearman (ρ) para determinar la relación entre las variables (Statview 1.0, Abacus Instruments). Para definir la significación estadística se utilizó un valor de p bilateral (dos colas) ≤ 0,05.
ResultadosEn la tabla 1 se muestran los datos fisiológicos de los pacientes y los controles. Como era de esperar, los pacientes presentaron un deterioro de la función pulmonar y una disminución de la fuerza del cuádriceps, en comparación con los individuos control [contracción voluntaria máxima 22 (17,34) kg frente a 34 (28,42) kg en individuos control, p=0,03].
Características clínicas de los pacientes y los individuos de control
| Pacientes con EPOC (n=15) | Individuos control (n=8) | |
|---|---|---|
| Edad (años) | 69 (63,75) | 69 (65,76) |
| Sexo | 53% de hombres | 50% de hombres |
| Tabaquismo | 2 actual, 13 ex fumadores | 8 ex fumadores, 2 no fumadores |
| Antecedentes de tabaquismo (paquetes/año) | 45 (30,75)* | 7 (1,14) |
| VEMS (l) | 0,86 (0,59, 1,05)* | 2,92 (2,53, 2,98) |
| VEMS (% del valor de referencia) | 33 (22,54)* | 109 (105,112) |
| TLCO (% del valor de referencia) | 36 (25,62)* | 89 (81,99) |
| PaO2 (kPa) | 9,8 (8,0, 10,4) | 10,4 (8,7, 11,4) |
| Índice de masa corporal (kg/m2) | 22,9 (20,7, 26,2) | 24,8 (21,0, 26,7) |
| Índice de masa corporal magra (kg/m2) | 16,2 (14,3, 18,6) | 15,8 (14,5, 19,5) |
| CVM del cuádriceps (kg) | 22 (17,34)† | 34 (28,42) |
| Tiempo de locomoción (min/12 h) | 57 (21,75) | 61 (56,159) |
Los valores son medianas (percentil 25 y percentil 75).
*p<0,0001; †p=0,03 para las comparaciones de grupo (analizadas con la prueba de la U de Mann Whitney).
CVM: contracción voluntaria máxima; EPOC: enfermedad pulmonar obstructiva crónica; PaO2: presión arterial parcial de oxígeno; TLCO: capacidad de difusión de monóxido de carbono; VEMS: volumen espiratorio máximo en el primer segundo.
El AT en las fibras de tipo IIx disminuyó y el cociente fibras de tipo I: fibras de tipo II disminuyó en pacientes con EPOC en comparación con individuos control.
En los pacientes se detectó un AT significativamente más pequeña en las fibras de tipo IIx que en individuos control [3.439 (2.348, 3.739) μm2 frente a 4.628 (4.087, 6.303) μm2 respectivamente, p=0,05], pero no hubo una diferencia significativa en el AT de los otros tipos de fibras entre grupos, como se ha descrito previamente26. En pacientes se detectó una proporción significativamente menor de fibras de tipo I y una mayor proporción de fibras de tipo IIa que en individuos control [34 (14, 39) % frente a 52 (47, 63) % y 60 (49, 70) % frente a 40 (35, 46) %, respectivamente), como se ha descrito previamente27 (tabla 2).
Niveles de YY1, HDAC 5, y HDAC 5 unida a YY1 y AT mediana de las fibras de tipo I, I/IIa, IIa y IIx en el cuádriceps de pacientes con EPOC e individuos de control
| Pacientes con EPOC (n=15) | Individuos de control (n=8) | |
|---|---|---|
| YY1 (UA/mg de proteína) | 3,25 (1,95, 7,17) (n=9) | 3,84 (2,18, 6,01) (n=7) |
| Niveles de ARNm-TNF-α (UA) | 0,08 (0,03, 0,11) (n=15) | 0,04 (0,03, 0,05) (n=8) |
| AT fibra tipo I (μm2) | 5.352 (4.151, 6.783) (n=15) | 5.644 (4.111, 7.411) (n=8) |
| AT fibra tipo I/IIa (μm2) | 4.971 (3.292, 7.309) (n=15) | 5.754 (5.005, 5.956) (n=3) |
| AT fibra tipo IIa (μm2) | 4.221 (2.996, 5.170) (n=15) | 3.314 (3.002, 5.408) (n=15) |
| AT fibra tipo IIx (μm2) | 3.439 (2.348, 3.739)† (n=14) | 5.015 (3.618, 6.303) (n=8) |
| Porcentaje de fibras tipo I | 34 (11, 38)* (n=15) | 52 (47, 63) (n=8) |
| Porcentaje de fibras tipo I/IIa | 3 (1, 6)* (n=15) | 0 (0, 4) (n=8) |
| Porcentaje de fibras tipo IIa | 60 (52, 70)* (n=15) | 40 (35, 46) (n=8) |
| Porcentaje de fibras tipo IIx | 3 (1, 16)* (n=15) | 1 (0,4) (n=8) |
Los valores son medianas (percentil 25, percentil 75). Los porcentajes de fibras en cada individuo ascienden al 100% (la suma de las medianas en cada grupo no necesariamente es igual al 100% debido a la varianza en torno a la mediana. Los niveles para ARNm se normalizan para los transcritos de RPLPO (gen interno).
*p<0,005; †p<0,05 para las comparaciones de grupo (analizadas con la prueba de la U de Mann Whitney).
AT: área transversal; HDAC: histona desacetilasa; RPLPO: fosfoproteína ribosómica ácida; TNF-α: factor de necrosis tumoral alfa; UA: unidades arbitrarias; YY1: Yin Yang 1.
Los niveles de YY1 en cuádriceps se asociaron con una disminución del AT de las fibras musculares en la EPOC.
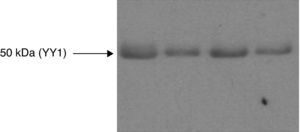
La cantidad de proteína YY1 en el cuádriceps no fue significativamente diferente en pacientes en comparación con individuos control (fig. 1, tabla 2). En pacientes e individuos control, los niveles de proteína YY1 se correlacionaron inversamente con el AT de las fibras de tipo IIx (ρ=–0,83, p<0,0001), al igual que con el AT de las fibras de tipo I (ρ=–0,59, p=0,017) y también se observó una tendencia hacia una correlación negativa con el AT de las fibras de tipo IIa (ρ=–0,43, p=0,09) (fig. 2). Sólo en el grupo de pacientes se identificó una correlación entre los niveles de YY1 y en el músculo el AT de las fibras de tipo IIx (ρ=–0,88, p=0,002). Los niveles de YY1 en músculo no se correlacionaron con el volumen espiratorio máximo en el primer segundo o la capacidad de difusión de CO2 (TLCO) como porcentaje del valor de referencia, contracción voluntaria máxima del cuádriceps o el índice de masa magra en pacientes e individuos control (p=0,69, 0,43, 0,94 y 0,21, respectivamente) o sólo se identificó correlación en el grupo de pacientes.
Análisis de inmunotransferencia para YY1 a partir del músculo cuádriceps de pacientes con EPOC e individuos control, sanos. Inmunotransferencia representativa de YY1 en muestras de músculo de un individuo control (izquierda) y tres pacientes con EPOC (derecha), sometidos a inmunoprecipitación utilizando un anticuerpo anti-YY1. Las bandas se observan en posición 50 kDa. No se identificaron diferencias estadísticamente significativas de los niveles de proteína YY1 en el músculo de los pacientes comparado con el de individuos control.
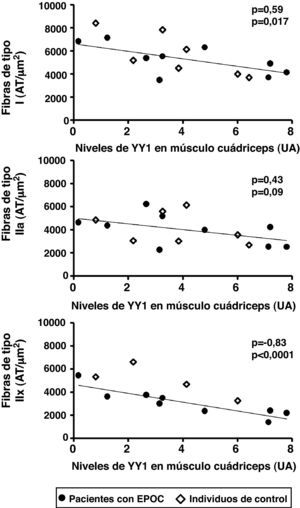
Diagramas de puntos de los niveles de proteína YY1 y área transversal (AT) de las fibras de tipo I, IIa y IIx en el cuádriceps de pacientes con EPOC e individuos control, sanos.
Hubo correlaciones negativas entre los niveles de proteína YY1 y el AT de las fibras de tipo I y IIx, y una tendencia hacia una correlación negativa entre los niveles del factor y el AT de las fibras de tipo IIa cuando se combinaron los pacientes y los individuos control (ρ=–0,83, p<0,0001; ρ=–0,59, p=0,017 y ρ=–0,43, p=0,09, respectivamente), y una correlación negativa entre el nivel de YY1 y el AT de las fibras de tipo IIx sólo detectada en pacientes (ρ=–0,88, p=0,002).
Los niveles de ARNm de TNF-α muscular fueron más altos en pacientes que en individuos control (0,08 [0,03, 0,1] unidades arbitrarias [UA] frente a 0,04 [0,03, 0,05] UA, p=0,05). Los transcritos de ARNm de TNF-α y los niveles de YY1 no se correlacionaron en pacientes e individuos control (p=0,38) o en los pacientes solos.
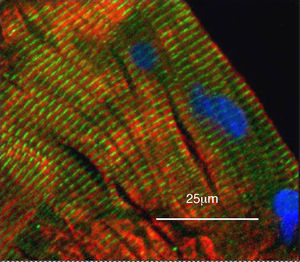
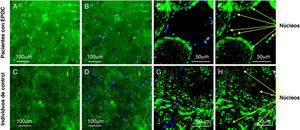
Presencia de localización nuclear de Yin Yang 1 en el músculo de un subgrupo de pacientes con enfermedad pulmonar obstructiva crónica pero no en individuos controlYY1 estuvo ausente del núcleo pero presente en el citoplasma en los cortes de cuádriceps de los individuos de control, sanos (fig. 3 y fig. 4C, D, G, H). YY1 en el citoplasma se alineó con los sarcómeros, pero no se colocalizó con la miosina (fig. 3).
Imagen con microscopio de campo ancho de un corte longitudinal de músculo cuádriceps de un individuo control, sano, demostrándose la localización de YY1 en relación con los núcleos musculares mediante inmunohistoquímica. El músculo se tiñó para YY1 (verde), la cadena pesada de la miosina rápida (rojo) y los núcleos utilizando 4’,6-diamidino-2-fenilindol (azul). Se observa la tinción de YY1 a lo largo de los sarcómeros, no colocalizada con la miosina, y la ausencia de los núcleos.
Imágenes en el microscopio de cortes musculares de cuádriceps de pacientes con EPOC e individuos ontrol, demostrándose en los miotúbulos la localización de YY1 con inmunohistoquímica en relación con los núcleos musculares. A-D: imágenes con microscopio de campo ancho y E-H: imágenes con microscopio confocal de cortes transversales de cuádriceps que demuestran la tinción de YY1 en verde y para los núcleos con 4’,6-diamidino-2-fenilindol en azul (B, D, E y G) y los mismos cortes que muestran tinción para YY1 sólo en verde (A, C, F y H). A, B, E y F muestran los cortes de un paciente en el que se identificó el patrón anómalo de tinción del factor tanto en el núcleo como en el citoplasma. C, D, G y H corresponden a un individuo de control en el que se demostró una tinción exclusivamente citoplasmática de YY1.
En ninguno de los individuos control, pero sí en 5 de los 10 pacientes se demostró tinción YY1 en la región nuclear; esta diferencia entre grupos fue estadísticamente significativa (prueba exacta de Fisher, p=0,04). Comparado con 6 de los 8 individuos control, sólo en 2 de los 10 pacientes se demostró una distribución de YY1 exclusivamente citoplasmática, que, una vez más, fue estadísticamente significativa (prueba exacta de Fisher, p=0,05). No se identificó una diferencia significativa entre pacientes con localización nuclear de YY1 y pacientes sin ella por lo que respecta a la función muscular o pulmonar, AT de las fibras del cuádriceps o niveles de proteína YY1.
DiscusiónDescribimos un nuevo hallazgo, es decir, que el factor de transcripción YY1, un represor de la expresión génica específica de músculo y de la miogénesis, se expresa en una proporción inversa al AT de las fibras de tipo IIx y tipo I en el músculo cuádriceps de pacientes con EPOC. En una proporción significativa de estos pacientes fue evidente la localización nuclear del factor, lo que contrasta con la distribución en el músculo de adultos sanos.
Crítica del métodoNaturalmente, el presente estudio adolece de limitaciones. En primer lugar, el tamaño de la muestra fue pequeño y las asociaciones detectadas tuvieron que distinguirse, por lo que, es posible que, debido a la falta de potencia, no se identificaran otras asociaciones o diferencias de grupo. Los individuos control incluidos en el presente estudio se caracterizaron por un índice de masa magra relativamente bajo y una amplia varianza en su grado de actividad física, para lo que no hay una explicación clara, lo que aumenta el umbral de la significación estadística de las diferencias de grupo. Aunque el estudio de pacientes en estadio II, III y IV de la iniciativa GOLD tendría que haber facilitado el hallazgo de correlaciones entre la función muscular y pulmonar y los niveles de YY1, porque no sería de esperar que los datos se agruparan, la utilización de pacientes en un estadio IV exclusivo podría haber aumentado al máximo la probabilidad de encontrar una diferencia significativa en la expresión de YY1 entre pacientes e individuos de control. En segundo lugar, el diseño observacional no permite la extracción de conclusiones acerca del efecto de las diferencias en YY1 sobre la estructura y función muscular, lo que meramente destaca una asociación entre el aumento de expresión del factor y el tamaño más pequeño de las fibras y entre la localización nuclear del factor y la presencia de EPOC y una fuerza menor del músculo cuádriceps que en individuos control. Por último, utilizamos la localización y expresión del factor como variable indirecta de la actividad porque YY1 es activado por transporte desde el citoplasma hasta el núcleo. Podrían haber corroborado nuestros hallazgos la cuantificación de YY1 unido a ADN (inmunoprecipitación de la cromatina, una técnica no publicada previamente sobre el uso en músculo del ser humano) o la cuantificación de YY1 capaz de unión a ADN (por ejemplo, mediante análisis electroforético del cambio de movilidad).
También podría argumentarse que el factor YY1 detectado en los núcleos no está presente en la periferia de las miofibrillas, sino en las células satélite, latentes. Sin embargo, consideramos que esto es improbable ya que las células satélite sólo representan el 2-5% de los núcleos del músculo28. Incluso suponiendo un aumento masivo de la población de células satélite en el tejido de los pacientes, el número de núcleos que se tiñeron para el factor supera considerablemente el número que podrían explicar las células satélite. Además, en las muestras del presente estudio, la ausencia de núcleos centralizados sugiere una activación limitada de las células satélite en el período de tiempo en torno a la obtención de las muestras.
Significación de los hallazgosLa implicación de una potente correlación inversa entre los niveles de factor YY1 y el tamaño de las fibras es que YY1 podría participar en el mecanismo de la atrofia de las fibras, en particular dado que la relación es más potente con el AT de las fibras de tipo IIx y estas fibras parecen ser el tipo que más se atrofia en la EPOC26. Sin embargo, esta hipótesis requeriría una investigación adicional, por ejemplo, examinando el efecto en el músculo esquelético de ratones adultos knockout o knockdown con enfisema inducido por el humo del tabaco u otros medios.
El hallazgo de que los pacientes con una localización nuclear del factor no necesariamente poseen niveles más altos puede explicarse por el hecho de que su localización y expresión pueden regularse de manera independiente. Es posible que los pacientes con una mayor expresión de YY1 y un tamaño más pequeño de las fibras se caractericen por mayores niveles de activación de NF-κB en el músculo, mientras que en otros una mayor reserva de actina despolimerizada daría lugar a una acumulación nuclear del factor sin un aumento de su expresión. No obstante, no encontramos una correlación entre los valores locales de TNF-α e YY1 en el músculo de los pacientes, lo que respalda la sugerencia de que los niveles del factor están determinados principalmente por TNF-α local que activaría el factor NF-κB.
En conclusión, describimos el nuevo hallazgo de que YY1, un factor de transcripción de represión de la expresión génica específica de músculo y la miogénesis, se expresa asociado a una disminución del AT de las fibras de tipo IIx y tipo I del músculo cuádriceps en la EPOC. YY1 también se localiza en los núcleos del cuádriceps de pacientes con EPOC, en comparación con individuos control, sanos, emparejados por edad. Especulamos que la mayor actividad de YY1 podría estar implicada en el deterioro de la regeneración del músculo esquelético y la atrofia de las fibras musculares en la EPOC.
Conflicto de interesesS. A. Natanek (nacida en Sathyapala) recibe financiación a través de una Wellcome Trust Clinical Research Training Fellowship y previamente recibió financiación de GlaxoSmithKline. G. S. Marsh y J. Riddoch-Contreras recibieron financiación a través de una beca educativa al Imperial College de GlaxoSmithKline. W. D-C. Man recibe funanciación del National Institute for Health Research Clinician Scientist Award. GlaxoSmithKline no desempeñó ningún papel en la obtención de los datos o la preparación del manuscrito. La NIHR Respiratory Biomedical Research Unit del Royal Brompton Hospital and Imperial College contribuyen a una parte del salario de M. I. Polkey.
AgradecimientosDamos las gracias a Derek Cramer y al Lung Function Department del Royal Brompton Hospital por la ejecución de las pruebas de función pulmonar; al Profesor David Hansell y el CT Department del Royal Brompton Hospital por la realización de los cortes gruesos; a Kathleen Daenen del University Hospital de Maastricht por el examen de los cortes congelados; a Gert Schaart y Lex Verdijk de la Maastricht University por su ayuda con la inmunofluorescencia para la detección del tipo y el tamaño de las fibras y a Harry Gosker y Ramon Langen de la Maastricht University por sus comentarios sobre el manuscrito.