El seudotumor inflamatorio es una patología relativamente poco frecuente de etiología incierta, generalmente considerada de origen reactivo. Puede observarse en diferentes localizaciones como masas únicas o múltiples. La intrapulmonar es una de sus posibles formas de presentación.
A pesar de su baja frecuencia, esta patología debe tenerse en cuenta a la hora de realizar el diagnóstico diferencial de nódulos pulmonares. De otro modo, los resultados histológicos y de las pruebas de imagen pueden llegar a ser confusos. Además, presenta una baja malignidad con buena respuesta al tratamiento quirúrgico y en menor medida al farmacológico.
Presentamos una revisión bibliográfica de esta patología basándonos en dos casos observados en nuestro hospital. Ambos pacientes comenzaron con cuadros respiratorios inespecíficos y nódulos pulmonares en pruebas de imagen, sospechosos de proceso neoplásico. Tras su estudio exhaustivo se llegó al diagnóstico de seudotumor inflamatorio pulmonar con excelente respuesta al tratamiento usado en cada caso.
Inflammatory pseudotumors are a relatively uncommon pathology of uncertain etiology, generally considered to be reactive in origin. They may be observed in different locations as single or multiple masses. One of the possible forms of presentation is intrapulmonary.
Despite its low frequency, this pathology should be considered in the differential diagnosis of lung nodules, even though the histologic results and the imaging tests can become confusing. In addition, pulmonary inflammatory pseudotumors present a low malignancy with good response to surgical treatment as well as to pharmacological therapy, although to a lesser degree.
We present a bibliographic review of this pathology based on two cases observed in our hospital. Both patients debuted with non-specific respiratory symptoms and lung nodules on imaging studies that were suspicious for neoplastic processes. After an exhaustive study, the diagnosis of pulmonary inflammatory pseudotumor was reached, with excellent responses to the treatment used in each case.
El seudotumor inflamatorio (STI) es una patología poco frecuente de etiología poco conocida, aunque se ha asociado a múltiples factores1,2. Se considera un proceso generalmente reactivo que se caracteriza por un crecimiento irregular de células de carácter inflamatorio: miofibroblastos, células plasmáticas, macrófagos, histiocitos, etc.1,3,4.
Su presentación y su historia natural son muy variables, pudiendo aparecer en el mesenterio, en el retroperitoneo, en la mucosa orofaríngea, etc. En el tórax es poco frecuente; está presente en el 0,04-1,2% de las toracotomías y representa el 0,7% de los tumores pulmonares1,5,6.
Puede resultar un factor de confusión en el diagnóstico diferencial de las masas pulmonares. Además, un diagnóstico precoz redundará en beneficio del paciente al empeorar el pronóstico con la progresión del cuadro. Presentamos dos casos que corresponden a las formas de presentación más habituales de esta patología, totalmente diferentes en sus características y con manejo inicial como neoplasia.
Observación clínicaCaso 1Mujer de 54 años que acudió a urgencias por un cuadro de varios días de evolución consistente en tos, expectoración herrumbrosa, fiebre, dolor torácico y disnea de esfuerzo progresiva. Como antecedentes personales refería frecuentes procesos respiratorios de vías bajas en los últimos años. En la exploración se apreciaron roncus y crepitantes bibasales a la auscultación pulmonar. En el hemograma, leucocitosis de 14,6×109l (rango normal, 4,5,10,5×109l) con neutrofilia. Durante su ingreso fue diagnosticada de hepatopatía crónica por virus B con cirrosis clase B de Child-Pugh, previamente desconocida.
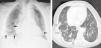
Dada la sospecha de proceso neumónico, se realizó una radiografía simple de tórax (fig. 1) en la que se identificaron múltiples nódulos bibasales, más numerosos en el lado derecho. También se observó una condensación en el lóbulo medio derecho sugestiva de proceso neumónico. Con el tratamiento antibiótico y fisioterapia respiratoria, la paciente presentó mejoría.
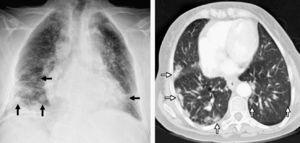
A la izquierda, en la radiografía simple de tórax tras biopsia quirúrgica se aprecian múltiples nódulos bibasales de predominio derecho (flechas negras). A la derecha, en el corte axial de tomografía computarizada (TC) con ventana pulmonar se observan nódulos hiperdensos periféricos bibasales de bordes mal delimitados, de mayor tamaño en el hemitórax derecho (flechas blancas).
Se realizó tomografía computarizada (TC) de tórax de forma programada (fig. 1, derecha), en la que se confirmaron los múltiples nódulos pulmonares bilaterales de bordes bien definidos y no espiculados, distribuidos difusamente por ambos lóbulos con predominio basal y periférico. Existían adenopatías subcarinales, peribronquiales y retroperitoneales de características patológicas. También se confirmó la opacidad con broncograma aéreo en el lóbulo medio derecho de características neumónicas. El diagnóstico de sospecha fue de metástasis hematógena de tumor primario desconocido versus proceso linfoproliferativo.
La fibrobroncoscopia no demostró lesiones intrabronquiales. La biopsia transbronquial dio como resultado infiltrado linfoide polimorfo, sin descartar un proceso linfoproliferativo. La biopsia quirúrgica mostró un infiltrado linfoide heterogéneo sin signos histológicos de malignidad compatibles con STI multifocal. Se remitió una muestra al Centro Nacional de Investigaciones Oncológicas (CNIO), que confirmó el diagnóstico.
Se decidió tratamiento médico con terapia esteroidea, dada la bilateralidad y la extensión de los nódulos. Se observó buena respuesta, con regresión completa de las lesiones en un control 8meses después de la instauración del tratamiento. La paciente persistió libre de lesiones hasta su fallecimiento 7meses más tarde por complicaciones asociadas a la cirrosis.
Caso 2Varón de 25 años que acudió al servicio de urgencias por dolor opresivo en hemitórax derecho que aumentaba con el ejercicio y episodios de tos autolimitada. No presentaba antecedentes personales de interés. La exploración clínica y la analítica fueron anodinas, salvo un nivel de leucocitos en el límite alto de la normalidad sin neutrofilia. La radiografía de tórax (fig. 2) urgente mostró una masa pulmonar derecha homogénea de bordes bien definidos en el lóbulo superior derecho, en contacto con la pleura y asociada a elevación del hemidiafragma ipsilateral.
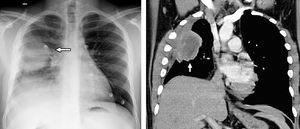
A la izquierda, la radiografía de tórax presenta una masa pulmonar homogénea de bordes bien definidos en el lóbulo superior derecho (flecha blanca), en contacto con la pleura y asociada a pérdida de volumen. A la derecha, en la reconstrucción coronal de tomografía computarizada (TC) con ventana de partes blandas se aprecia la masa bien delimitada con una zona de necrosis central, en contacto con la pleura y que produce el engrosamiento de la misma, así como la pérdida de volumen del hemitórax derecho.
En la TC de tórax (fig. 2, derecha) se observó una masa en el lóbulo superior y medio derechos de 60×43mm de contornos parcialmente definidos con zona de necrosis central, en contacto con ambas cisuras, y pleura que producía engrosamiento de la misma. Presentaba pérdida de volumen del hemitórax derecho y adenopatías hiliares derechas y mediastínicas patológicas. Se realizó biopsia con control por TC, obteniendo como muestra áreas de fibrosis con células plasmáticas y eosinófilos, negativa para malignidad. Ante la duda diagnóstica se decidió exéresis quirúrgica realizando resección transegmentaria.
La anatomía patológica de la pieza posquirúrgica no mostró evidencia de malignidad, observándose fibrosis e intensa inflamación crónica con algunos cambios tipo neumonía organizada y bronquiolitis folicular. El diagnóstico definitivo fue de STI unifocal. Al seguimiento el paciente presentó buena evolución, sin signos de recidiva hasta la actualidad (24 meses tras la cirugía).
DiscusiónEl STI es una entidad poco frecuente, aún en estudio6-8. Ha recibido múltiples denominaciones: tumor miofibroblástico inflamatorio, granuloma de células plasmáticas, fibroxantoma, tumor fibromixoide seudosarcomatoso o proliferación miofibrohistiocítica inflamatoria3,4,6,9,10. No se considera un proceso maligno, aunque este dato es controvertido dado el potencial invasivo que presenta3,7,8. Se han descrito casos de comportamiento agresivo con invasión vascular, infiltración de estructuras adyacentes, destrucción ósea, recurrencia tras cirugía, diseminación metastásica o incluso degeneración sarcomatosa1,6,7,9. Algunos autores lo consideran una neoplasia de bajo grado8,9.
No se conoce con exactitud su etiología. Se lo ha relacionado con una respuesta inflamatoria incontrolada crónica y focal a antígenos o infecciones pulmonares1,2,6,9. Existen tres patrones histológicos de presentación, aunque habitualmente se presenta como una mezcla de ellos con uno predominante: vascular mixoide, células fusiformes compactas o fibroso hipocelular, sin diferencia clínica, radiológica o pronóstica entre ellos7,10.
El STI pulmonar puede darse en un amplio rango de edad, sin predominio de género. Sin embargo es más frecuente en niños y en adultos jóvenes (el 60% de los casos son menores de 40 años)1,3,5,7,11. Es el tumor pulmonar primario más frecuente en niños3,5,6,11. El comportamiento invasivo es más frecuente en la infancia (hasta el 20% de los casos)6.
Es asintomático en el 50-70% de los casos, y se descubre de forma incidental en una prueba de imagen4,5,7,9. En ocasiones los pacientes pueden referir síntomas respiratorios como disnea, dolor torácico, tos o hemoptisis en relación con la localización del STI, y en algunos casos fiebre o pérdida de peso1,2,9,11. Hasta un tercio de los pacientes refieren una historia previa de infecciones de vías respiratorias bajas, pero no se ha demostrado una cronología clara2,3,7,9,11. Las pruebas de laboratorio son normales o con alteraciones inespecíficas9.
En las pruebas de imagen presentan características variables. Suelen aparecer en localizaciones periféricas y en los lóbulos inferiores, y en raras ocasiones son intrabronquiales (10,7-12%)3,4,9,11. Pueden ser multifocales, pero es más frecuente la presentación como masa única (hasta el 87%)3,7-9,11. En la radiología simple de tórax habitualmente se encuentran lesiones redondeadas u ovales de bordes bien definidos y densidad homogénea (lesión en moneda)2,5,11.
En la TC los hallazgos son variables, no específicos. Habitualmente se observan masas de bordes lisos o lobulados bien definidos, con un patrón heterogéneo de realce tras la introducción de contraste3,4,8,9,11. A veces se ha descrito un realce de predominio periférico irregular3. Menos frecuentemente se observan calcificaciones (15%, más frecuentes en niños), necrosis (10%), afectación de la vía aérea (10%, frecuentemente como pólipo), cavitación (5%), cicatriz central y raramente adenopatías (7%) o hemorragia2-4,9,11.
En la tomografía por emisión de positrones (PET) el STI pulmonar suele presentar captación con características tumorales, representando un falso positivo6,12. Esta característica podría ser útil para descartar recidivas o metástasis a distancia una vez confirmado el diagnóstico histológico, pero no existen estudios al respecto. En la resonancia magnética (RM) presenta señal intermedia en secuencias potenciadas en T1, hiperintenso en T2 y realce heterogéneo tras el contraste, si bien no hemos encontrado estudios exhaustivos del STI con esta técnica3,8.
El diagnóstico final suele ser quirúrgico, dada la inespecificidad de los hallazgos y la dificultad de realizar un diagnóstico mediante biopsia transbronquial o transtorácica1,7,9. En el diagnóstico diferencial debemos incluir neoplasias malignas pulmonares y las metástasis. También granuloma y hamartoma (sobre todo cuando presenta calcificaciones), hemangioma, adenoma y secuestro pulmonar. En los STI de presentación endobronquial debemos incluir el carcinoide, el carcinoma mucoepidermoide y el carcinoma adenoide quístico2,3,11.
El tratamiento de primera elección es la resección quirúrgica de las lesiones con un adecuado margen de seguridad1,2,6-8,10. Se opta por lobectomía/neumonectomía en las localizaciones centrales y resección segmentaria en las periféricas. En casos invasivos se indica una cirugía más agresiva1,6,7. El pronóstico es excelente, con el 78-100% de remisión completa a los 3,3 años y hasta el 89% a los 10 años6,7. Se ha descrito recidiva intratorácica en el 5% de los casos, habitualmente relacionada con márgenes afectados. Los factores de riesgo relacionados con mala evolución son la necesidad de reintervención, con hasta el 96% de mortalidad a los 5 años, y el tamaño mayor de 3cm6-8. Existen casos descritos de recidiva extratorácica.
La terapia esteroidea presenta efectos variables, desde resolución completa a totalmente ineficaz6-9. Existen múltiples casos con buen resultado cuando se usa como tratamiento primario, aunque no hemos hallado datos sobre seguimiento a largo plazo6. Por ello se considera como tratamiento alternativo cuando existe contraindicación para la cirugía (por inoperabilidad o por el número de lesiones)2,6-8. En nuestro primer caso se pudieron comprobar 7 meses de evolución libre de enfermedad hasta su fallecimiento por otras causas. La quimioterapia presenta resultados variables, con pocos estudios y resultados poco favorables en solitario. Podría ser útil en lesiones multifocales, invasión local o recurrencia6,7. La radioterapia presenta resultados poco concluyentes y ha sido poco utilizada6,7. También se han descrito algunos raros casos de regresión espontánea2,9.