Al mejorar la supervivencia del cáncer, la presencia de tumores múltiples en un paciente es cada vez más frecuente. El objetivo del estudio ha sido analizar la evolución a largo plazo, especialmente las posibles recidivas y segundos tumores primarios, en pacientes con cáncer de pulmón (CP) y supervivencia≥3 años.
Material y métodosEstudio retrospectivo de 1.769 pacientes con CP. Se incluyen 218 (136 tratados con cirugía y 82 con otros tratamientos) con supervivencia global≥3 años, de cualquier estirpe y seguidos durante un período entre 5 y 23 años. Se registró la evolución del CP y las enfermedades intercurrentes.
ResultadosUn total de 65 presentaron recidiva del tumor, de los cuales el 60,9% apareció en los 3 primeros años; 26 desarrollaron segundos primarios pulmonares (84,6% después de 5 años) y 24, 2 o más segundos extrapulmonares (66,6% después de 5 años), la mayoría relacionados con el tabaco. La incidencia de segundos primarios fue superior a la incidencia esperable de cáncer en población general de similar edad y género.
ConclusiónEl efecto carcinogénico múltiple del tabaco persiste y se manifiesta en diversos órganos después de pasados 5 años tras el diagnóstico de CP, incluso en pacientes que han tenido una larga supervivencia. Después de 5 años, un segundo tumor es más probable que una recidiva del primero y el pulmón es el órgano con mayor probabilidad de desarrollar un segundo tumor.
As cancer survival improves, the appearance of multiple tumors in a single patient is becoming more common. The aim of this study was to analyze long-term evolution, focusing particularly on disease recurrence and second primary tumors, in patients with lung cancer (LC) and ≥ 3 years overall survival.
Material and methodsRetrospective study of 1,769 patients with LC. A total of 218 (136 treated with surgery and 82 with other treatments), followed up for between 5 and 23 years were enrolled. LC progress and intercurrent diseases were recorded.
ResultsA total of 65 patients presented tumor relapse, of which 60.9% occurred in the first 3 years; 26 patients developed secondary primary tumors (84.6% after 5 years) and 24 developed 2 or more second extrapulmonary tumors (66.6% after 5 years), most of which were smoking-related. The incidence of second primaries was greater than the expected incidence of cancer in the general population matched for age and sex.
ConclusionThe multiple carcinogenic effect of smoking persists and manifests in various organs, more than 5 years after the diagnosis of LC, even in patients with long survival. After 5 years, a second tumor is more likely than a relapse of the primary disease, and the lung is the most common site of development of a second tumor.
El cáncer de pulmón (CP) es el tumor que produce mayor mortalidad en el mundo. Su pronóstico es pobre, con tasas de supervivencia a 5 años entre 10 y 20% en la mayoría de países1,2. Durante muchos años, la posibilidad de larga supervivencia ha estado limitada casi exclusivamente a pacientes candidatos a resección quirúrgica completa3. Sin embargo, desde hace 25 años, la introducción de nuevas pautas de quimioterapia (QT), combinadas con radioterapia torácica (RTT) mediante diferentes esquemas, deparó un aumento de respuestas favorables en pacientes con estado locorregional avanzado, alcanzando algunos una supervivencia prolongada4–6. Más recientemente, la introducción de nuevos fármacos frente a dianas moleculares específicas aplicables a ciertos subgrupos de CP con determinados rasgos genético-moleculares, ha deparado respuestas favorables duraderas en algunos pacientes con estadio iv7, aunque todavía hay pocos datos sobre las expectativas de vida a 5 años.
En la pequeña proporción de casos de supervivencia prolongada, la aparición de recidivas tardías o segundos tumores primarios (STP) es relativamente frecuente. A este respecto, hay publicaciones en pacientes resecados8–12, aunque pocos estudios centrados en la evolución de pacientes con CP no tratados mediante cirugía y con larga supervivencia13–15.
En este trabajo hemos analizado la evolución de nuestros pacientes con CP y supervivencia≥3 años, con el objetivo de conocer la frecuencia de aparición de recidivas y segundos tumores, así como los intervalos temporales entre ellos.
Pacientes y métodosEs un estudio retrospectivo en el que se revisan las historias clínicas de 1.769 pacientes con CP diagnosticados entre 1991 y 2009 (ambos inclusive): 310 recibieron tratamiento quirúrgico con o sin medicación neoadyuvante o adyuvante; 1.009 recibieron QT, RTT, o QT y RTT combinadas y 450, solo medicación paliativa.
Se incluye en este estudio a 218 pacientes con diagnóstico citohistológico de CP y supervivencia global≥3 años (12,3% de los examinados), independientemente de cuál fuese el tratamiento recibido. Se han registrado los datos siguientes relativos al momento del diagnóstico: edad, género, hábito tabáquico, estirpe histológica, estadio TNM (clasificación de la IASLC de 2009) y modalidad terapéutica aplicada. En cuanto al seguimiento, los pacientes diagnosticados de CP fueron revisados al menos 3 veces al año durante los 2 primeros años y una vez al año a partir del tercer año; los tratados con QT o RTT fueron revisados con mayor frecuencia durante los 2 primeros años. El estudio fue cerrado en diciembre de 2014 e incluyó a pacientes diagnosticados hasta final de 2009, por lo que se dispone de un seguimiento mínimo de 5 años en los aún vivos. Se registraron durante la evolución las enfermedades intercurrentes, y, con objeto de conocer la incidencia de neoplasias extrapulmonares, en muchos pacientes ha sido preciso revisar la historia y documentación electrónica de otros servicios o especialidades, así como los informes de biopsias de diferentes órganos.
Para diferenciar en algunos casos entre recidiva del tumor primario y segundo primario pulmonar (SPP) se adoptaron los criterios de Martini y Melamed, con la modificación temporal propuesta por Detterbeck16,17, de modo que se consideró segundo primario en caso de: a) diferente estirpe; b) localización pulmonar diferente en ausencia de afectación ganglionar mediastínica, o c) intervalo temporal>4 años17.
La frecuencia de recidivas y las tasas de STP, pulmonares y extrapulmonares, se expresan en n.° de casos/100 personas/año, para lo que se computó la suma de los tiempos de seguimiento hasta el último contacto con cada paciente. Para valorar la magnitud de dichas tasas, se compararon con las tasas de incidencia de CP en población general de nuestro medio18,19, obteniendo así una estimación del riesgo relativo. Con respecto a las tasas de STP, las comparaciones se realizaron con las de regiones españolas que disponen de registros poblacionales de cáncer homologados20 (en nuestra región no se dispone aún de tales registros). Dado el pequeño n.° de mujeres en nuestra serie, todas las comparaciones se efectuaron solo en hombres.
Análisis estadístico: la comparación de medias se efectuó mediante la prueba de la t de Student. Para la comparación de porcentajes se usó la prueba de χ2.
Consentimiento del comité ético: aunque se trata de un estudio observacional, se solicitó y se obtuvo la autorización del Comité Ético de nuestro centro.
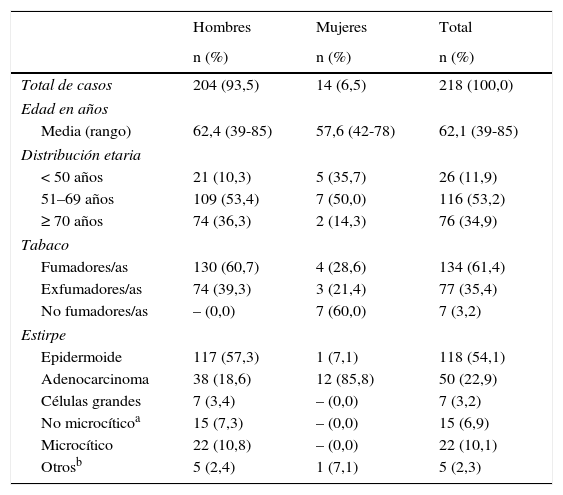
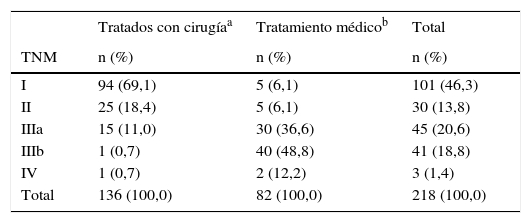
ResultadosLas características demográficas, hábito tabáquico y estirpe histológica de los 218 pacientes incluidos con supervivencia≥3 años se muestran en la tabla 1. En la tabla 2 se presenta la distribución de estadios TNM en función de la modalidad terapéutica aplicada: 1) cirugía o 2) otro tratamiento, a saber: 20 pacientes tratados con QT aislada, 3 con RTT aislada, 55 con una combinación de QT y RTT y 4 con solo medidas paliativas. La gran mayoría de los pacientes quirúrgicos (n=136) tenían estadios I y II, a diferencia de los que recibieron tratamiento médico (n=84), cuyos tumores estaban en estadios avanzados (tabla 2).
Pacientes con cáncer de pulmón y supervivencia≥3 años. Características generales
| Hombres | Mujeres | Total | |
|---|---|---|---|
| n (%) | n (%) | n (%) | |
| Total de casos | 204 (93,5) | 14 (6,5) | 218 (100,0) |
| Edad en años | |||
| Media (rango) | 62,4 (39-85) | 57,6 (42-78) | 62,1 (39-85) |
| Distribución etaria | |||
| < 50 años | 21 (10,3) | 5 (35,7) | 26 (11,9) |
| 51–69 años | 109 (53,4) | 7 (50,0) | 116 (53,2) |
| ≥ 70 años | 74 (36,3) | 2 (14,3) | 76 (34,9) |
| Tabaco | |||
| Fumadores/as | 130 (60,7) | 4 (28,6) | 134 (61,4) |
| Exfumadores/as | 74 (39,3) | 3 (21,4) | 77 (35,4) |
| No fumadores/as | – (0,0) | 7 (60,0) | 7 (3,2) |
| Estirpe | |||
| Epidermoide | 117 (57,3) | 1 (7,1) | 118 (54,1) |
| Adenocarcinoma | 38 (18,6) | 12 (85,8) | 50 (22,9) |
| Células grandes | 7 (3,4) | – (0,0) | 7 (3,2) |
| No microcíticoa | 15 (7,3) | – (0,0) | 15 (6,9) |
| Microcítico | 22 (10,8) | – (0,0) | 22 (10,1) |
| Otrosb | 5 (2,4) | 1 (7,1) | 5 (2,3) |
Estadio TNM según modalidad terapéutica aplicada
El tiempo de seguimiento de los pacientes fue desde 5 hasta 23 años, salvo en los fallecidos antes de 5 años. Con respecto a la evolución, estos fueron clasificados según se muestra en la tabla 3: a) 63 permanecían vivos sin evidencia de recidiva ni de aparición de segundas neoplasias; b) 24 habían fallecido por causas diferentes de recidiva o segunda neoplasia; c) 65 presentaron recidiva (local o a distancia) o progresión tumoral del primer tumor, de los cuales 61 habían fallecido y 4 permanecían vivos; d) 26 desarrollaron un 2.° tumor primario pulmonar, habiendo fallecido 15 de ellos y e) 24 desarrollaron uno o más segundos tumores de localización extrapulmonar, de los cuales, 18 habían fallecido. Finalmente, en 16 (7,3% de los 218), aunque se pudo conocer su estado vital, no se obtuvo información adecuada de su situación médica por inasistencia a la visita programada o traslado a otra comunidad o país.
Evolución, recidivas e incidencia de segundos tumores
| Fallecidos n % | Vivos en la última visitaa n (%) | |
|---|---|---|
| Aún vivos sin evidencia de recidiva ni aparición de 2.° tumor primario | – | 63 (75,0) |
| Fallecidos por causa no neoplásica sin evidencia de recidiva ni 2.° tumor primario | 24 (20,3) | – |
| Pacientes con recidiva o progresión del tumor primario (local o a distancia) | 61 (51,7) | 4 (4,8) |
| Pacientes con segundo tumor primario pulmonar 1.° y 2.° de igual estirpe 1.° y 2.° de diferente estirpe | 15 (12,7) 7 (5,9) 8 (6,8) | 11 (13,1) 4 (4,8) 7 (8,3) |
| Pacientes con segundo tumor primario de origen extrapulmonar | 18 (15,2) | 6 (7,1) |
| Total de pacientes con información sobre evolución | 118 (100,0) | 84 (100,0) |
| Pacientes con información insuficiente sobre la evoluciónb | 14 – | 2 – |
| Total | 132 | 86 |
La media y rango del intervalo temporal transcurrido desde el diagnóstico del CP hasta la recidiva o aparición de un segundo tumor pulmonar o extrapulmonar se recogen en la tabla 4. Estos intervalos se clasificaron en 3 grupos: a)<3 años; b) de 3 a 5 años, y c)>5 años: la mayoría de las recidivas (60,9%) se detectaron durante los primeros 3 años y solo el 7,8% de ellas aparecieron después de 5 años. Por el contrario, la aparición de segundos tumores fue mucho más frecuente después de 5 años, tanto los pulmonares (84,6%) como los extrapulmonares (66,6%). En cuanto a los segundos pulmonares, en 11 casos las estirpes del primero y el segundo fueron iguales: en estos, la diferente localización del segundo, la ausencia de adenopatías mediastínicas y el intervalo transcurrido sugerían un segundo primario frente a la alternativa de recidiva del primero. En otros 14 casos, las estirpes del primero y segundo fueron diferentes.
Intervalo entre el diagnóstico del tumor primario y la recidiva o aparición de un segundo tumor primario
| Recidiva del tumor primario | Segundo primario pulmonar | Segundo primario extrapulmonar | p | |
|---|---|---|---|---|
| Intervalo medio (rango) en meses | 36,1 (12-90) | 86,7 (19-180) | 75,1 (24-234) | < 0,01 |
| n (%) | n (%) | n (%) | ||
|---|---|---|---|---|
| Intervalo<3 años | 39 (60,9) | 1 (1,8) | 4 (16,6) | < 0,001 |
| Intervalo entre 3 y 5 años | 20 (31,3) | 3 (13,6) | 4 (16,6) | < 0,001 |
| Intervalo>5 años | 5 (7,8) | 22 (84,6) | 16 (66,6) | < 0,001 |
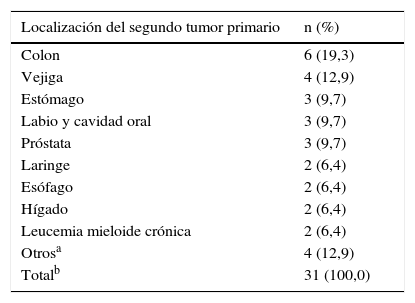
Con respecto a los segundos tumores extrapulmonares, la tabla 5 muestra sus lugares de asiento: el colon (6 casos) y la vejiga (4 casos) fueron los más comunes.
Segundos tumores primarios de localización extrapulmonar
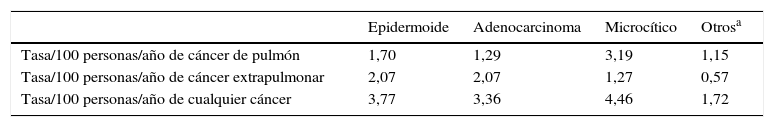
Las tasas de incidencia de a) SPP, b) de cáncer extrapulmonar, o c) cualquier cáncer en el grupo de hombres, expresadas en n.° de casos/100 personas-año, se analizaron en función de la estirpe del primer CP. La tasa de SPP fue: a) 1,29 personas/año en los adenocarcinomas; b) 1,7 en los epidermoides; c) 3,19 en los microcíticos y d) 1,15/100 en el grupo de «otras estirpes» (tabla 6). También se analizaron dichas tasas según que nuestros pacientes hubiesen recibido o no RTT para el tratamiento del primer tumor, con o sin otro tratamiento adicional. Como puede verse, apenas hubo diferencias entre ambos grupos a este respecto (tabla 7). Finalmente, las tasas de segundos cánceres observadas en hombres se compararon con las de incidencia registradas en población general de más de 40 años del mismo sexo en nuestro ámbito geográfico18,19 y las publicadas en registros homologados de provincias de nuestro país20 (tabla 8): el riesgo relativo de cáncer en general (un segundo cáncer, en nuestros pacientes) fue casi 3 veces mayor que en la población general de similar edad, si bien la mayor parte del incremento de riesgo fue debido al aumento de riesgo de CP (riesgo relativo mayor de 7).
Tasa de 2.° cáncer de pulmón y otros cánceres según la estirpe del primero
| Epidermoide | Adenocarcinoma | Microcítico | Otrosa | |
|---|---|---|---|---|
| Tasa/100 personas/año de cáncer de pulmón | 1,70 | 1,29 | 3,19 | 1,15 |
| Tasa/100 personas/año de cáncer extrapulmonar | 2,07 | 2,07 | 1,27 | 0,57 |
| Tasa/100 personas/año de cualquier cáncer | 3,77 | 3,36 | 4,46 | 1,72 |
Cálculo de tasas y estimación del riesgo relativo de cáncer de pulmón y otros cánceres. Riesgo relativo de segunda neoplasia según tratamiento con RTT
| Pacientes que recibieron RTT | Pacientes que no recibieron RTT | Riesgo relativo | |
|---|---|---|---|
| Tasa/100 personas/año de cáncer de pulmón | 1,49 | 1,88 | 0,79 |
| Tasa/100 personas/año de cáncer extrapulmonar | 2,09 | 2,06 | 1,01 |
| Tasa/100 personas/año de cualquier cáncer | 3,58 | 3,93 | 0,91 |
RTT: radioterapia torácica.
Cálculo de tasas y estimación del riesgo relativo de cáncer de pulmón y otros cánceres. Estimación del riesgo relativo de cáncer en relación con la población general
El envejecimiento de la población occidental y la disponibilidad de mejores tratamientos ha contribuido a que actualmente el padecimiento de múltiples neoplasias no sea infrecuente14,15. En lo que respecta al CP, la mayoría de estudios con seguimiento largo se han realizado en pacientes intervenidos en estadios tempranos, y en ellos se ha registrado un aumento en la incidencia de segundas neoplasias con respecto a la incidencia de cáncer en población general8–12. Dado que aquella incidencia depende de la duración del seguimiento, es más adecuado expresar la misma en tasa/100 personas/año, teniendo así en cuenta no solo el n.° de pacientes sino el tiempo de seguimiento total.
En este estudio analizamos, mediante un seguimiento temporal muy amplio, la evolución de nuestros pacientes con CP que han sobrevivido más de 3 años, independientemente de la estirpe o tratamiento recibido.
La supervivencia global del CP es pobre2,3, y en nuestra serie de casos no seleccionados, solo el 12,3% superó los 3 años. En estos, la posibilidad de recidiva o aparición de segunda neoplasia es muy elevada. Así, 65 (32,2%) de nuestros 202 pacientes con evolución conocida presentaron recidiva, local o a distancia. A este respecto, Kelsey et al.11 encuentran que los tiempos medios hasta la recidiva, local o a distancia, en pacientes resecados en estadios tempranos son 14,1 y 12,5 meses, respectivamente. El mayor tiempo observado por nosotros (36 meses) se debe a que nuestro estudio incluyó solo pacientes con supervivencia≥3 años. Sin embargo, además de esa cifra media, tiene sentido clínico clasificar esos intervalos en períodos amplios. Así, en nuestra experiencia, si bien la mayoría de las recidivas sucedieron durante los primeros 3 años (60,9%), todavía fueron relativamente frecuentes hasta los 5 años (31,3% de recidivas detectadas entre 3 y 5 años). Después de 5 años, la probabilidad de recidiva disminuye y en nuestra casuística detectamos solo 5 (7,8%). Esta distribución de intervalos temporales es bastante próxima a la observada en una serie de pacientes con carcinoma pulmonar no microcítico (CPNM) resecados en estadio i8, pese a que nuestros casos fueron diferentes en muchos aspectos (estadio, estirpe y tratamiento heterogéneos).
Con respecto a los STP en pacientes con CP, se ha estudiado especialmente la incidencia de SPP en pacientes resecados, y tales estudios, casi todos retrospectivos, refieren tasas de 1-2 casos/100 personas/año9,14. Aunque en un trabajo prospectivo dicha cifra fue de 4/100, otro análisis también prospectivo en pacientes intervenidos con estadios II y III observó tasas inferiores20. Otros14 han comunicado la incidencia de STP (pulmonares y extrapulmonares), en pacientes con carcinoma pulmonar microcítico (CPM) que sobrevivieron más de 2 años tras el diagnóstico y encuentran tasas de 2-13/100 personas/año y riesgos relativos elevados con respecto a lo esperable en población general13. Al igual que en otras experiencias8,13–16, también en la nuestra los SPP fueron los segundos primarios más comunes, con tasas de 1,79/100 personas/año y representaron casi la mitad de todos los STP. Al diferenciar esas tasas según la estirpe del primer tumor, observamos que era mayor en los CPM. Existen pocas publicaciones a este respecto, pero este hallazgo concuerda con los resultados de Johnson et al.14.
Puesto que en nuestra población general masculina la incidencia de CP es elevada17,18, comparamos la tasa de SPP con la de incidencia de CP en población general de hombres mayores de 40 años de nuestra área, y encontramos un riesgo relativo de 7,19. También la incidencia de otros cánceres era mayor que la registrada en población general de otras regiones españolas, aunque el riesgo relativo era menor (1,9). Si bien no hemos encontrado publicaciones que analicen este aspecto en series globales de pacientes con CP en nuestro país, Kawahara et al.13, en una serie japonesa, detectaron, en casos de CPM, un riesgo relativo de 3,6 de STP y de 7 de SPP con respecto a la población general. Sería interesante conocer si nuestros resultados, referidos a casos de CP mayoritariamente del sexo masculino, son extrapolables a las mujeres en las que la distribución de estirpes es diferente, pero hasta muy recientemente, la incidencia de CP en mujeres de nuestro ámbito era muy baja y no hemos podido analizar ese aspecto.
En cuanto al intervalo transcurrido desde el primer tumor, un SPP puede aparecer en cualquier momento, pero la mayoría de los casos tiene lugar a partir del 3.er y 4. año. Aziz et al.12, en pacientes resecados en estadio temprano, hallan un intervalo medio de 46 meses; para Keller21, en estadios II y iiia intervenidos, ese tiempo fue de 36 o 43 meses, según la modalidad de tratamiento adyuvante; Jeremic et al.22, en estadios tempranos tratados solo con radioterapia, observaron que, a partir de 5 años, la tasa de SPP aumentaba desde 1,1 hasta 2,2/100 personas/año, aunque los segundos extrapulmonares incidían más frecuentemente durante el primer quinquenio. También en casos de CPM tratados con QT y RTT, la mayoría de SPP se detectan a partir del 4.° o 5.° años13. Por el contrario, Duchateau et al.15, en casos de CPNM con estadios diversos tratados con varias modalidades (cirugía, QT o RTT), encuentran que el 80% de segundos tumores primarios (pulmonares o extrapulmonares) aparecieron dentro del primer año, aunque en esta serie el seguimiento fue corto y se incluyó a todos los pacientes, muchos con corta supervivencia global. En nuestros casos, todos supervivientes de 3 años o más, con tiempos de seguimiento extensos (5 a 23 años) —lo que permite una perspectiva más amplia— encontramos un intervalo medio muy superior (86 meses) y la gran mayoría de los SPP (84,6%) apareció después de 5 años tras el primer tumor. Opinamos que las diferencias observadas entre distintos autores se deben a diferencias en el tipo de pacientes (estirpes, estadios y modalidades terapéuticas) y en la metodología practicada, pero la mayoría de los SPP tienen lugar a partir del 4.° o 5.° año, a diferencia de las recidivas del primario que predominan durante los 3 primeros años, intervalos en consonancia con los criterios orientativos de Detterbeck et al.17 para distinguir entre recidivas del primero y SPP en casos dudosos.
Varios estudios retrospectivos han buscado circunstancias que expliquen esta elevada frecuencia de segundas neoplasias. Así, Kawahara et al.13 y Johnson et al.14 opinan que la persistencia del hábito tabáquico y la irradiación torácica aplicada sobre el primer tumor contribuyen a ese aumento del riesgo. Sin embargo, Jeremic et al.22, en pacientes con CPNM en estadios tempranos tratados con radioterapia concluye que estos, si bien presentan una elevada incidencia de segundas neoplasias, lo hacen con tasas similares a las de pacientes con los mismos estadios tratados solo mediante cirugía. Nosotros hemos comparado la tasa de SPP y extrapulmonares en 2 grupos de pacientes según que hubieran recibido o no RTT y no observamos diferencias (tabla 7). Aunque la RTT no fue el único tratamiento aplicado, y por tanto no podemos extraer conclusiones sólidas sobre su influencia, nuestros resultados no señalan un papel relevante de la radioterapia en la incidencia de SPP. Para confirmarlo, se necesitarían análisis prospectivos amplios en pacientes tratados con RTT aislada y con seguimiento superior a 10 años, a partir de los cuales parece que podrían manifestarse los efectos cancerígenos de la radiación14.
En cualquier caso, queda por explicar la mayor incidencia de STP en pacientes con CP que no recibieron radioterapia. En este sentido, la hipótesis más plausible es la formulada hace más de 50 años por Slaughter et al.23 para explicar el desarrollo de múltiples tumores primarios en el cáncer de la cavidad oral. Esta hipótesis, conocida bajo la expresión de «cancerización de campo» o síndrome de la «mucosa condenada», se extendió después a otros órganos, como cabeza y cuello, pulmón, esófago, etc., y se refiere al daño generalizado en las mucosas de diversas localizaciones en forma de lesiones preneoplásicas proclives a degenerar en cáncer. Este concepto tiene especial aplicación en relación con el tabaco y las vías aéreas superiores y bronquios, y ha sido replanteado recientemente por Braakhuis et al.24, mediante análisis moleculares realizados en diversas lesiones preneoplásicas: en los márgenes, libres de tumor, de neoplasias de cabeza y cuello, observaron células con alteraciones genéticas que las emparentaban con las del tumor extirpado. En lo que al CP respecta, este concepto no solo proporciona una explicación plausible de la elevada frecuencia de SPP sino de la común asociación entre CP y cáncer de cabeza y cuello, hace tiempo conocida25. Entre nuestros pacientes, fumadores o exfumadores en su casi totalidad, varios casos de STP fueron de laringe, esófago y cavidad oral y, al igual que otros autores, nosotros también hallamos elevado n.° de STP en colon, vejiga y estómago (tabla 5), tumores para los que se considera establecido el papel causal del tabaco26.
Pese al elevado tiempo de seguimiento de nuestros pacientes, la naturaleza retrospectiva del estudio no permite asegurar el registro exhaustivo de segundos neoplasias, algo que exigiría un estudio prospectivo largo y diseñado para la búsqueda en profundidad de nuevos tumores. Es previsible que en tales estudios se encontrasen riesgos relativos aún más elevados. Por otro lado, nuestra estimación del riesgo relativo es indirecta, y ha sido preciso, aunque solo para la comparación de la incidencia de segundos cánceres en general, recurrir a registros de otras comunidades de nuestro país. Sin embargo, creemos que las diferencias entre regiones españolas no son lo suficientemente grandes para alterar de forma sustancial nuestras estimaciones finales.
ConclusiónEn pacientes que han sobrevivido a un CP largo tiempo, más allá de posibles recidivas, los efectos cancerígenos del tabaco sobre múltiples órganos persisten mucho después de pasados 5 años y es el pulmón el órgano con mayores probabilidades de desarrollar un segundo tumor. Después de 5 años, es más probable un STP que una recidiva del primer tumor.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.