La fibrosis pulmonar idiopática (FPI) es una forma crónica y progresiva de neumonía intersticial fibrosante que se caracteriza por un empeoramiento progresivo funcional y sintomático, sin filiación etiológica bien determinada. Se reconoce la asociación de la FPI con el tabaquismo pasivo, reflujo gastroesofágico, infecciones víricas crónicas, enfisema pulmonar y las neoplasias pulmonares1,2. La presencia de neoplasia pulmonar es más elevada en estos pacientes (documentada mediante seguimiento clínico e informes post mortem), con una incidencia acumulada a los 3 años del 82%, lo que permite considerar la FPI un factor de riesgo independiente para el desarrollo de neoplasia pulmonar (NP), relacionándose con el tiempo acumulado tras el diagnostico3–7.
Nos encontramos, por tanto, ante una enfermedad progresiva con mal pronóstico y con una incidencia de NP más elevada, en la que el manejo clínico supone un reto para la toma de decisiones terapéuticas.
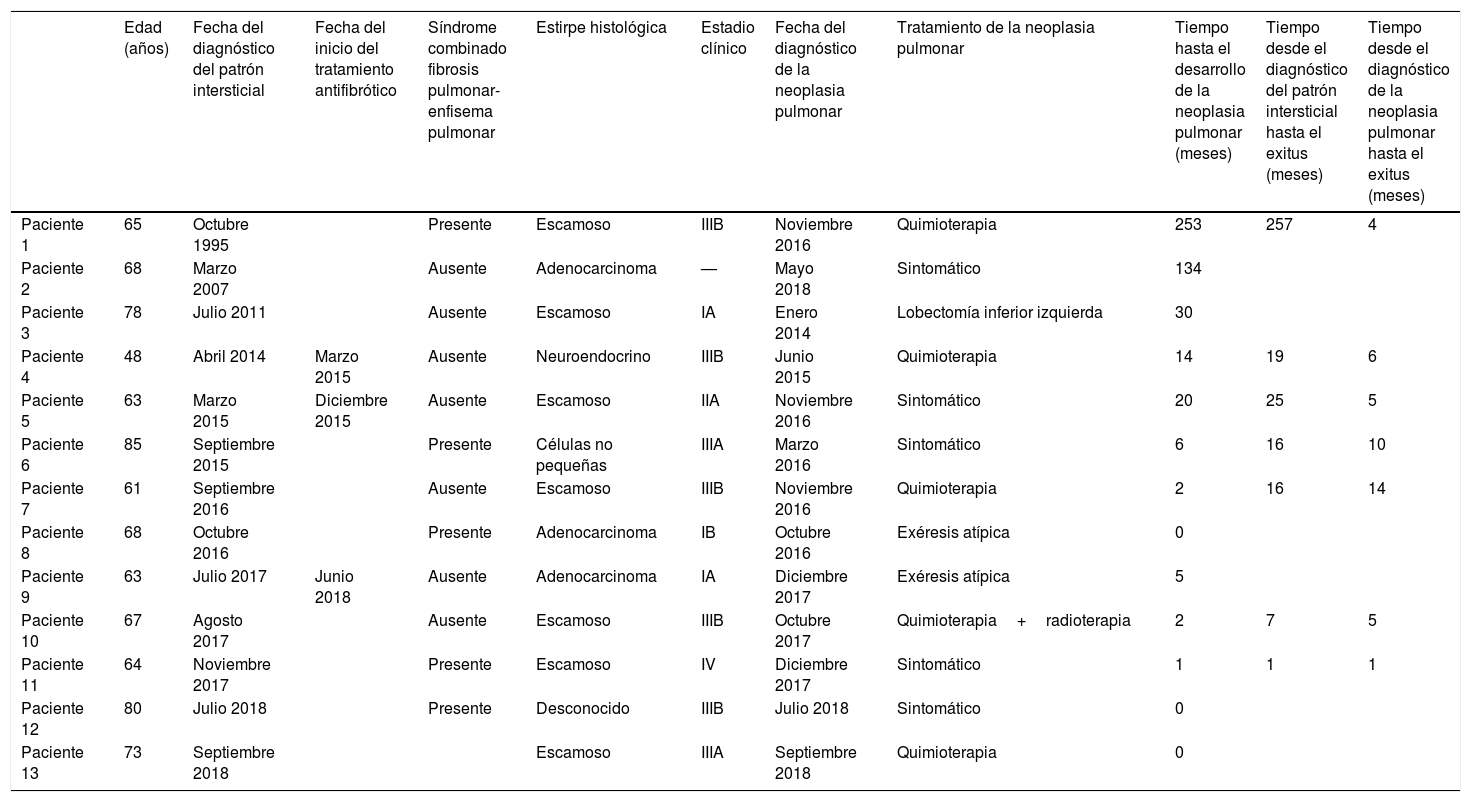
Presentamos la serie de nuestro centro compuesta por 13 pacientes (tabla 1) con un periodo de inclusión comprendido entre enero 2014-diciembre 2018. El 93% de la muestra eran varones (n=12) y presentaban una edad media de 67,9 años, siendo destacable el antecedente de tabaquismo (actual o pasado) en todos los casos. Mediante una anamnesis detallada se recogió una incidencia de antecedentes familiares de neoplasia pulmonar en el 30% de los casos, así como FPI con agrupación familiar en uno de los pacientes. El 38% de la muestra (n=5) reunían criterios radiológicos para ser considerados combinación de fibrosis pulmonar y enfisema (CFPE).
Características detalladas de los pacientes con fibrosis pulmonar idiopática y neoplasia pulmonar
| Edad (años) | Fecha del diagnóstico del patrón intersticial | Fecha del inicio del tratamiento antifibrótico | Síndrome combinado fibrosis pulmonar-enfisema pulmonar | Estirpe histológica | Estadio clínico | Fecha del diagnóstico de la neoplasia pulmonar | Tratamiento de la neoplasia pulmonar | Tiempo hasta el desarrollo de la neoplasia pulmonar (meses) | Tiempo desde el diagnóstico del patrón intersticial hasta el exitus (meses) | Tiempo desde el diagnóstico de la neoplasia pulmonar hasta el exitus (meses) | |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Paciente 1 | 65 | Octubre 1995 | Presente | Escamoso | IIIB | Noviembre 2016 | Quimioterapia | 253 | 257 | 4 | |
| Paciente 2 | 68 | Marzo 2007 | Ausente | Adenocarcinoma | — | Mayo 2018 | Sintomático | 134 | |||
| Paciente 3 | 78 | Julio 2011 | Ausente | Escamoso | IA | Enero 2014 | Lobectomía inferior izquierda | 30 | |||
| Paciente 4 | 48 | Abril 2014 | Marzo 2015 | Ausente | Neuroendocrino | IIIB | Junio 2015 | Quimioterapia | 14 | 19 | 6 |
| Paciente 5 | 63 | Marzo 2015 | Diciembre 2015 | Ausente | Escamoso | IIA | Noviembre 2016 | Sintomático | 20 | 25 | 5 |
| Paciente 6 | 85 | Septiembre 2015 | Presente | Células no pequeñas | IIIA | Marzo 2016 | Sintomático | 6 | 16 | 10 | |
| Paciente 7 | 61 | Septiembre 2016 | Ausente | Escamoso | IIIB | Noviembre 2016 | Quimioterapia | 2 | 16 | 14 | |
| Paciente 8 | 68 | Octubre 2016 | Presente | Adenocarcinoma | IB | Octubre 2016 | Exéresis atípica | 0 | |||
| Paciente 9 | 63 | Julio 2017 | Junio 2018 | Ausente | Adenocarcinoma | IA | Diciembre 2017 | Exéresis atípica | 5 | ||
| Paciente 10 | 67 | Agosto 2017 | Ausente | Escamoso | IIIB | Octubre 2017 | Quimioterapia+radioterapia | 2 | 7 | 5 | |
| Paciente 11 | 64 | Noviembre 2017 | Presente | Escamoso | IV | Diciembre 2017 | Sintomático | 1 | 1 | 1 | |
| Paciente 12 | 80 | Julio 2018 | Presente | Desconocido | IIIB | Julio 2018 | Sintomático | 0 | |||
| Paciente 13 | 73 | Septiembre 2018 | Escamoso | IIIA | Septiembre 2018 | Quimioterapia | 0 |
En nuestra serie, la estirpe escamosa fue la más frecuente (n=9) seguida del adenocarcinoma (n=3), siendo similar a las descritas en la literatura4,5,8. Sin embargo, no se encontró asociación estadística entre la mayor incidencia de lesiones periféricas y su localización en lóbulos inferiores descrita por Kwak et al.9 (p>0,05) El diagnóstico de FPI se realizó mediante criterio clínico/radiológico10 (n=8) o histología pulmonar compatible con patrón de neumonía intersticial usual (n=7).
En 3 casos, el diagnóstico de neoplasia pulmonar fue sincrónico con el de FPI, siendo un hallazgo casual; cifra muy inferior que la presentada por Huddad y Massaro5. En el resto de los pacientes (n=10), se objetivó la presencia de neoplasia pulmonar tras un seguimiento medio de 18,2 meses (DE: 78,56). Los estadios neoplásicos clínicos en nuestra muestra fueron: IA (n=2), IB (n=1), IIA (n=1), IIIA (n=2), IIIB (n=5), estadio IV (n=1) y en uno de los casos el paciente rehusó la estadificación tumoral completa. Estos hallazgos discrepan con la elevada incidencia de neoplasias pulmonares en estadios precoces descritos en otras series4,8.
Todos los pacientes fueron valorados por el comité de tumores torácicos de nuestro centro. La decisión final del mismo fue: tratamiento quirúrgico en 3 casos, oncológico en 5 (4 quimioterapia y una quimioterapia y radioterapia) y tratamiento sintomático en 5 ante el estado funcional previo. En un segundo momento, los pacientes sometidos a tratamiento quirúrgico (tras un periodo mínimo de 6 meses libre de enfermedad) fueron valorados en el comité de enfermedades intersticiales, instaurándose tratamiento con fármacos antifibróticos en el 66% (pirfenidona en todos ellos) y seguimiento clínico-funcional estrecho en el caso restante dada la ausencia de sintomatología. Ninguno de los pacientes sometidos a tratamiento quirúrgico padeció agudizaciones de FPI o/y complicaciones postoperatorias, a pesar de ser considerada la cirugía torácica una de las posibles etiologías11. No se encontraron diferencias estadísticamente significativas en el tipo histológico de las NP y el estadio en el momento del diagnóstico en el subgrupo de pacientes de CFPE.
Teniendo en cuenta las limitaciones del estudio como el tiempo de seguimiento no uniforme condicionado por la baja incidencia de casos, en el momento actual, el 54% de los pacientes de la serie ha fallecido (n=7). En el grupo de los pacientes fallecidos, el tiempo de supervivencia medio desde el diagnóstico de FPI fue de 9 meses (DE: 80,54), siendo mayor en los pacientes que recibieron tratamiento con antifibróticos (supervivencia media 22 meses). El análisis del tiempo de supervivencia medio desde el diagnóstico de neoplasia pulmonar fue de 10,5 meses (DE: 11,39), sin embargo, en el subgrupo de los pacientes sometidos a tratamiento quirúrgico el 66% (n=2) continúan vivos, siendo la supervivencia del único paciente fallecido de este grupo de 39 meses. El subanálisis llevado a cabo en el grupo de CFPE reveló una mortalidad total similar (60%) con un tiempo menor de supervivencia medio desde el diagnóstico de NP (5,3 meses, DE: 3,68)
Por otra parte, en nuestra serie, al igual que en otras descritas previamente, la FPI parece ser el factor determinante en la esperanza de vida8,12; siendo necesaria considerar la opción de tratamiento quirúrgico en casos seleccionados. Resulta fundamental una adecuada y detallada valoración funcional del paciente para optimizar los tratamientos de forma individualizada. Consideramos imprescindible, por tanto, el papel de los comités de tumores torácicos y patología intersticial para un abordaje conjunto.
A pesar de que estos resultados deben ser interpretados con prudencia, inducen a pensar que el seguimiento radiológico que supone el diagnóstico previo de FPI, podría implicar la detección precoz de neoplasias pulmonares, haciendo esta asociación previamente anecdótica cada vez más frecuente en la práctica clínica. Es mandatorio valorar la necesidad de un seguimiento radiológico tomográfico específico y personalizado destinado a la detección de neoplasias pulmonares en estadios precoces en esta población seleccionada.
Ante la imposibilidad de autoría de todos los miembros, nos gustaría expresar nuestro agradecimiento, y que así constase por escrito en la publicación, a todos los miembros asistentes del Comité de Oncología Torácica del Hospital Clínico Universitario de Valladolid y del Comité de Enfermedades Intersticiales del Hospital Clínico Universitario de Valladolid.