El estudio con contraste ecográfico es de gran utilidad para evaluar las lesiones pulmonares de localización periférica o contenidas dentro de una consolidación1, ya que la aplicación del contraste nos permite identificar las áreas necróticas y así mejorar la precisión diagnóstica en la obtención de muestras2. Igualmente, el estudio con contraste nos permite establecer un diagnóstico diferencial debido a las características específicas de determinadas patologías como el infarto pulmonar, la atelectasia, las neoplasias agresivas y las atelectasias obstructivas por neoplasia central2.
El tiempo de realce del parénquima o de una lesión pulmonar varía según si existe un aporte vascular por parte de las arterias pulmonares (<6 segundos) o bien si proviene de las arterias bronquiales (>6 segundos). Igualmente, el patrón y la extensión del realce así como el lavado (superior a 60 segundos) en un foco consolidativo o en una lesión pulmonar nos permite determinar si se trata de un colapso pulmonar, un proceso infeccioso/absceso, un infarto o un tumor. En general, los tumores obtienen un aporte vascular arterial que procede de las arterias bronquiales, pues las arterias pulmonares no tienen capacidad de neoangiogénesis. El retraso en la captación de las lesiones malignas se explica por las vasoconstricciones intrínsecas dado el estado de hipoxia intrínseco de la lesión neoproliferativa. Por otro lado, las lesiones benignas reciben doble aporte arterial de las arterias pulmonares y las bronquiales, por lo que tienen un realce precoz3.
Así pues, en caso de las atelectasias pasivas observaremos una consolidación homogénea en el modo B con broncograma hiperecogénico en su interior y con un realce arterial precoz que persiste durante toda la exploración y puede mantenerse más allá de 5 min4. Los hallazgos para áreas de infarto pulmonar serán similares a los de la atelectasia en modo B y podemos llegar a identificar nodularidades hipoecoicas dentro de la misma. Tras la administración de contraste apreciaremos una ausencia de realce de las áreas infartadas4. Los abscesos pulmonares presentan un realce tardío (>6s) con áreas centrales hipoecoicas e hipocaptantes correspondientes a necrosis, las cuales pueden aparecer sobre neoplasias preexistentes4.
La neumonía y las lesiones metastásicas o lesiones malignas constituyen un reto diagnóstico sobre todo en casos en que coexisten ambas entidades. Las neumonías en general presentan un realce arterial precoz (<6s) y homogéneo. No obstante, en algunos casos ambas patologías presentan un realce retardado (>6s). Se diferencian en que la neumonía mantiene un realce homogéneo en fases tardías con lavado tardío (>60s) mientras que las lesiones metastásicas mostrarán un lavado precoz (<60s) de la lesión respecto al parénquima circundante4.
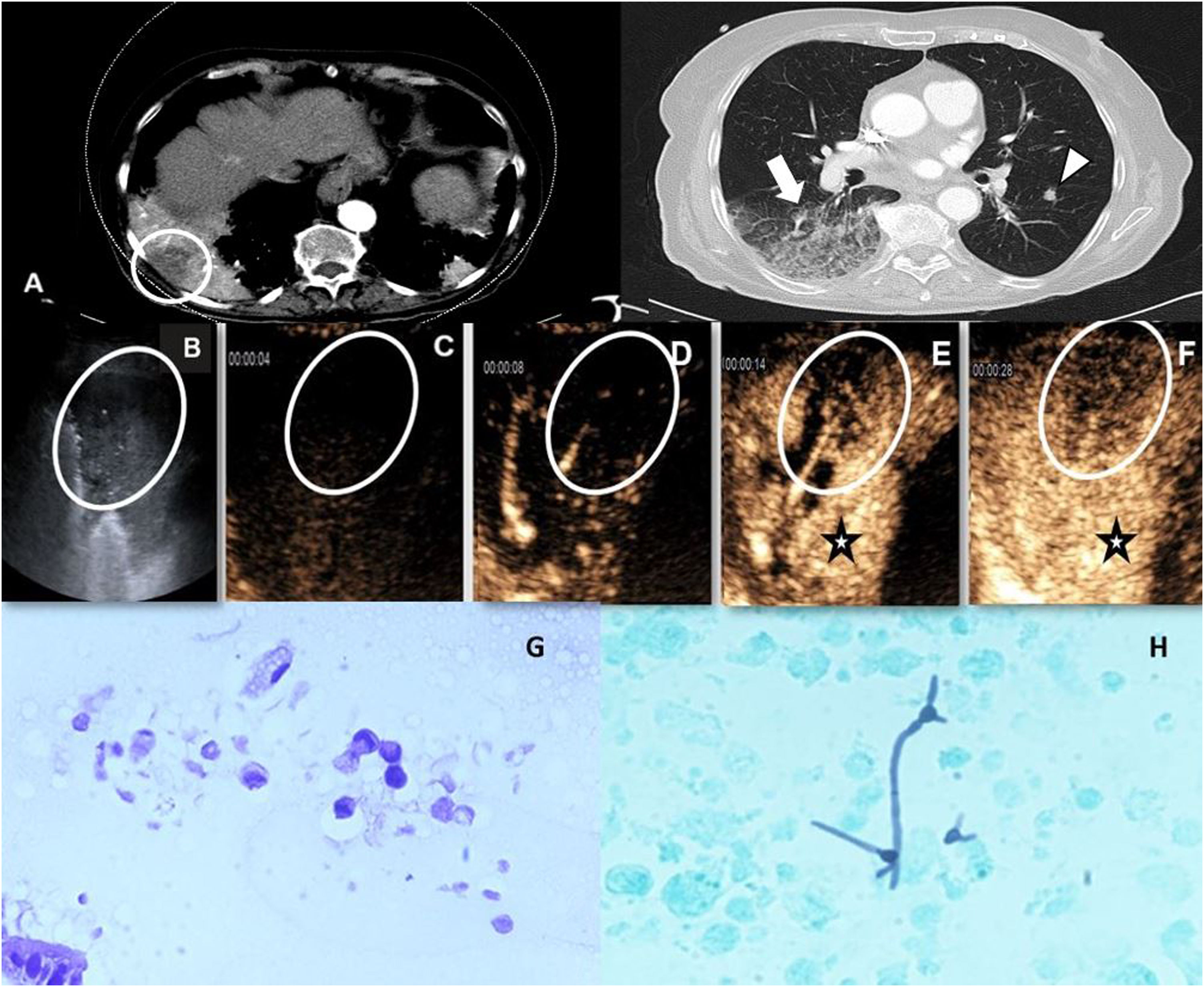
Presentamos el caso de una mujer de 79 años con antecedentes de carcinoma papilar de tiroides que acudió a urgencias por disnea progresiva hasta hacerse de mínimos esfuerzos. Presentaba múltiples focos consolidativos en la radiografía de tórax. Se realizó una tomografía computarizada (TC) que descartó tromboembolismo pulmonar, pero evidenció consolidaciones heterogéneas en ambos lóbulos inferiores junto con áreas sugestivas de bronquiolitis infecciosa y algunos nódulos sólidos (fig. 1A). Se obtuvo una analítica positiva para marcadores tumorales (CA 19-9 y CYFRA 21-1) y ante la sospecha de un posible origen neoplásico, se realizó una tomografía por emisión de positrones (PET/TC) con fluorodesoxiglucosa que objetivó un probable cáncer pancreático y posibles metástasis pulmonares consolidativas. Dado que la consolidación de mayor tamaño, localizada en el lóbulo inferior derecho, presentaba amplio contacto con la pleura periférica, se optó por realizar una biopsia con guía ecográfica. Se administraron 2,4ml de contraste ecográfico (SonoVue, Rovi, Pozuelo de Alarcón, Madrid, España) y se objetivaron dos zonas diferenciadas según el patrón de captación: un área periférica con captación tardía (más allá de los 6 segundos postinyección) y lavado precoz (desaparición de la captación de contraste a los pocos segundos de iniciarse la captación) y el resto de la consolidación con captación precoz (antes de 6 segundos) y homogénea y lavado tardío (más allá de un minuto) (fig. 1B-F). Ante estos hallazgos se decidió biopsiar la primera de las zonas descritas con aguja fina de 22G con el resultado de metástasis alveolar de adenocarcinoma pancreático (fig. 1G). Debido a que el resto de la consolidación mostró características sugestivas de proceso neumónico se decidió realizar fibrobroncoscopia y toma de muestras que demostraron una infección fúngica (fig. 1H).
A) TC tras la administración de contraste yodado intravenoso. Se muestran cortes axiales en ventana de mediastino (izquierda) y de parénquima pulmonar (derecha) donde se observa una consolidación heterogénea en el lóbulo inferior derecho con áreas hipocaptantes (círculo) junto con zonas en vidrio deslustrado y árbol en brote (flecha). Adicionalmente existen algunos nódulos sólidos pulmonares bilaterales (cabeza de flecha) en probable relación con metástasis. B) Ecografía en modo B practicada en el mismo paciente donde se visualiza una consolidación heterogénea sin broncograma aéreo y un área subpleural anecoica (elipse). C-F) Imágenes ecográficas tras la inyección de contraste ecográfico identificando un realce homogéneo, aunque retrasado (estrella) del parénquima pulmonar consolidado (patrón neumónico). Adicionalmente, se observa un área de morfología triangular subpleural cuyo realce es más retrasado respecto al parénquima consolidado circundante (oval). Además, muestra un lavado precoz, hallazgos sugestivos de malignidad. Se realizó posteriormente biopsia guiada con ecografía sobre el área sospechosa con resultados histológicos de metástasis de adenocarcinoma pancreático. Posteriormente, una fibrobroncoscopia confirmó la infección fúngica sobreañadida en el parénquima circundante. G) Grupos de células epiteliales grandes atípicas y vacuoladas en relación con metástasis de adenocarcinoma pancreático. H) Análisis microbiológico de la muestra de lavado broncoalveolar en el área consolidativa donde se observan estructuras ramificadas correspondientes a hifas.
El caso expuesto se incluye dentro de este grupo, pues existía una consolidación neumónica preexistente con un área hipoecoica en su interior. Tras el estudio con contraste ecográfico la consolidación presentó una captación tardía y homogénea con lavado tardío a excepción del área central y periférica cuyo comportamiento mostró una captación tardía pero lavado precoz, sugestivo de malignidad. El patrón de captación objetivado permitió además guiar la biopsia percutánea hacia la zona deseada más sospechosa para mejorar la rentabilidad diagnóstica en la obtención de muestras.
La biopsia con guía ecográfica es una alternativa a la realizada mediante TC para las lesiones pulmonares periféricas o pleurales1,3 y alcanza una efectividad y rentabilidad diagnóstica similar a la obtenida con TC5. Adicionalmente, los procedimientos percutáneos guiados por ecografía ofrecen ciertas ventajas tales como la monitorización del procedimiento en tiempo real, la ausencia de radiación, menores costes y duración del procedimiento, con ratios de complicaciones similares o menores a los de la biopsia guiada por TC1,2. En muchos casos el estudio con ecografía torácica con contraste ayuda a comprender la naturaleza de la lesión a estudio y guiar, en caso que fuere necesario, la toma de muestras hacia áreas de interés evitando focos necróticos1,2,6 o hacia las zonas de mayor sospecha de malignidad como en el caso presentado.