La magnitud de la resistencia actual a fármacos antituberculosos en España es desconocida. El objetivo del estudio es describir la resistencia a fármacos antituberculosos de primera línea y determinar sus factores asociados.
MétodosEstudio prospectivo multicéntrico de pacientes tuberculosos adultos con aislamiento de Mycobacterium tuberculosis y antibiograma de fármacos de primera línea en 32 hospitales y un centro extrahospitalario del sistema sanitario nacional durante los años 2010 y 2011.
ResultadosSe estudió a 519 pacientes, 342 españoles y 177 (34,1%) extranjeros, 48 de ellos (9,2%) con resistencia a cualquier fármaco, de los que 35 (6,7%) eran resistentes a isoniacida. Hubo 10 casos multirresistentes (1,9%) y ninguno extremadamente resistente. Se detectó resistencia inicial a isoniacida en 28 de los 487 (5,7%) pacientes sin antecedentes de tratamiento antituberculoso previo, afectando más a los extranjeros (p<0,01), y resistencia adquirida en 7 (22,6%) casos previamente tratados. La multirresistencia fue inicial en 6 casos (1,2%) y adquirida en otros 4 (12,9%). Los factores asociados a tener resistencia inicial a isoniacida fueron ser inmigrante y la convivencia en grupo (OR=2,3; IC del 95%, 0,98-5,67, y OR=2,2; IC del 95%, 1,05-7,07, respectivamente). El factor asociado a la existencia de resistencia adquirida a isoniacida fue la edad inferior a 50 años (p=0,03).
ConclusionesLa tasa de resistencia inicial a isoniacida es superior a la estimada, probablemente debida al aumento de la inmigración durante los últimos años, lo que aconseja su vigilancia nacional sistemática. Los individuos inmigrantes y los que conviven en grupo tienen mayor riesgo de tener resistencia a isoniacida.
The magnitude of current resistance to antituberculosis drugs in Spain is unknown. The objective of this study is to describe resistance to first-line antituberculosis drugs and determine the associated factors.
MethodsProspective multicenter study of adult tuberculosis patients with positive Mycobacterium tuberculosis culture and antibiogram including first-line drugs in 32 hospitals and one out-patient center of the Spanish Health System between 2010 and 2011.
ResultsA total of 519 patients, 342 Spanish nationals and 177 (34.1%) foreigners were studied. Drug resistance was found in 48 (9.2%), of which 35 (6.7%) were isoniazid-resistant. There were 10 (1.9%) multiresistant cases and no strain was extremely resistant. Initial isoniazid resistance was detected in 28 of the 487 (5.7%) antituberulosis-naïve patients, most of whom were foreigners (P<.01). Acquired resistance was seen in 7 (22.6%) previously treated cases. Multiresistance was initial in 6 cases (1.2%) and acquired in another 4 (12.9%). Factors associated with initial isoniazid resistance were immigrant status and group cohabitation OR=2.3; 95%CI: .98-5.67 and OR=2.2; 95%CI: 1.05-7.07 respectively). The factor associated with acquired resistance to isoniazid was age below 50 years (P=.03).
ConclusionsThe rate of initial isoniazid resistance is greater than estimated, probably due to the increase in immigration during recent years, suggesting that systematic national monitoring is required. Immigrants and those who cohabit in groups have a higher risk of isoniazid resistance.
La Organización Mundial de la Salud (OMS) estima que en 2011 hubo 8,7 millones (125/100.000 habitantes) de nuevos casos de tuberculosis (TB), el 13% de ellos infectados por VIH. La mortalidad mundial de la TB ha disminuido un 41% desde 19901, mientras se espera también un descenso en su morbilidad al haberse logrado una tasa de cumplimiento del tratamiento mayor del 85% en los nuevos casos y del 87% en enfermos bacilíferos1, esperanza que puede truncarse por el aumento de casos con Mycobacterium tuberculosis (MT) resistente a fármacos (DR-TB), multirresistentes (MDR-TB) y extremadamente resistentes (XDR-TB). Se estima que el 3,7% de los nuevos casos y el 20% de los casos tratados con anterioridad tienen MDR-TB, siendo XDR-TB el 9% de las MDR-TB notificadas1. La OMS y la Unión Internacional contra la Tuberculosis y las Enfermedades Respiratorias iniciaron en 1994 su Proyecto Global para la Vigilancia de la Resistencia a Fármacos Antituberculosos, recopilando datos mundiales estandarizados de cepas de MT estudiadas en laboratorios de microbiología expresamente acreditados2. En su último informe, con datos de 2002-2007, estima una prevalencia media de DR-TB del 11,1% y una prevalencia de MDR-TB del 1,6% en pacientes nuevos sin tratamiento previo3,4. Un informe posterior concluye que en 2009 y en 2010 se registraron las tasas globales de MDR-TB más altas de la historia (65,1% en Moldavia)5.
Las tasas de resistencia detectadas durante 2005 en las únicas 3 zonas españolas (Barcelona, Galicia y Aragón) que participan en dicho programa oscilaron entre: DR-TB 7,3-9,9%; resistencia a isoniacida (DR-TB-H) 3,9-7,1% y MDR-TB 0,3-1,8%3-5. El Centro Europeo para el Control de las Enfermedades, basándose en datos españoles del 2010 con antibiograma realizado en el 35,5% de los casos, publica tasas de DR-TB-H del 7,7% y MDR-TB del 3,5%, de las que el 6,1% son XDR-TB6. Dos estudios representativos de la población tuberculosa española describen resultados similares con las siguientes tasas: DR-TB del 7,9-8,3%, DR-TB-H próximas al 5% y escasa MDR-TB en pacientes nunca tratados con anterioridad7,8.
El objetivo de nuestro estudio es realizar una estimación prospectiva de la DR-TB a fármacos de primera línea en España, en una cohorte de pacientes tuberculosos con cultivo de MT y antibiograma sistemáticos.
MétodoEl estudio RETUBES es un estudio observacional prospectivo y multicéntrico de una cohorte de pacientes diagnosticados de TB en España entre el 1 de enero del 2010 y el 31 de diciembre del 2011, en los que se ha aislado MT y se ha determinado su antibiograma. El estudio fue diseñado por el Programa Integrado de Investigación en Tuberculosis (PII-TB) de la Sociedad Española de Neumología y Cirugía Torácica (SEPAR) y ofrecido a todos sus miembros con el soporte de la infraestructura del PII-TB y de una beca SEPAR 2008 de ayudas a la investigación.
Se ha incluido a 519 pacientes adultos diagnosticados de TB por neumólogos y especialistas en enfermedades infecciosas del PII-TB en 32 hospitales y una unidad extrahospitalaria de 13 comunidades autónomas (CC. AA.) que aceptaron participar en el estudio. Los criterios de inclusión de los pacientes han sido: haber cumplido 18 años, aislamiento de MT, investigación con antibiograma de fármacos de primera línea y consentimiento informado del paciente para la utilización de sus datos. Para caracterizar a los pacientes según el antecedente o no de tratamiento antituberculoso previo, se ha excluido un caso por pérdida del dato.
El aislamiento de MT se ha efectuado en cada centro por su método habitual a partir de cultivos en medio sólido de Lowenstein-Jensen (L-J) o en medio líquido confirmado posteriormente por L-J. Los antibiogramas se han realizado en los hospitales de tercer nivel por el método habitual en su laboratorio, mientras que en el resto de los hospitales se han derivado a centros de referencia nacional. La sensibilidad a fármacos se ha estudiado por métodos fenotípicos convencionales, en medio sólido por el método indirecto de las proporciones o en medio líquido mediante BACTEC™ MGIT 960 automatizado (Becton Dickinson Diagnostic Systems, Sparks, MD, EE. UU.).
DefinicionesDR-TB: TB con resistencia de MT a cualquier fármaco antituberculoso de primera línea.
DR-TB-H: TB con resistencia de MT a H.
MDR-TB: TB con resistencia de MT, al menos a H y rifampicina (R).
XDR-TB: MDR-TB con resistencia adicional de MT a una fluoroquinolona y al menos a uno de los 3 fármacos antituberculosos de segunda línea (capreomicina, kanamicina o amicacina).
Resistencia inicial: resistencia de MT a uno o más fármacos antes de iniciar el tratamiento de un paciente nuevo que nunca ha sido tratado con fármacos antituberculosos.
Resistencia adquirida: resistencia de MT a uno o más fármacos en pacientes previamente tratados durante uno o más meses con fármacos antituberculosos.
Extranjero: en este estudio, los casos de TB se corresponden con emigrantes por motivos económicos procedentes de países en vías de desarrollo.
VariablesLos datos se recogieron y registraron en un cuaderno electrónico cumplimentado en la web para su depuración y análisis. La variable principal fue la resistencia a fármacos antituberculosos de primera línea, mientras las variables secundarias incluyeron las características epidemiológicas, microbiológicas y clínicas.
Análisis estadísticoSe realizó un estudio descriptivo de la prevalencia de MT con resistencias a fármacos mediante distribución de frecuencias para las variables cualitativas. El análisis bivariado se realizó mediante la prueba de la χ2 con el test de Fisher bilateral y la corrección de Yates cuando los valores esperados fueron inferiores a 5. Los factores de riesgo para DR-TB-H en pacientes nunca tratados se analizaron mediante regresión logística (método stepwise), incluyendo de forma exploratoria todos aquellos factores que influían a nivel bivariado. La prueba de Hosmer y Lemeshow se usó para comprobar la bondad del ajuste del modelo. Un valor de p<0,05 se consideró estadísticamente significativo. Los factores asociados a DR-TB-H en pacientes previamente tratados solo se pudieron explorar a nivel bivariado, ya que, a nivel multivariado, tenían insuficiente poder estadístico. Como medida de asociación se calculó la odds ratio (OR) con intervalos de confianza del 95% (IC del 95%). Todos los análisis se realizaron usando el paquete estadístico SPSS v.18.0 (SPSS Inc, Chicago, EE. UU.).
El proyecto fue aprobado por el Comité Ético de Investigación Clínica (CEIC) del Hospital Universitario Dr. Peset de Valencia y por los CEIC de otros 12 hospitales nacionales. Todos los registros con datos identificativos de pacientes fueron tratados de manera confidencial de acuerdo con la Ley española 15/1999 de Protección de Datos de Carácter Personal.
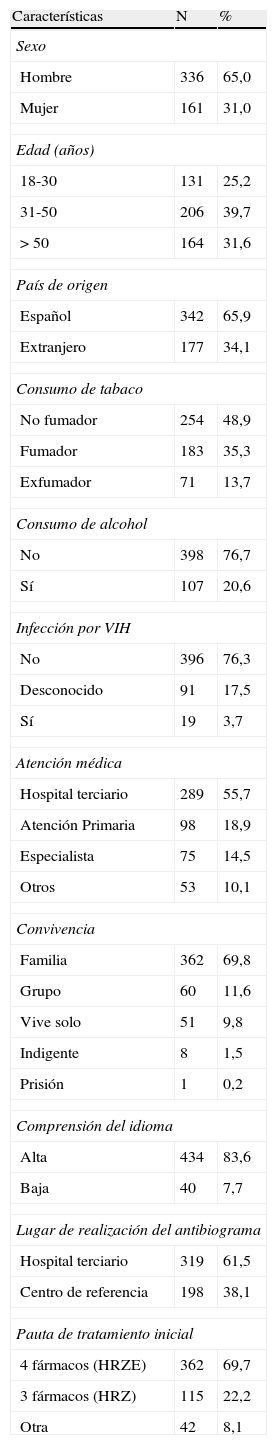
ResultadosSe incluyó a 554 pacientes tuberculosos con cultivo positivo de MT, limitando la muestra del estudio a los 519 que disponían de antibiograma, 342 (65,9%) españoles y 177 (34,1%) extranjeros. Las características sociodemográficas y clínicas se describen en tabla 1.
Características sociodemográficas y clínicas de los 519 pacientes tuberculosos incluidos en el estudio RETUBES
| Características | N | % |
| Sexo | ||
| Hombre | 336 | 65,0 |
| Mujer | 161 | 31,0 |
| Edad (años) | ||
| 18-30 | 131 | 25,2 |
| 31-50 | 206 | 39,7 |
| > 50 | 164 | 31,6 |
| País de origen | ||
| Español | 342 | 65,9 |
| Extranjero | 177 | 34,1 |
| Consumo de tabaco | ||
| No fumador | 254 | 48,9 |
| Fumador | 183 | 35,3 |
| Exfumador | 71 | 13,7 |
| Consumo de alcohol | ||
| No | 398 | 76,7 |
| Sí | 107 | 20,6 |
| Infección por VIH | ||
| No | 396 | 76,3 |
| Desconocido | 91 | 17,5 |
| Sí | 19 | 3,7 |
| Atención médica | ||
| Hospital terciario | 289 | 55,7 |
| Atención Primaria | 98 | 18,9 |
| Especialista | 75 | 14,5 |
| Otros | 53 | 10,1 |
| Convivencia | ||
| Familia | 362 | 69,8 |
| Grupo | 60 | 11,6 |
| Vive solo | 51 | 9,8 |
| Indigente | 8 | 1,5 |
| Prisión | 1 | 0,2 |
| Comprensión del idioma | ||
| Alta | 434 | 83,6 |
| Baja | 40 | 7,7 |
| Lugar de realización del antibiograma | ||
| Hospital terciario | 319 | 61,5 |
| Centro de referencia | 198 | 38,1 |
| Pauta de tratamiento inicial | ||
| 4 fármacos (HRZE) | 362 | 69,7 |
| 3 fármacos (HRZ) | 115 | 22,2 |
| Otra | 42 | 8,1 |
VIH: virus de la inmunodeficiencia humana.
La diferencia entre 519 y los totales de cada variable corresponden a casos en los que no consta el dato.
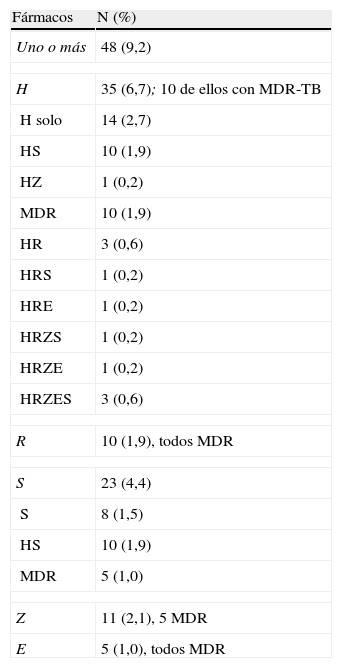
Se detectó DR-TB en 48 (9,2%) pacientes, 35 (6,7%) de ellos resistentes a H, 10 (1,9%) resistentes a R, todos ellos MDR-TB, y el resto resistentes a otros fármacos (tabla 2). La resistencia a H fue más frecuente en extranjeros (tabla 3).
Resistencia a fármacos antituberculosos en los 519 casos incluidos en el estudio RETUBES
| Fármacos | N (%) |
| Uno o más | 48 (9,2) |
| H | 35 (6,7); 10 de ellos con MDR-TB |
| H solo | 14 (2,7) |
| HS | 10 (1,9) |
| HZ | 1 (0,2) |
| MDR | 10 (1,9) |
| HR | 3 (0,6) |
| HRS | 1 (0,2) |
| HRE | 1 (0,2) |
| HRZS | 1 (0,2) |
| HRZE | 1 (0,2) |
| HRZES | 3 (0,6) |
| R | 10 (1,9), todos MDR |
| S | 23 (4,4) |
| S | 8 (1,5) |
| HS | 10 (1,9) |
| MDR | 5 (1,0) |
| Z | 11 (2,1), 5 MDR |
| E | 5 (1,0), todos MDR |
E: etambutol; H: isoniacida; MDR: multirresistencia a fármacos antituberculosos. R: rifampicina; S: estreptomicina; Z: piracinamida.
Las diferentes combinaciones de resistencia a H, R y otros fármacos corresponden a las 10 MDR.
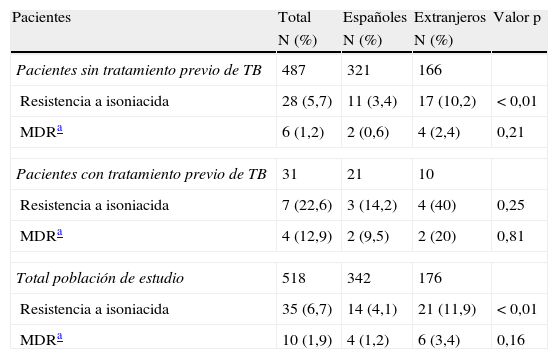
Resistencia a isoniacida y multirresistencia según el tipo de resistencia y el país de origen en los pacientes del estudio RETUBES (N=518)
| Pacientes | Total | Españoles | Extranjeros | Valor p |
| N (%) | N (%) | N (%) | ||
| Pacientes sin tratamiento previo de TB | 487 | 321 | 166 | |
| Resistencia a isoniacida | 28 (5,7) | 11 (3,4) | 17 (10,2) | < 0,01 |
| MDRa | 6 (1,2) | 2 (0,6) | 4 (2,4) | 0,21 |
| Pacientes con tratamiento previo de TB | 31 | 21 | 10 | |
| Resistencia a isoniacida | 7 (22,6) | 3 (14,2) | 4 (40) | 0,25 |
| MDRa | 4 (12,9) | 2 (9,5) | 2 (20) | 0,81 |
| Total población de estudio | 518 | 342 | 176 | |
| Resistencia a isoniacida | 35 (6,7) | 14 (4,1) | 21 (11,9) | < 0,01 |
| MDRa | 10 (1,9) | 4 (1,2) | 6 (3,4) | 0,16 |
MDR: multirresistencia a fármacos.
Entre los 518 casos en que fue posible conocer el antecedente de tratamiento antituberculoso previo, 487 (94,0%) nunca habían sido tratados —321 españoles y 166 extranjeros en similar porcentaje—, mientras que de los 31 (6,1%) casos que habían sido previamente tratados, 21 eran españoles y 10 extranjeros. De los 35 pacientes resistentes a H, 28/487 (5,7%) no habían sido anteriormente tratados, mientras 7/31 (22,6%) sí lo habían sido. De los 10 pacientes con MDR-TB, 6/487 (1,2%) nunca habían sido tratados con anterioridad y 4/31 (12,9%) lo habían sido. Once de los 28 pacientes nunca tratados con DR-TB-H eran españoles (3,4%) y 17 (10,2%) extranjeros (tabla 3). El 70% de los pacientes del estudio iniciaron el tratamiento de la TB con 4 fármacos (HRZE) y el 22% con un régimen de 3 fármacos (HRZ) (tabla 1).
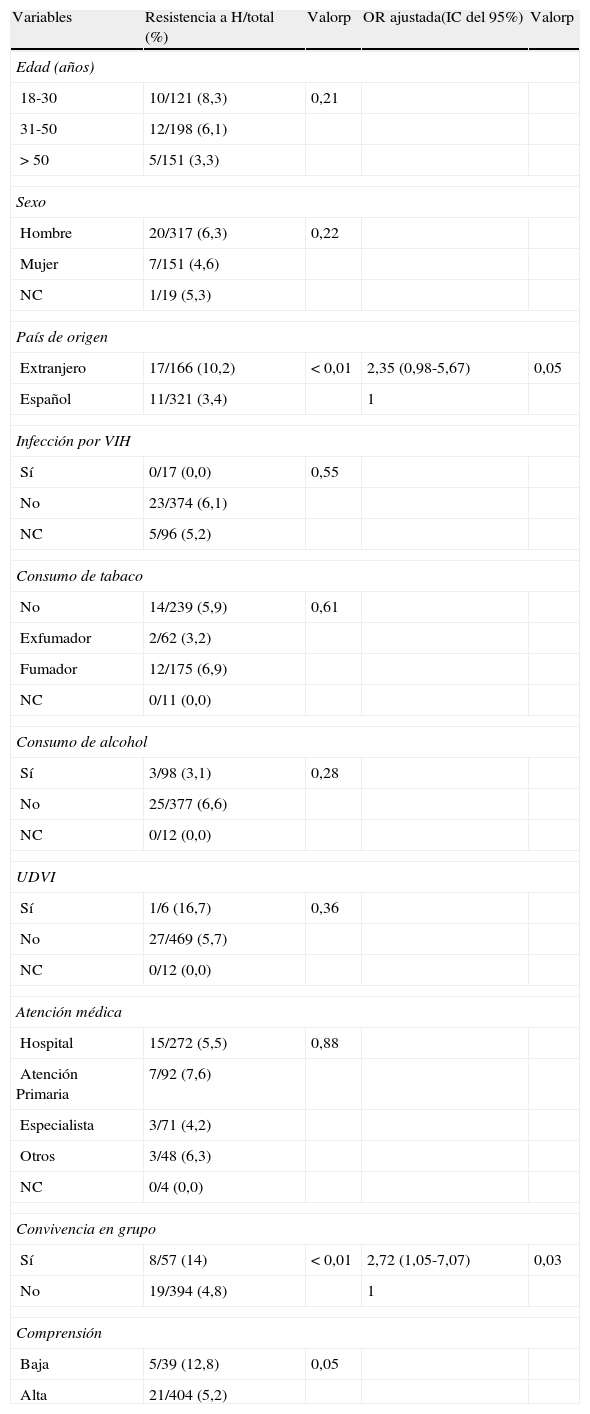
Resultaron ser factores de riesgo para DR-TB-H inicial ser extranjero y la convivencia en grupo (tabla 4). La edad menor de 50 años fue también un factor asociado a la DR-TB-H adquirida (tabla 5).
Factores predictores de resistencia a isoniazida en los pacientes sin tratamiento antituberculoso previo (N=487). Análisis univariado y multivariado
| Variables | Resistencia a H/total (%) | Valorp | OR ajustada(IC del 95%) | Valorp |
| Edad (años) | ||||
| 18-30 | 10/121 (8,3) | 0,21 | ||
| 31-50 | 12/198 (6,1) | |||
| > 50 | 5/151 (3,3) | |||
| Sexo | ||||
| Hombre | 20/317 (6,3) | 0,22 | ||
| Mujer | 7/151 (4,6) | |||
| NC | 1/19 (5,3) | |||
| País de origen | ||||
| Extranjero | 17/166 (10,2) | < 0,01 | 2,35 (0,98-5,67) | 0,05 |
| Español | 11/321 (3,4) | 1 | ||
| Infección por VIH | ||||
| Sí | 0/17 (0,0) | 0,55 | ||
| No | 23/374 (6,1) | |||
| NC | 5/96 (5,2) | |||
| Consumo de tabaco | ||||
| No | 14/239 (5,9) | 0,61 | ||
| Exfumador | 2/62 (3,2) | |||
| Fumador | 12/175 (6,9) | |||
| NC | 0/11 (0,0) | |||
| Consumo de alcohol | ||||
| Sí | 3/98 (3,1) | 0,28 | ||
| No | 25/377 (6,6) | |||
| NC | 0/12 (0,0) | |||
| UDVI | ||||
| Sí | 1/6 (16,7) | 0,36 | ||
| No | 27/469 (5,7) | |||
| NC | 0/12 (0,0) | |||
| Atención médica | ||||
| Hospital | 15/272 (5,5) | 0,88 | ||
| Atención Primaria | 7/92 (7,6) | |||
| Especialista | 3/71 (4,2) | |||
| Otros | 3/48 (6,3) | |||
| NC | 0/4 (0,0) | |||
| Convivencia en grupo | ||||
| Sí | 8/57 (14) | < 0,01 | 2,72 (1,05-7,07) | 0,03 |
| No | 19/394 (4,8) | 1 | ||
| Comprensión | ||||
| Baja | 5/39 (12,8) | 0,05 | ||
| Alta | 21/404 (5,2) | |||
H: isoniacida; IC: intervalo de confianza; NC: no consta; OR: odds ratio; UDVI: uso de drogas por vía intravenosa; VIH: virus de la inmunodeficiencia humana.
Los totales para edad, familia y comprensión no suman 28 porque se han perdido datos de 1 o 2 pacientes.
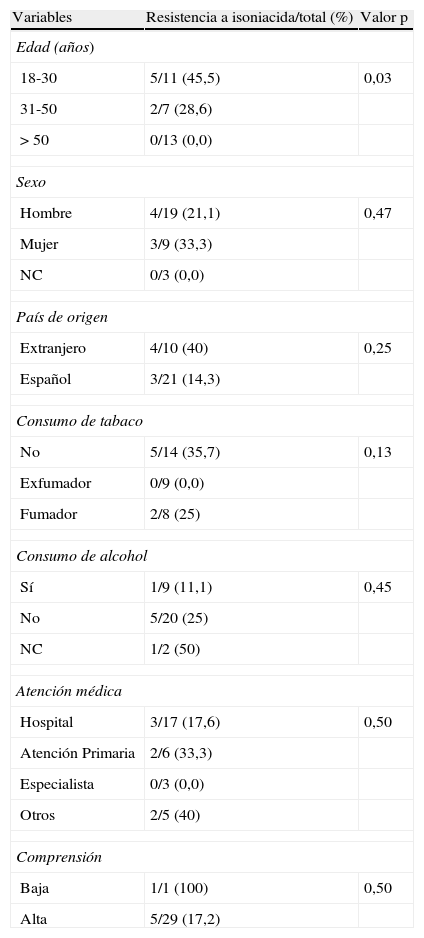
Factores predictores de resistencia a isoniacida en los pacientes con tratamiento antituberculoso previo (N=31). Análisis univariado
| Variables | Resistencia a isoniacida/total (%) | Valor p |
| Edad (años) | ||
| 18-30 | 5/11 (45,5) | 0,03 |
| 31-50 | 2/7 (28,6) | |
| > 50 | 0/13 (0,0) | |
| Sexo | ||
| Hombre | 4/19 (21,1) | 0,47 |
| Mujer | 3/9 (33,3) | |
| NC | 0/3 (0,0) | |
| País de origen | ||
| Extranjero | 4/10 (40) | 0,25 |
| Español | 3/21 (14,3) | |
| Consumo de tabaco | ||
| No | 5/14 (35,7) | 0,13 |
| Exfumador | 0/9 (0,0) | |
| Fumador | 2/8 (25) | |
| Consumo de alcohol | ||
| Sí | 1/9 (11,1) | 0,45 |
| No | 5/20 (25) | |
| NC | 1/2 (50) | |
| Atención médica | ||
| Hospital | 3/17 (17,6) | 0,50 |
| Atención Primaria | 2/6 (33,3) | |
| Especialista | 0/3 (0,0) | |
| Otros | 2/5 (40) | |
| Comprensión | ||
| Baja | 1/1 (100) | 0,50 |
| Alta | 5/29 (17,2) | |
NC: no consta.
Excluidas las variables con p>0,5.
El control adecuado de la TB precisa conocer periódicamente la prevalencia de las resistencias de MT a fármacos antituberculosos. El Sistema Nacional de Salud, a instancias del Área de Tuberculosis e Infecciones Respiratorias de la SEPAR, promovió en 2007 el Plan para la Prevención y Control de la Tuberculosis en España, en el que se recomienda el estudio sistemático con antibiograma9 pero los resultados publicados hasta ahora por la Red Nacional de Vigilancia Epidemiología (RENAVE) no recogen dicho dato10,11. Este es el primer estudio prospectivo de DR-TB realizado en España por una sociedad científica a partir de antibiogramas sistemáticos en una amplia cohorte de pacientes.
Nuestro estudio detectó una prevalencia aceptable de resistencia de MT a fármacos de primera línea, especialmente en la población autóctona (tablas 2 y 4), aunque superior a la descrita en estudios previos3,8, lo que probablemente se debe al fenómeno migratorio observado en España durante los últimos años. Destacamos que todos los casos de resistencia a R son MDR-TB, la ausencia de XDR-TB en contra de un estudio previo12 y la detección de factores de riesgo para DR-TB-H.
La tasa de DR-TB-H en nuestro estudio es superior a la de Portugal, similar a las de Francia y Dinamarca, e inferior a las de Italia y otros países centroeuropeos y nórdicos con mayor proporción de pacientes extranjeros13-15. El aumento de DR-TB-H, que se ha relacionado con la transmisión de la TB en población extranjera16, puede propagar la infección por cepas resistentes a H, sobre todo entre los sujetos más jóvenes17.
Las tasas de DR-TB-H y MDR-TB en los casos sin tratamiento antituberculoso previo reflejan fielmente la transmisión reciente de la TB, siendo la resistencia a H el primer escalón para el desarrollo de MDR-TB y XDR-TB3,18. La DR-TB-H inicial, es decir, la diagnosticada antes de iniciar el tratamiento de un paciente nuevo sin antecedentes de tratamiento antituberculoso previo19,20, puede incluir resistencia primaria o resistencia adquirida oculta pero suele ser transmitida18.
Hasta ahora, se desconocía la tasa actual de DR-TB-H inicial en España, mientras que la tasa de MDR-TB inicial se cifraba en el 2%21, superando la estimación previa del 0,2%3. Es inquietante que la tasa de DR-TB-H inicial en nuestro estudio sea superior a la publicada para España por organizaciones internacionales3,4 y por un estudio previo8. Aun así, las tasas iniciales de DR-TB-H y MDR-TB observadas son inferiores a las tasas medias de la CEE en el 2010 (7,8% y 2,6%, respectivamente), similares a las descritas para Gran Bretaña y Portugal, aunque inferiores a las de otros países centroeuropeos y nórdicos con mayor proporción de pacientes extranjeros22. En el contexto nacional, nuestras tasas son muy superiores a las referidas en una excelente revisión de estudios previos que publica, en pacientes nunca tratados, una tasa promedio del 3,0% en DR-TB-H, con gran variabilidad (0%-5,1%), y 0,37% en MDR-TB23. En estudios locales posteriores, la tasa de DR-TB-H inicial oscila del 1,9 al 4,4%, llegando al 5,3% en una comarca con abundante inmigración24-27, mientras la MDR-TB inicial no sobrepasa el 1,4%25,26.
La resistencia a fármacos antituberculosos en casos previamente tratados se suele etiquetar como resistencia adquirida, aunque también puede incluir a pacientes inicialmente infectados o reinfectados por una cepa resistente3,18. Nuestras tasas de DR-TB-H adquirida (22,6%) y MDR-TB adquirida (12,9%) son similares a las de otro estudio nacional8, inferiores a la media de la CEE, Rumanía, Bulgaria y Suecia, aunque superiores a las de otros países28.
La probabilidad de generar una cepa resistente durante el tratamiento de la TB es máxima en la fase inicial de tratamiento intensivo, cuado la población bacteriana es mayor29. El 70% de nuestros pacientes iniciaron su tratamiento con una pauta de 4 fármacos (HRZE), superando el porcentaje de un estudio previo12, mientras el 22% lo hicieron con pauta de 3 fármacos (HRZ), parte de ellos con visión directa negativa, cultivo positivo y antibiograma conocido. En pacientes nuevos sin enfermedad previa, se debe iniciar el tratamiento con 4 fármacos mantenidos hasta conocer el resultado del antibiograma y, si no se dispone de él, es necesario estimar la probabilidad de DR-TB para evitar el desarrollo de cepas resistentes30-33, ya que la incidencia de fracasos, abandonos, resistencia adquirida e incluso MDR-TB es mayor entre los casos con DR-TB inicial no identificada, sobre todo con resistencia a R y en menor proporción a H, que han sido tratados con pauta estándar, especialmente si es con solo 3 fármacos19,29,33.
En nuestro estudio, los pacientes nuevos sin tratamiento antituberculoso previo que son extranjeros o conviven en grupo tienen mayor riesgo de presentar resistencia inicial. La condición de extranjero es un conocido factor de riesgo de DR-TB y MDR-TB20,34-36 debido a que son inmigrantes por motivos económicos y proceden de países con limitados programas de control, mientras que la convivencia en grupo, que suele solaparse a otras condiciones20, puede facilitar una TB o una infección tuberculosa latente (ITL) por MT resistente a H36, en la que el tratamiento estándar de la ITL será inefectivo37.
Se estima que los pacientes del estudio son una muestra bastante representativa de la población tuberculosa española, aunque con menor tasa de pacientes infectados por VIH10,11. Nuestra proporción de nuevos casos sin tratamiento antituberculoso previo (94%), similar a la nacional (92,8%) y a la reseñada en estudios previos7,8,10,11,26, creemos que puede deberse al resultado satisfactorio del tratamiento en cerca del 90% de los casos7,12,26 —superior al nacional11 y a la media de la CEE y varios de sus países6,13—, que atribuimos tanto al seguimiento del paciente en el sistema sanitario público con escasas pérdidas y abandonos7,12, y a la disponibilidad de fármacos combinados a dosis fijas para el tratamiento de la TB, como a la tasa de extranjeros en nuestro estudio (34,1%), inferior a la de otros países europeos10-13.
Son varias las limitaciones del estudio. El estudio microbiológico no se ha centralizado, aunque se han utilizado métodos totalmente aceptados y reconocidos. El aislamiento de MT se ha realizado en cada hospital o en su centro de referencia mediante cultivo de la muestra en medio sólido o líquido, confirmado por cultivo en medio sólido, e identificación de MT por sonda genética o método automatizado. No hemos estudiado todos los antibiogramas en laboratorios de referencia, sino que siguiendo el proceso diagnóstico habitual en la red sanitaria nacional se han estudiado por métodos reconocidos para detectar con fiabilidad la resistencia a H y R38, la mayoría de ellos mediante BACTEC™ MGIT 960 y el resto por el método de las proporciones. Otras limitaciones son que no han participado en el estudio 4 CC. AA. ni la población reclusa, sin distorsionar, a nuestro juicio, la representatividad de la muestra10.
En conclusión, los resultados de este estudio prospectivo muestran un ligero incremento de la resistencia a fármacos antituberculosos en España, aumento que podría deberse a la inmigración masiva observada durante los últimos años en nuestro país. Las tasas de resistencia a H y de MDR-TB en pacientes sin antecedentes de tratamiento antituberculoso previo indican la necesidad de una vigilancia sistemática. Finalmente, concluimos que los pacientes nuevos sin tratamiento previo de TB que procedan de otros países y los que conviven en grupo tienen mayor riesgo de ser resistentes a H.
FinanciaciónEstudio financiado por la Beca número 886 de la convocatoria de Becas SEPAR 2008 de ayudas a la investigación.
Conflicto de interesesLos autores niegan conflicto de intereses.
N. Altet (Unidad Prevención y Control Tuberculosis, Barcelona); F. Álvarez-Navascués (H. San Agustín, Avilés, Asturias); M. Barrón (H. San Millán-San Pedro, Logroño); R. Blanquer (H. Dr. Peset, Valencia); A. Bustamante (H. Sierrallana, Torrelavega); J.L. Calpe (H. La Marina Baixa, Villajoyosa); J.A. Caminero (Complejo Hospitalario Dr. Negrín, Las Palmas de Gran Canaria); F. Cañas (H. Insular de Gran Canaria, Las Palmas de Gran Canaria); M. Casals (Agencia de Salud Pública de Barcelona, Barcelona); X. Casas (H. Sant Boi, Barcelona); J.A. Caylà (Agencia de Salud Pública de Barcelona, Barcelona); M.L. de Souza (Unidad Prevención y Control Tuberculosis, Barcelona); J. Gallardo (H. Universitario de Guadalajara, Guadalajara); M. Gallego (Corporación Sanitaria Parc Taulí, Sabadell); F.J. García (H. Universitario de la Princesa, Madrid); J.M. García-García (H. San Agustín, Avilés, Asturias); J.A. Gullón (Hospital Universitario de Canarias, La Laguna); M.A. Jiménez (Unidad Prevención y Control Tuberculosis, Barcelona); T. Lloret (H. General Universitario de Valencia, Valencia); M. Marín (H. General de Castellón, Castellón); J.F. Medina (H Universitario Virgen del Rocío, Sevilla); C. Milà (Unidad Prevención y Control Tuberculosis, Barcelona); I. Mir (H. Son Llàtzer, Palma de Mallorca); V. Moreno (H. Carlos III, Madrid); T. Pascual (H. de Cabueñes, Gijón); A. Penas (Complejo Hospitalario Xeral-Calde, Lugo); T. Rodrigo (Fundación Respira de SEPAR); J. Ruiz-Manzano (H. Universitario Germans Trías i Pujol, Badalona); J. Sala (H. Universitario Joan XXIII, Tarragona); P. Sánchez (H. del Mar, Barcelona); F. Sanz (H. General Universitario de Valencia, Valencia); E. Valencia (H. Carlos III, Madrid); A. Vargas (H. Universitario Puerto Real, Cádiz); R. Vidal (H. Vall D’Hebrón, Barcelona); M.A. Villanueva (H. San Agustín, Avilés, Asturias).