Se define como oxigenoterapia el uso terapéutico del oxígeno y consiste en su administración a concentraciones mayores de las que se encuentran en el aire ambiente, con la intención de tratar o prevenir las manifestaciones de la hipoxia. Esta medida terapéutica ha demostrado aumentar la supervivencia en los enfermos con enfermedad pulmonar obstructiva crónica (EPOC) e insuficiencia respiratoria. A pesar de que este concepto se ha extendido por analogía a la insuficiencia respiratoria crónica originada por otras enfermedades respiratorias y no respiratorias, la efectividad de la oxigenoterapia continua no está demostrada en otras entidades. La oxigenoterapia no se ha demostrado efectiva en términos de supervivencia en pacientes con EPOC e hipoxemia moderada. Tampoco hay consenso sobre su empleo durante las desaturaciones nocturnas en EPOC y durante las desaturaciones al esfuerzo. La elección de la fuente de oxígeno se debe realizar por criterios técnicos, de comodidad y adaptabilidad del paciente y de coste. Se debería ajustar el flujo para conseguir una adecuada corrección de la saturación transcutánea de oxihemoglobina.
Oxygen therapy is defined as the therapeutic use of oxygen and consists of administering oxygen at higher concentrations than those found in room air, with the aim of treating or preventing hypoxia. This therapeutic intervention has been shown to increase survival in patients with chronic obstructive pulmonary disease (COPD) and respiratory failure. Although this concept has been extended by analogy to chronic respiratory failure caused by respiratory and non-respiratory diseases, continuous oxygen therapy has not been shown to be effective in other disorders. Oxygen therapy has not been shown to improve survival in patients with COPD and moderate hypoxaemia, nor is there consensus regarding its use during nocturnal desaturations in COPD or desaturations caused by effort. The choice of the oxygen source must be made on the basis of criteria such as technical issues, patient comfort and adaptability and cost. Flow must be adjusted to achieve appropriate transcutaneous oxyhaemoglobin saturation correction.
La oxigenoterapia es un tratamiento antiguo, pero sin duda continúa siendo una de las medidas más importantes en el manejo del paciente con enfermedad respiratoria crónica evolucionada. El objetivo básico de la oxigenoterapia crónica es corregir la hipoxemia grave que suelen presentar estos pacientes en las fases avanzadas de la enfermedad, mejorando en último término la oxigenación tisular.
El descubrimiento del oxígeno se atribuye a Joseph Priestley en 1772, que al calentar óxido de mercurio al calor del sol en una vasija liberó gas, que resultó ser oxígeno. Sin embargo, la primera utilización terapéutica del oxígeno se atribuye a Chaussier, quien en 1780 lo aplicó a pacientes disneicos y a recién nacidos cianóticos. En 1887 el Dr. Holzapple lo utilizó para tratar a un joven aquejado de neumonía, generando oxígeno a partir de clorato potásico y dióxido de manganeso. A finales del sigloxix se descubrió el proceso para producir aire líquido por compresión y enfriamiento, pudiendo aislar oxígeno por destilación fraccional del aire líquido. A lo largo del sigloxx se demostraron los efectos beneficiosos sobre algunas de las consecuencias más habituales de la enfermedad (disminución de la policitemia, control de los episodios de cor pulmonale, reducción en el número y días de hospitalización), aunque no es hasta la década de los ochenta cuando varios estudios establecieron las bases para los criterios de selección de pacientes que se beneficiarían de la utilización de la oxigenoterapia continua domiciliaria (OCD) y que aún hoy son de aplicación1.
Como veremos a lo largo de esta normativa, aparte de algunas indicaciones claramente establecidas, hay otras situaciones en las que no existe consenso para la utilización de la oxigenoterapia. Es reseñable que algunas de estas indicaciones están basadas en trabajos de hace más de 30años, y en algunos casos con un número limitado de pacientes. Esta normativa pretende ser un instrumento sencillo y útil que ayude en la toma de decisión en la prescripción de este tipo de terapia. Para clasificar la calidad de la evidencia y la fuerza de las recomendaciones disponibles, en las cuestiones más relevantes se ha seguido el sistema GRADE (tabla 1). Además, siempre que ha sido posible, al final de cada apartado se ha realizado una recomendación, a partir de lo explicado previamente y la evidencia disponible.
Clasificación de las recomendaciones y calidad de la evidencia según el sistema GRADE
| Grado de recomendación | Nivel de evidencia | Implicaciones |
| Recomendación consistentea, calidad evidencia alta | ECA bien realizados, de modo excepcional EO bien realizados | Se puede aplicar a la mayoría de los pacientes en la mayoría de las ocasiones |
| Recomendación consistentea, calidad evidencia moderada | ECA con limitaciones o EO bien realizados con defectos importantes | Se puede aplicar a la mayoría de los pacientes en la mayoría de las ocasiones |
| Recomendación consistentea, calidad evidencia baja | Al menos un resultado importante de ECA o EO con defectos importantes | Puede cambiar cuando se disponga de una evidencia mayor |
| Recomendación consistentea, calidad evidencia muy baja | Al menos un resultado importante de observaciones clínicas no sistemáticas o evidencia muy indirecta | Puede cambiar cuando se disponga de una evidencia mayor |
| Recomendación débilb, calidad evidencia alta | ECA bien realizados, de modo excepcional EO bien realizados | Puede diferir dependiendo de las circunstancias o los pacientes |
| Recomendación débilb, calidad evidencia moderada | ECA con limitaciones o EO bien realizados con defectos importantes | Otras opciones pueden ser mejores para algunos pacientes en determinadas circunstancias |
| Recomendación débilc, calidad evidencia baja | Al menos un resultado importante de ECA o EO con defectos importantes | Otras opciones pueden ser de igual manera razonables |
| Recomendación débild, calidad evidencia muy baja | Al menos un resultado importante de observaciones clínicas no sistemáticas o evidencia muy indirecta | Otras opciones pueden ser de igual manera razonables |
ECA: estudios controlados y aleatorizados; EO: estudios observacionales.
Fuente: GRADE Working Group. Grading of recommendations of assessment development and evaluations. Disponible en: http://www.gradeworkinggroup.org/
La función principal del aparato respiratorio consiste en mantener un adecuado intercambio pulmonar de gases fisiológicos. El parámetro de oxigenación arterial que evalúa la función pulmonar es la presión parcial de oxígeno en sangre arterial (PaO2), ya que es la función intercambiadora de gases del pulmón la que generalmente determina su valor. Los valores normales de PaO2 en el adulto varían ligeramente con la edad y se sitúan entre 100mmHg (13,6kPa; 1kPa=7,5mmHg) y 96mmHg (12,8kPa) a los 20 y 70años, respectivamente. Los valores de la presión parcial de dióxido de carbono en sangre arterial (PaCO2) también disminuyen con la edad (4mmHg entre los 20 y los 70años), oscilando entre 38 y 34mmHg, respectivamente, y con una media de 37±3mmHg (4,9kPa).
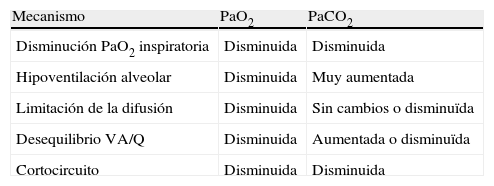
En rigor, hipoxemia se refiere a una disminución del contenido de O2 y/o PaO2. Sin embargo, esta definición amplia se presta a confusión, ya que la relación entre PaO2 y contenido de O2 no es lineal y depende de muchas variables: la PaO2 puede descender sin cambios significativos en su contenido, mientras que el contenido puede estar muy disminuido sin cambios en la PaO2 (anemia o intoxicación con CO). Para evitar estos problemas, nos atendremos a la acepción de uso más difundido: hipoxemia es la disminución de la PaO2 por debajo de los límites normales para la edad del sujeto2. En la práctica clínica se dice que existe hipoxemia arterial cuando la PaO2 es inferior a 80mmHg (10,7kPa), e hipercapnia arterial cuando la PaCO2 es superior a 45mmHg (6,0kPa), respirando aire ambiente y a nivel del mar. La disminución de la PaO2 puede deberse a múltiples factores (tabla 2). La insuficiencia respiratoria se define cuando los valores de PaO2 se sitúan por debajo de 60mmHg (8,0kPa). Para demostrar la existencia de insuficiencia respiratoria es necesario practicar una gasometría arterial mediante punción transcutánea de una arteria periférica, preferentemente la radial. Como técnica alternativa se puede emplear la pulsioximetría, aceptándose como valor indicativo de insuficiencia respiratoria una saturación arterial de oxihemoglobina (SpO2) inferior al 90%. Los valores de la SpO2 son mucho más variables que los de la PaO2, pueden estar influidos por factores extrapulmonares y no aportan información sobre la PaCO2 ni el pH3.
Causas de hipoxemia e hipercapnia
| Mecanismo | PaO2 | PaCO2 |
| Disminución PaO2 inspiratoria | Disminuida | Disminuida |
| Hipoventilación alveolar | Disminuida | Muy aumentada |
| Limitación de la difusión | Disminuida | Sin cambios o disminuïda |
| Desequilibrio VA/Q | Disminuida | Aumentada o disminuïda |
| Cortocircuito | Disminuida | Disminuida |
PaCO2: presión arterial de dióxido de carbono; PaO2: presión arterial de oxígeno; VA/Q: relación ventilación-perfusión pulmonar.
De Soler y Rodríguez-Roisin3.
La hipoxia se define como la disminución del aporte de oxígeno a las células, lo que limita la producción de energía a niveles por debajo de los requerimientos celulares. Puede generarse por diversos mecanismos (tabla 3). Del balance entre los efectos nocivos de la hipoxia y los efectos compensatorios que ella misma desencadena depende que se mantenga el aporte de oxígeno a los tejidos vitales. Los diversos órganos muestran distintos grados de susceptibilidad a la hipoxia, dependiendo de la relación entre su actividad metabólica, su flujo sanguíneo y las posibilidades del órgano de modificar estos factores en caso de necesidad. Mientras más rápida es la caída de la PaO2, mayores son los trastornos que se producen, porque los mecanismos de compensación agudos son de capacidad limitada. En cambio, cuando la hipoxemia es de instauración lenta (enfermedades crónicas pulmonares y cardíacas), hay tiempo para el desarrollo de mecanismos de compensación eficaces4.
Mecanismos fisiopatológicos de la hipoxia
| Hipoxémica | Disminución de la FiO2 Shunt derecha-izquierda Disbalance VA/Q Hipoventilación alveolar Alteración de la difusión Bajo CvO2 |
| Anémica | Disminución de hemoglobina Intoxicación por CO Metahemoglobinemia |
| Isquémica | Reducción del flujo sanguíneo (shok, insuficiencia cardíaca) |
| Toxicidad tisular | Intoxicación por cianuro |
| Consumo excesivo de O2 tisular | Fiebre alta, ejercicio muscular intenso |
CO: monóxido de carbono; CvO2: contenido de oxígeno en sangre venosa; FiO2: fracción inspiratoria de oxígeno; VA/Q: relación ventilación-perfusión pulmonar.
De Rodríguez-Roisin2.
La disminución de la PaO2 produce un aumento de la ventilación mediada por los quimiorreceptores aórticos y carotídeos. A nivel del corazón, se produce aumento tanto de la frecuencia como de la fuerza de contracción, lo que aumenta el gasto cardíaco. El sistema excitoconductor también se ve afectado, aumentando la frecuencia de arritmias de distinto tipo y gravedad. La circulación pulmonar reacciona en forma diferente al resto de los vasos del organismo: la hipoxia alveolar produce un aumento local de la resistencia vascular pulmonar (que determina el desarrollo de una hipertensión pulmonar), básicamente por acción directa sobre los vasos pulmonares precapilares, constituyendo el principal mecanismo de redistribución selectiva del flujo sanguíneo pulmonar a las zonas mejor ventiladas. En el cerebro, el aumento del flujo es proporcionalmente mayor que el aumento del gasto cardíaco, debido a la disminución de la resistencia vascular cerebral que produce la hipoxia. El tejido cerebral tiene, junto con el miocardio, la más alta sensibilidad del organismo a la falta de oxígeno. Otra respuesta del organismo ante la hipoxia es el aumento del volumen total de glóbulos rojos por un incremento de la producción de eritropoyetina, principalmente por el riñón. Este aumento de la capacidad de transporte de oxígeno tiene un efecto compensador, ya que si bien cada glóbulo rojo lleva menos oxígeno que lo normal, un mayor número de glóbulos rojos aminora el déficit de transporte global de la sangre5.
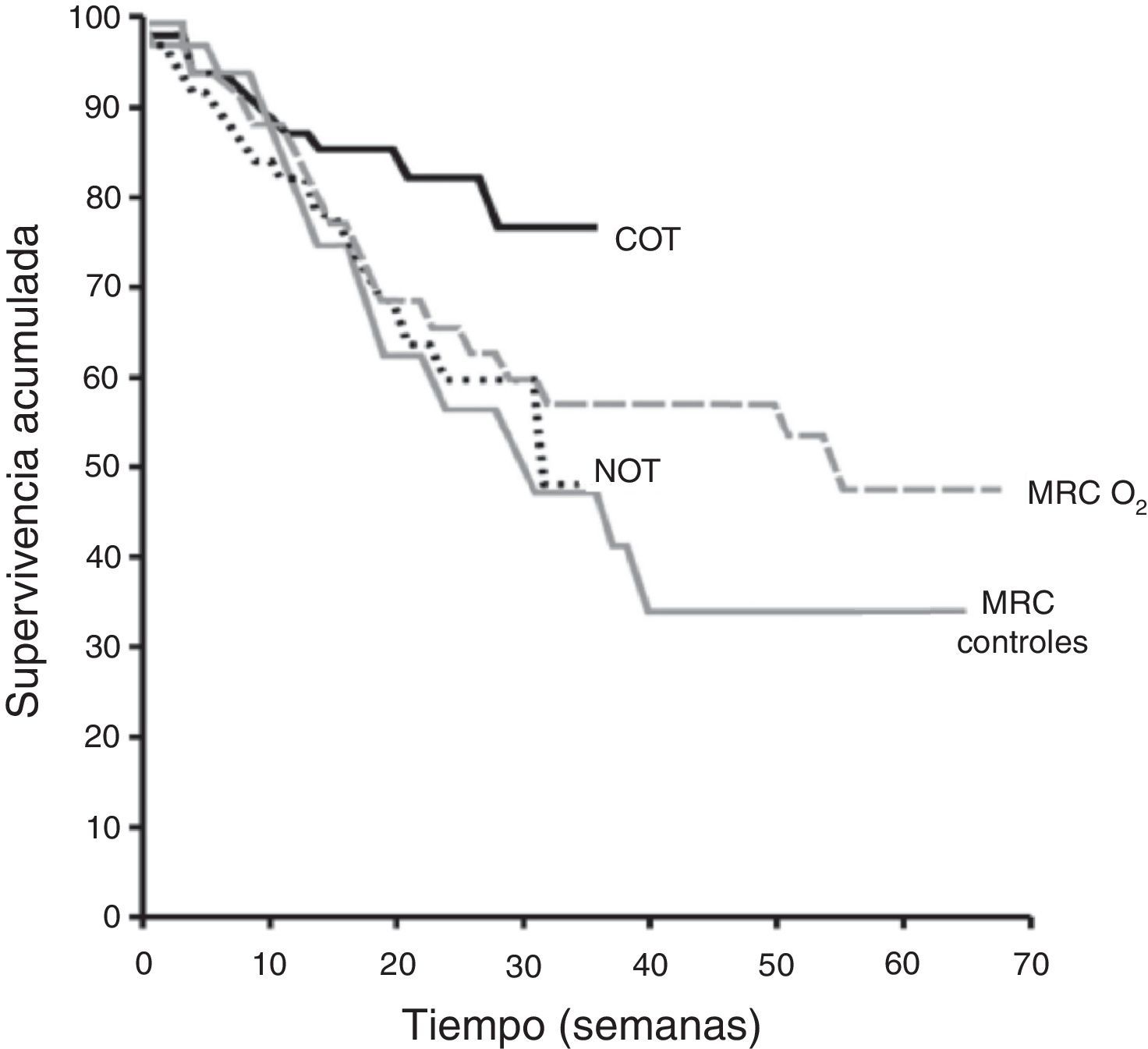
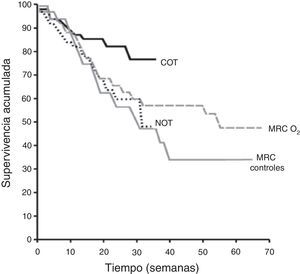
Efectos de la oxigenoterapiaPacientes con hipoxemia basalSupervivenciaHipoxemia grave. La evidencia disponible de prescripción de la OCD procede de 2ensayos clínicos aleatorizados de pacientes con EPOC publicados hace casi 30años: el estudio del Medical Research Council (MRC)6 y el Nocturnal Oxygen Therapy (NOTT)7 (fig. 1). El estudio del MRC comparó el uso de oxígeno durante 15h al día (incluyendo la noche) con tratamiento habitual sin oxígeno. Participaron 87pacientes con EPOC grave menores de 70años con hipoxemia grave (PaO2, 49-52mmHg, 6,5-6,9kPa), hipercapnia (PaCO2, 56-59mmHg, 7,5-7,7kPa) e hipertensión pulmonar leve. La supervivencia a los 3años del grupo con oxigenoterapia fue del 55%, frente al 33% en el grupo control (p<0,05). El otro estudio, el NOTT7, en el que participaron 203sujetos, tenía como objetivo evaluar si la oxigenoterapia continua era superior a la oxigenoterapia nocturna. Los participantes del grupo con oxigenoterapia continua acabaron recibiendo oxígeno 17,7±4,8h al día, mientras que los pacientes del grupo de oxigenoterapia nocturna recibieron 12,0±2,5h al día. Durante el seguimiento (media de 19,3meses) la supervivencia en el grupo de oxigenoterapia continua fue mejor que en el grupo de oxigenoterapia nocturna (fig. 1). En conjunto, los resultados de estos 2ensayos sugieren que en pacientes con EPOC e hipoxemia grave en reposo la oxigenoterapia produce un beneficio claro de supervivencia cuando se administra al menos 15h al día, incluyendo la noche.
Supervivencia a largo plazo con oxígeno de varones con EPOC e hipoxemia grave. Estudios controlados de oxigenoterapia a largo plazo del Medical Research Council (MRC) y el Nocturnal Oxygen Therapy (NOTT).COT: grupo con oxigenoterapia continua del estudio del NOTT; MRC controles: grupo que no recibió oxígeno en el estudio del MRC; MRC O2: grupo con oxigenoterapia 15h al día, incluyendo la noche, del estudio del MRC; NOT: grupo con oxigenoterapia nocturna del estudio del NOTT.
De Report of the Medical Research Council Working Party6 y Nocturnal Oxygen Therapy Trial group7.
A diferencia de los pacientes con EPOC, no hay prueba alguna de que la oxigenoterapia influya en la supervivencia a largo plazo ni en la calidad de vida relacionada con la salud de los pacientes con enfermedades intersticiales e hipoxemia moderada o grave8. En un estudio en pacientes con fibrosis pulmonar idiopática (FPI) no se observaron diferencias en la calidad de vida relacionada con la salud entre pacientes que recibían oxígeno y sin oxígeno9.
Hipoxemia moderada. En contraste con los resultados anteriores la oxigenoterapia no se ha demostrado efectiva en términos de supervivencia en pacientes con EPOC e hipoxemia moderada7,10–12. En un estudio de 135pacientes con una PaO2 entre 56 y 65mmHg (7,5-8,7kPa), se aleatorizaron a recibir oxígeno 17h al día o no recibir oxígeno suplementario. La supervivencia no fue distinta entre ambos grupos durante el periodo de observación (media de 41meses)11. En otro estudio orientado a determinar los efectos de la oxigenoterapia nocturna en pacientes con EPOC con hipoxemia diurna de leve a moderada (PaO2 56-69mmHg [7,4-9,2kPa]) y desaturaciones nocturnas, en los que se había descartado un síndrome de apneas-hipopneas durante el sueño (SAHS), no hubo diferencias en la supervivencia ni en la hemodinámica pulmonar10. En otro pequeño ensayo12 de 28pacientes con EPOC grave e hipoxemia moderada (PaO2, 66±6mmHg [8,5±0,8kPa]) se aleatorizaron los pacientes a recibir oxígeno 15h al día o sin oxígeno suplementario. La mortalidad fue similar en ambos grupos tras un seguimiento de 3años.
Hemodinámica pulmonarEn un clásico estudio13 se evaluaron 16pacientes con EPOC grave; todos tenían un cateterismo derecho previo (T1) 47±28meses antes de iniciar la oxigenoterapia, y en ese momento su PaO2 era de 59±9mmHg y la presión media de la arteria pulmonar (PAPm), de 23±7mmHg. Al inicio del tratamiento (T2) se repitió el cateterismo; entonces la PaO2 era de 50±7mmHg y la PAPm de 28±7 (p<0,008). Recibieron oxígeno 15-18h al día, y a los 31±19meses (T3) se les practicó un nuevo cateterismo. De T2 a T3 la PaO2 se mantuvo estable, mientras que PAPm bajó a 25±7mmHg (p<0,05). En el estudio más largo14 con hemodinámica de pacientes con EPOC e hipoxemia (PaO2 55±6mmHg) que recibieron oxígeno (14,7h al día de media), se midió la PAPm cada 2años durante 6años. En los 39participantes a los que se les hizo cateterismo derecho a los 2años, la PAPm disminuyó ligeramente de 25±8 a 23±6mmHg. En los 12pacientes que completaron los 6años, la PAPm se redujo de 25±7 a 21±4mmHg a los 2años, pero a partir de entonces volvió a los valores basales (PAPm 26±7 y 26±6mmHg a los 4 y 6años de seguimiento). Los autores concluyeron que la administración de oxígeno provocaba en los pacientes con EPOC una disminución a corto plazo de la PAPm seguida de una estabilización a pesar de la progresión de la obstrucción.
Pacientes con hipoxemia durante la actividad físicaSupervivenciaVarios estudios sugieren que la desaturación durante el ejercicio es un indicador de mal pronóstico en los pacientes con EPOC o con FPI10,15–24. Sin embargo no existe evidencia de que la oxigenoterapia tenga efecto sobre la supervivencia en estos pacientes. En un subestudio retrospectivo de 471pacientes con hipoxemia en ejercicio del brazo que recibió tratamiento médico en el National Emphysema Treatment Trial (NETT) no se encontraron diferencias en la supervivencia entre sujetos que hubiesen sido tratados con oxígeno o sin él. Por tanto, aunque la hipoxemia de esfuerzo en pacientes con EPOC o FPI que permanecen normoxémicos en reposo augura un mal pronóstico, no hay información prospectiva del efecto de la oxigenoterapia en la supervivencia de estos pacientes.
Capacidad de esfuerzoEl oxígeno suplementario mejora la capacidad de esfuerzo a corto plazo de pacientes con EPOC, fibrosis quística y enfermedades intersticiales que solo tienen hipoxemia con el ejercicio25–30. El mecanismo parece deberse a sus efectos sobre el patrón ventilatorio, como parece demostrar un estudio en el que el oxígeno suplementario aumentó la tolerancia al esfuerzo de resistencia, redujo la frecuencia respiratoria y la hiperinsuflación dinámica durante el ejercicio en pacientes con EPOC e hipoxemia leve31. Es interesante indicar que la saturación cerebral disminuye durante el ejercicio en pacientes con desaturaciones durante el mismo32. El oxígeno suplementario mejora la oxigenación cerebral y, por tanto, existe la posibilidad de que ayude a mantener la función cerebral durante el esfuerzo.
Pocos estudios han analizado el efecto a largo plazo de la oxigenoterapia sobre la capacidad de esfuerzo en pacientes que desaturan durante el ejercicio. Un estudio de 12semanas, doble ciego, aleatorizado, cruzado comparó la oxigenoterapia con aire en 26pacientes con SpO2 en reposo casi normal (94±2,1%) y desaturación en ejercicio. Se encontró que el oxígeno tenía un efecto agudo sobre la distancia recorrida en 6min, pero no tuvo beneficio a largo plazo en la capacidad de esfuerzo, la disnea o la calidad de vida. En otro pequeño ensayo de 28pacientes con EPOC grave e hipoxemia moderada (PaO2, 66±6mmHg [8,5±0,8kPa]) se aleatorizó a los pacientes a recibir oxígeno 15h al día o no recibir oxígeno, durante 3años. Al año, la resistencia al ejercicio en cicloergómetro y disnea de esfuerzo eran mejores en los pacientes que recibieron oxígeno10. Por tanto, hay poca información —y contradictoria— sobre los beneficios a largo plazo de la administración de oxígeno en la capacidad de esfuerzo.
Los estudios sobre el efecto de la oxigenoterapia sobre la eficacia de la rehabilitación pulmonar en pacientes con hipoxia durante el ejercicio sin hipoxemia basal son contradictorios, posiblemente por variaciones metodológicas33–36. Un reciente metaanálisis concluyó que el oxígeno parecía aumentar los beneficios de la rehabilitación en pacientes con hipoxemia de esfuerzo, aunque reconocían la escasa y limitada calidad de la evidencia disponible37.
Calidad de vida relacionada con la saludEl suplemento de oxígeno durante 12semanas en pacientes con desaturación durante el ejercicio mejoró la calidad de vida según cuestionarios específicos y generales, así como la ansiedad y la depresión. Sin embargo, no hubo correlación entre el efecto agudo del oxígeno en la distancia o en la disnea de la prueba de marcha de 6min (PM6M) y la mejoría según los citados cuestionarios, y el 41% de los que mejoraron en los cuestionaros rechazaron seguir con oxígeno37,38.
Pacientes con hipoxemia nocturnaSupervivenciaExisten datos retrospectivos que indican que la supervivencia puede estar disminuida en pacientes con desaturación nocturna39, pero solo unos pocos estudios han examinado el impacto del oxígeno suplementario nocturno sobre la mortalidad en los pacientes con EPOC y desaturación nocturna11,39,40. En pacientes con hipoxemia leve o moderada durante el día (PaO2, 56-69mmHg, 7,5-7,9kPa) y desaturación nocturna no se ha observado mayor supervivencia con oxigenoterapia nocturna10,39.
HemodinámicaAlgunos investigadores han comunicado elevaciones de la resistencia vascular pulmonar y de la PAPm en pacientes con desaturación nocturna41, pero otros no42. De manera similar, los resultados de los estudios con oxigenoterapia nocturna sobre la hemodinámica pulmonar son discrepantes10,41. En un estudio de pacientes con desaturación nocturna aislada, el grupo con OCD mostró un descenso de la PAPm con terapia de oxígeno suplementario en comparación con un incremento en el grupo sin oxígeno41. Por el contrario, otro estudio no encontró cambios en la PAPm de pacientes con desaturación nocturna10.
Extrasistolia ventricularLas extrasístoles ventriculares se presentan en el 64% de los pacientes con EPOC durante el sueño43,44 y son particularmente frecuentes en aquellos con hipoxemia nocturna43. Sin embargo, en un estudio, el oxígeno suplementario no disminuyó el número medio de extrasístoles ventriculares del grupo tratado, aunque 4 de los 10sujetos experimentaron una disminución del 50% en la frecuencia de extrasístoles ventriculares41.
Calidad del sueñoLa calidad del sueño es deficiente en pacientes con EPOC41,45–47. Los resultados de los estudios que investigaron los efectos de la oxigenoterapia nocturna en la calidad del sueño son limitados y contradictorios, con un estudio que demuestra una mejoría de la calidad de sueño45 y otro que no encuentran este beneficio48.
RecomendaciónEn pacientes con EPOC e insuficiencia respiratoria en reposo la oxigenoterapia produce un aumento de la supervivencia cuando se administra al menos 15h al día, incluyendo la noche. No hay pruebas de que este efecto positivo sobre la supervivencia se produzca en insuficiencia respiratoria de otras etiologías o en pacientes con EPOC con hipoxemias más moderadas.
Indicaciones de la oxigenoterapia continua domiciliaria en patología respiratoriaEnfermedad pulmonar obstructiva crónicaLa oxigenoterapia es la única intervención, además de la supresión del tabaquismo, que reduce la mortalidad en pacientes con EPOC e hipoxemia grave (recomendación consistente, calidad de evidencia alta). Además, atenúa la insuficiencia cardíaca derecha originada por el cor pulmonale, mejora la función neuropsicológica y aumenta la tolerancia al ejercicio y la capacidad para realizar actividades de la vida cotidiana (recomendación consistente, calidad de la evidencia moderada).
Oxigenoterapia continuaLa administración de oxígeno corrige la hipoxemia solo durante su aplicación, sin efecto residual. Cuando se suprime el aporte suplementario de oxígeno, reaparece la hipoxemia, por lo que para obtener un efecto sostenido es necesario prolongar el tiempo de administración durante más de 15h al día.
La indicación de oxigenoterapia continua en pacientes con hipoxemia grave se establece por su efecto sobre la supervivencia. Como ya se ha comentado previamente, los estudios NOTT7 y MRC6 demostraron que la oxigenoterapia aumenta la supervivencia media de los pacientes con EPOC cuando se administra un tiempo mínimo de 15h diarias y a un flujo suficiente para obtener una PaO2 de más de 60mmHg, correspondiente a una SpO2 ≥92%, sin aumentar la PaCO2. Estos 2estudios demuestran que la OCD mejora la supervivencia de pacientes con EPOC y una PaO2<55mmHg (7,3kPa)1. Los criterios de selección del estudio NOTT también incluían a pacientes con una PaO2 entre 55 y 60mmHg con evidencia de cor pulmonale, insuficiencia cardíaca derecha o poliglobulia, en los que igualmente se demostró un efecto beneficioso de la oxigenoterapia sobre su supervivencia7.
Varios estudios han valorado la utilidad de la administración de oxígeno a pacientes con PaO2 comprendidas entre 56 y 65mmHg (7,4-8,7kPa), siendo los resultados uniformemente pobres11,12. Górecka et al.11 no identificaron un incremento de la supervivencia a los 3años entre un grupo de enfermos con una PaO2 de 56-65mmHg tratados con oxigenoterapia frente a un grupo control. De igual modo, Haidl et al.12 tampoco hallaron una mayor supervivencia a los 3años en un pequeño grupo de pacientes con EPOC e hipoxemia leve-moderada tratados con oxígeno con respecto a un grupo control, pese a identificar una ligera mejoría en la tolerancia al ejercicio y en la disnea. Por todo ello, y en función de la información disponible hasta el momento, la oxigenoterapia continua no parece mejorar la supervivencia de pacientes con EPOC e hipoxemia leve-moderada1. Sin embargo, los estudios mencionados presentan diversas limitaciones. Carecen de la potencia suficiente para descartar un efecto beneficioso y, además, cabe la posibilidad de que para producir un beneficio se requiera un mayor tiempo de uso de la oxigenoterapia (que en ambos estudios no alcanzó la media de 15h diarias). Tampoco permiten descartar la existencia de subgrupos de pacientes respondedores a la oxigenoterapia y no valoran a pacientes con EPOC y comorbilidades, principalmente cardiovasculares y cerebrovasculares, que podrían ser más sensibles al efecto de esta intervención.
Ante la ausencia de un efecto demostrado sobre la supervivencia en este grupo de enfermos, se necesita más información sobre el efecto de la oxigenoterapia sobre otras variables clínicas49,50. Pese a la gran heterogeneidad de los ensayos clínicos analizados, un reciente metaanálisis identifica que la oxigenoterapia produce una mejoría significativa de la disnea51. Además, datos muy parciales sugieren que podría mejorar la calidad de vida relacionada con la salud, incrementar la tolerancia al ejercicio y disminuir la frecuencia de hospitalizaciones, así como mejorar la depresión y la función cognitiva de estos pacientes49,52. Todavía no se ha demostrado con suficiente solidez su hipotético papel en la estabilización de la hipertensión pulmonar y en la disminución de arritmias y alteraciones electrocardiográficas sugestivas de isquemia miocárdica13,14. El estudio LOTT (NCT00692198) posiblemente aportará información relevante sobre estos aspectos en los próximos años.
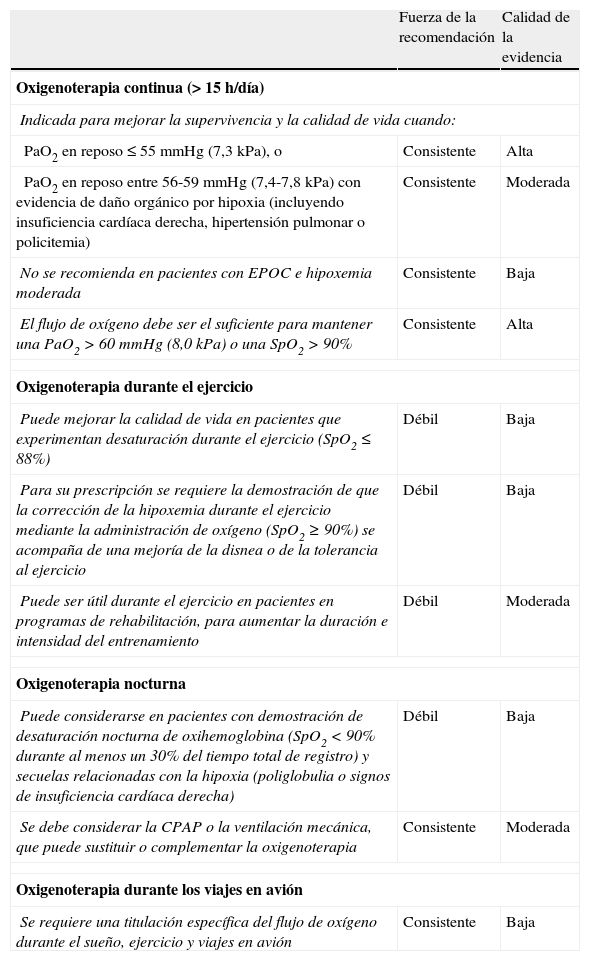
Por todo ello, la oxigenoterapia continua está indicada en pacientes con EPOC que, en reposo y respirando aire ambiente, mantienen una PaO2 inferior o igual a 55mmHg (recomendación consistente, calidad de evidencia alta), y también en aquellos enfermos que presentan una PaO2 entre 55 y 59mmHg, pero además muestran evidencia clínica o electrocardiográfica de hipertensión pulmonar, un hematocrito superior al 55% o signos de insuficiencia cardíaca derecha (recomendación consistente, calidad de la evidencia moderada). No se recomienda la oxigenoterapia continua en pacientes con EPOC e hipoxemia moderada (recomendación consistente, calidad de la evidencia baja) (tabla 4)53–56.
Indicaciones de oxigenoterapia en pacientes con enfermedad pulmonar obstructiva crónica
| Fuerza de la recomendación | Calidad de la evidencia | |
| Oxigenoterapia continua (>15h/día) | ||
| Indicada para mejorar la supervivencia y la calidad de vida cuando: | ||
| PaO2 en reposo ≤55mmHg (7,3kPa), o | Consistente | Alta |
| PaO2 en reposo entre 56-59mmHg (7,4-7,8kPa) con evidencia de daño orgánico por hipoxia (incluyendo insuficiencia cardíaca derecha, hipertensión pulmonar o policitemia) | Consistente | Moderada |
| No se recomienda en pacientes con EPOC e hipoxemia moderada | Consistente | Baja |
| El flujo de oxígeno debe ser el suficiente para mantener una PaO2>60mmHg (8,0kPa) o una SpO2>90% | Consistente | Alta |
| Oxigenoterapia durante el ejercicio | ||
| Puede mejorar la calidad de vida en pacientes que experimentan desaturación durante el ejercicio (SpO2≤88%) | Débil | Baja |
| Para su prescripción se requiere la demostración de que la corrección de la hipoxemia durante el ejercicio mediante la administración de oxígeno (SpO2≥90%) se acompaña de una mejoría de la disnea o de la tolerancia al ejercicio | Débil | Baja |
| Puede ser útil durante el ejercicio en pacientes en programas de rehabilitación, para aumentar la duración e intensidad del entrenamiento | Débil | Moderada |
| Oxigenoterapia nocturna | ||
| Puede considerarse en pacientes con demostración de desaturación nocturna de oxihemoglobina (SpO2<90% durante al menos un 30% del tiempo total de registro) y secuelas relacionadas con la hipoxia (poliglobulia o signos de insuficiencia cardíaca derecha) | Débil | Baja |
| Se debe considerar la CPAP o la ventilación mecánica, que puede sustituir o complementar la oxigenoterapia | Consistente | Moderada |
| Oxigenoterapia durante los viajes en avión | ||
| Se requiere una titulación específica del flujo de oxígeno durante el sueño, ejercicio y viajes en avión | Consistente | Baja |
En todos los casos, la indicación de oxigenoterapia se debe establecer a partir de una gasometría duplicada en un periodo de 3semanas, durante una fase de estabilidad clínica (3meses sin agudización) y bajo tratamiento farmacológico adecuado. Debe comprobarse que el suministro de oxígeno al flujo necesario para aumentar eficazmente la PaO2 no desencadena hipercapnia ni acidosis agudas. Por último, se debe reconsiderar la indicación de oxigenoterapia en los pacientes que, pese a cumplir los requisitos necesarios, siguen fumando, tienen una historia clara de mal cumplimiento terapéutico o son incapaces de manipular correctamente los sistemas de suministro de oxígeno.
Oxigenoterapia intermitentePacientes con una PaO2 basal superior a 60mmHg pueden desarrollar hipoxemia grave en determinadas circunstancias, especialmente durante el ejercicio y el sueño, que pueden plantear la administración de oxígeno.
EPOC con hipoxemia en ejercicio. Un porcentaje variable de pacientes con EPOC e hipoxemia leve-moderada experimenta desaturación en ejercicio, que puede ser identificada por alcanzar una SpO2≤88% sostenida durante al menos 2min en una PM6M57,58.
La reversión de la hipoxemia en ejercicio mediante oxigenoterapia mejora el aporte periférico de oxígeno, reduce la demanda ventilatoria, atenúa la hiperinsuflación dinámica y mejora la función cardíaca derecha59. La administración de oxígeno durante el ejercicio a pacientes que desaturan origina un beneficio a corto plazo, con aumento de su tolerancia al ejercicio y reducción de la disnea60–63. Este beneficio se podría mantener a medio plazo, con mejoría de la calidad de vida relacionada con la salud38 e incremento de la capacidad de ejercicio58. Sin embargo, y pese a que la desaturación en ejercicio de pacientes con EPOC que permanecen normoxémicos en reposo supone un factor de mal pronóstico, no se ha demostrado que la oxigenoterapia modifique su supervivencia58.
En ausencia de información más específica, la consideración de oxigenoterapia durante el ejercicio para incrementar la calidad de vida de pacientes con hipoxemia en ejercicio requiere la demostración de la corrección de la hipoxemia mediante la administración de oxígeno (SpO2≥90%) así como de una mejoría de la disnea o de la tolerancia al ejercicio (incremento de la distancia recorrida de al menos 25-30m64,65) (recomendación débil, calidad de la evidencia baja).
En pacientes con limitación al ejercicio por hipoxemia, la administración de oxígeno durante el ejercicio puede permitir aumentar la intensidad de esfuerzo y disminuir la disnea y, por tanto, facilitar la rehabilitación, cuya eficacia está sobradamente demostrada55,56. El efecto del entrenamiento con suplemento de oxígeno frente a aire comprimido en pacientes sin hipoxemia grave ha sido evaluado en diversos estudios de corta duración, comprobando que con oxígeno aumenta la potencia pico y el tiempo de resistencia en un ejercicio de carga constante, mientras que disminuye la frecuencia respiratoria en isotiempo36, así como la disnea62. Un metaanálisis del efecto de la oxigenoterapia durante un programa de entrenamiento confirma que mejora el tiempo de resistencia y disminuye la disnea durante el ejercicio de carga constante y durante la prueba de caminata en lanzadera (shuttle walking test), mientras que no se identifica efecto sobre la prueba de ejercicio cardiorrespiratorio progresivo ni sobre la PM6M37. Sin embargo, no existen estudios que demuestren que los pacientes que realizan rehabilitación sin oxígeno tengan una peor evolución que los pacientes que reciben oxígeno. Por todo ello, se recomienda considerar la administración de oxígeno durante el ejercicio en pacientes con desaturación en ejercicio incluidos en programas de rehabilitación, para aumentar la duración e intensidad del entrenamiento (recomendación débil, calidad de la evidencia moderada) (tabla 4).
EPOC con hipoxemia nocturna. Existen diversos criterios para la identificación de hipoxemia nocturna. Se demuestra su existencia cuando de objetiva un episodio de desaturación de al menos 5min de duración con una SpO2 mínima ≤85%, al menos una vez durante la noche, preferentemente en sueño REM39. Aunque la definición más operativa consiste en un tiempo con SpO2<90%≥30% de la duración total del registro66, se ha comprobado que los pacientes con EPOC e hipoxemia moderada en vigilia presentan una peor supervivencia a los 3años si tienen desaturación nocturna que si no la tienen39.
Todavía se dispone de poca información sobre el efecto de la oxigenoterapia nocturna. Dos pequeños estudios no han detectado efecto sobre la supervivencia ni sobre la indicación de oxigenoterapia continua10,39. Pese a que sus tamaños muestrales no resultan adecuados para evaluar la incidencia de estos episodios, la evidencia disponible actualmente sugiere que la oxigenoterapia nocturna no parece mejorar la supervivencia de pacientes con EPOC que solo tienen desaturación nocturna1. La evaluación de otros posibles efectos de la oxigenoterapia nocturna muestra resultados controvertidos y ausencia de información consistente sobre su repercusión en la calidad del sueño, desarrollo de arritmias o de hipertensión pulmonar58. Mientras que algún estudio describe un mínimo efecto sobre el incremento de la presión pulmonar40, en otro no se detecta impacto sobre la hemodinámica pulmonar10. Es previsible que en los próximos años el ensayo INOX (NCT01044628) proporcione información más sólida para determinar si en pacientes con EPOC e hipoxemia moderada que presentan desaturación nocturna la oxigenoterapia nocturna afecta a su mortalidad o a la necesidad futura de oxigenoterapia continua.
Puede considerarse la oxigenoterapia nocturna en pacientes con demostración de desaturación nocturna de oxihemoglobina (SpO2<90% durante al menos un 30% del tiempo total de registro) y secuelas relacionadas con la hipoxia (poliglobulia o signos de insuficiencia cardíaca derecha) (recomendación débil, calidad de la evidencia baja). En dicha situación se debe considerar la CPAP o la ventilación mecánica, que pueden sustituir o complementar la oxigenoterapia (recomendación consistente, calidad de la evidencia moderada) (tabla 4).
Otras situaciones especiales. Pacientes con EPOC grave e hipoxemia moderada a nivel del mar pueden precisar suplementación de oxígeno durante viajes en avión, especialmente en vuelos transoceánicos. Tanto la evaluación de las necesidades de oxígeno como la titulación del flujo requerido durante los viajes en avión deben realizarse según las recomendaciones específicas67,68.
Otras enfermedades respiratoriasEl concepto del aumento de supervivencia en pacientes con EPOC tratados con oxigenoterapia se ha extendido por analogía a la insuficiencia respiratoria crónica originada por otras enfermedades69. Si bien esta actitud parece razonable, cabe recordar que está basada en la hipótesis de que el efecto beneficioso del oxígeno se debe a la corrección de la hipoxemia independientemente de la causa de la misma, lo que no está demostrado. Se dispone de información preliminar sobre el papel de la oxigenoterapia en algunas enfermedades.
Hipertensión pulmonarNo existen datos consistentes sobre los efectos a largo plazo de la oxigenoterapia en pacientes con hipertensión pulmonar70. Aunque en algunos pacientes con hipertensión arterial pulmonar se ha descrito una mejoría en la hipertensión pulmonar con oxígeno a bajo flujo13,71, esto no ha sido confirmado en estudios controlados. En un estudio controlado en pacientes con síndrome de Eisenmenger, la oxigenoterapia nocturna no demostró efecto sobre las variables hematológicas, la calidad de vida o la supervivencia72, mientras que un estudio previo sugirió un incremento de la supervivencia73.
En estos pacientes se indica oxigenoterapia continua si la PaO2 es menor de 60mmHg, tratando de mantener una SpO2>90% (recomendación consistente, calidad de la evidencia baja)74–76. La oxigenoterapia durante el ejercicio se puede considerar cuando existe evidencia de beneficio sintomático de la corrección de la desaturación en ejercicio (recomendación débil, calidad de la evidencia baja)76.
Enfermedad pulmonar intersticial difusaLa hipoxemia en reposo y la desaturación durante el ejercicio en pacientes con FPI constituyen factores de mal pronóstico77,78, por lo que su reversión podría tener interés clínico. Además, la oxigenoterapia podría atenuar el componente de hipertensión pulmonar originado por la hipoxemia y ayudar a mejorar la tolerancia al ejercicio y la calidad de vida de estos enfermos79. Sin embargo, no se ha demostrado que la administración de oxígeno mejore la supervivencia de pacientes con FPI80,81.
A falta de datos específicos, se recomienda administrar OCD ante la constatación de hipoxemia grave en reposo (PaO2<60mmHg) o desaturación durante el ejercicio (recomendación consistente, calidad de la evidencia muy baja)82.
Fibrosis quísticaEn pacientes con fibrosis quística se ha demostrado que la oxigenoterapia nocturna no tiene efectos sobre la mortalidad, hospitalizaciones ni progresión de la enfermedad, aunque reduce el absentismo escolar y laboral83. A su vez, la administración de oxígeno durante el ejercicio parece mejorar el trabajo ventilatorio y cardiovascular, aumentar la capacidad de ejercicio y disminuir la desaturación de oxihemoglobina27,84. La gran heterogeneidad de los ensayos realizados se evidencia en un metaanálisis que confirma que la oxigenoterapia no muestra efecto sobre la supervivencia pero mejora el absentismo85. Además, se evidencia que la oxigenoterapia durante el ejercicio permite incrementar la duración del mismo85.
Por ello, y en ausencia de información más específica, se recomienda considerar la oxigenoterapia ante la existencia de hipoxemia grave (PaO2<60mmHg), haciendo especial énfasis en la necesidad de titular adecuadamente el flujo de oxígeno requerido en ejercicio (recomendación consistente, calidad de la evidencia baja).
Reevaluación de la indicaciónUna vez realizada la indicación de oxigenoterapia, se recomienda su reevaluación al mes o los 2meses de la prescripción, para verificar el cumplimiento, comprobar que el paciente continúa sin fumar y evaluar su impacto clínico, tanto en percepción de beneficio subjetivo como en efecto sobre la calidad de vida del paciente. También se requiere una valoración gasométrica basal para descartar hipoxemia grave ficticia, que puede originar hasta un 30% de prescripciones innecesarias durante el alta hospitalaria86,87. Además, se recomienda realizar una gasometría con el flujo de oxígeno prescrito para verificar que permite mantener una PaO2>60mmHg.
Aunque no existe una recomendación consensuada sobre la frecuencia de las revisiones periódicas, parece razonable que como mínimo sea anual.
RecomendaciónLa oxigenoterapia continua está indicada en pacientes con EPOC con PaO2 en reposo ≤55mmHg o PaO2 en reposo entre 56-59mmHg con evidencia de daño orgánico por hipoxia. La desaturación durante el ejercicio puede mejorar la calidad de vida en pacientes que experimentan desaturación durante el esfuerzo (SpO2≤88%), requiriéndose para su prescripción la demostración de una mejoría de la disnea o de la tolerancia al esfuerzo con la administración de oxígeno. La oxigenoterapia nocturna puede considerarse en pacientes con demostración de desaturación nocturna de oxihemoglobina (SpO2<90% durante al menos un 30% del tiempo total de registro) y secuelas relacionadas con la hipoxia.
Indicaciones en otras situacionesMostramos a continuación las recomendaciones y la evidencia disponible del uso de oxígeno en otras situaciones clínicas.
Insuficiencia cardíaca congestivaDatos procedentes de estudios controlados y aleatorizados sobre el papel de la OCD en pacientes con insuficiencia cardíaca congestiva no evidencian beneficios sobre la supervivencia o grado funcional de los pacientes (recomendación consistente, calidad de la evidencia muy baja).
Se ha descrito que hasta el 33-82% de pacientes con insuficiencia cardíaca crónica pueden tener apneas centrales con respiración periódica de Cheyne-Stokes88,89. La supresión de la hipoxemia nocturna con oxigenoterapia permite mejorar la respiración de Cheyne-Stokes89–93, reducir la actividad simpática y aumentar la tolerancia al ejercicio89. En estos enfermos, se ha demostrado que la oxigenoterapia nocturna mejora los parámetros de sueño, la función del ventrículo izquierdo y la calidad de vida relacionada con la salud89,94,95.
Por tanto, en pacientes con insuficiencia cardíaca (fracción de eyección del ventrículo izquierdo <45%) y respiración de Cheyne-Stokes se recomienda considerar la oxigenoterapia nocturna, una vez verificada la corrección de los parámetros de sueño, y utilizarla preferiblemente asociada a servoventilación (recomendación consistente, calidad de evidencia alta).
Síndrome hepatopulmonarEl síndrome hepatopulmonar (SHP) se caracteriza por un incremento del gradiente alveoloarterial de oxígeno causado por vasodilatación pulmonar. Inicialmente puede cursar sin hipoxemia y ocurre en el seno de una enfermedad hepática, tanto aguda como crónica, principalmente en la cirrosis hepática. La causa de la hipoxemia en el SHP es la dilatación de los vasos precapilares y poscapilares pulmonares, que permiten que sangre venosa desaturada pase rápidamente a las venas pulmonares, con la consiguiente disminución de la oxigenacio¿n de la sangre arterial. La mayoría de los estudios han objetivado que los pacientes cirróticos con SHP tienen una mayor mortalidad que los pacientes sin SHP con similar grado de disfunción hepática. El pronóstico es peor en los que tienen una PaO2<60 mmHg96.
La intensidad del SHP se establece siempre que exista un gradiente alveoloarterial de O2 elevado (>15mmHg), en función del grado de hipoxemia: leve cuando la PaO2 es >80mmHg; moderado entre 60 y 80mmHg; grave entre menos de 60 y más de 50mmHg, y muy grave cuando es inferior a 50mmHg. El tratamiento de elección es el trasplante hepático96.
La administración de O2 ha mostrado en casos aislados que proporciona alivio sintomático, aunque no hay evidencias para la generalización de su uso. Se ha descrito mejora de la función hepática en 2pacientes tratados con oxigenoterapia, reforzando el concepto de que la hipoxia puede alterar directamente el funcionalismo hepático y su regeneración. Las recomendaciones de las sociedades científicas establecen la indicación de OCD en pacientes con PaO2 entre 50 y 60mmHg, considerando que hay que individualizar la indicación en aquellos con hipoxemia grave (recomendación consistente, calidad de la evidencia muy baja)97.
Cefalea en racimosEsta entidad está catalogada como uno de los dolores más insoportables que puede experimentar un ser humano. El tratamiento farmacológico de elección durante la crisis son los triptanos (sumatriptán). Este medicamento se inyecta por vía subcutánea y empieza a hacer efecto en tan solo 15min; sin embargo, está contraindicado en pacientes con enfermedad isquémica, y su uso debe limitarse a 2inyecciones al día. La alternativa es la inhalación de O2 al 100%98. La gran ventaja del O2 es que se puede combinar con el tratamiento farmacológico, se puede usar varias veces al día, carece de efectos secundarios y puede ser utilizado en pacientes en los que están contraindicados los triptanos99. Estudios controlados han demostrado que la administración de O2 al 100% durante 15min al comienzo del ataque es un tratamiento seguro y efectivo en términos de abortar la crisis, y así se ha recogido en las guías de actuación terapéutica100. Recientemente se han publicado los resultados de un estudio doble ciego, cruzado, controlado con placebo, aportando evidencia científica sólida sobre la superioridad de la administración de O2 frente a aire, en la eliminación del dolor a los 15min y en alcanzar una mejoría significativa del dolor en este periodo de tiempo101. Queda abierta la puerta a la realización de estudios que demuestren cuál es el mejor modo de administrar el O2 y a qué dosis en el domicilio de los pacientes con cefaleas en racimos (recomendación consistente, calidad de la evidencia moderada).
Disnea secundaria a cáncerSe asume que la administración de oxígeno a pacientes oncológicos con disnea podría aliviar parcialmente su sintomatología102, y por tanto se considera como tratamiento paliativo en diversas normativas103,104.
Sin embargo, 2metaanálisis no verificaron la eficacia del oxígeno como tratamiento sintomático de la disnea refractaria en pacientes con cáncer sin hipoxemia grave105,106. Abernethy et al.107 tampoco demostraron superioridad del oxígeno frente al aire comprimido en el control sintomático de pacientes oncológicos con limitación de la expectativa de vida, disnea refractaria y una PaO2>55mmHg. Un reciente metaanálisis que evalúa la eficacia de diversos tratamientos sintomáticos de la disnea secundaria a cáncer confirma el efecto beneficioso de los opiáceos, mientras que no lo detecta para el oxígeno108.
Por tanto, en el tratamiento sintomático de la disnea secundaria a cáncer, el oxígeno es menos eficaz que los opiáceos (recomendación consistente, calidad de evidencia alta), y solo se podría considerar si se identifica un efecto adicional en un ensayo terapéutico de corta duración (recomendación débil, calidad de la evidencia baja).
Oxigenoterapia en niñosEl tratamiento con oxígeno presenta algunas diferencias en niños con respecto a los adultos109. La mayoría de las situaciones clínicas que requieren oxigenoterapia en el niño son exclusivas de la edad pediátrica, aunque a veces existe un solapamiento entre los niños mayores y los adultos jóvenes. El pronóstico suele ser bueno y muchos niños solo necesitan oxígeno durante un periodo limitado, que está condicionado por el crecimiento y el desarrollo neurológico. Además, muchos niños solo requieren aporte de oxígeno durante la noche, generalmente menos de 15h110,111.
Las indicaciones específicas de oxigenoterapia en niños se limitan a 3situaciones: hipoxemia grave (3desviaciones estándar por debajo de lo esperable con el niño en situación estable respirando aire ambiente); desaturación nocturna (tiempo con SpO2<90% mayor del 20% del registro), o presencia de hipertensión pulmonar, hipertrofia ventricular derecha o policitemia secundaria a hipoxemia crónica (recomendación consistente, calidad de la evidencia moderada)110,111.
En la enfermedad pulmonar crónica neonatal la oxigenoterapia reduce o previene la hipertensión pulmonar, reduce las desaturaciones intermitentes, disminuye las resistencias de las vías aéreas y promueve el crecimiento (recomendación consistente, calidad de la evidencia baja). También es beneficiosa para el desarrollo neurológico (recomendación consistente, calidad de la evidencia muy baja), puede disminuir el riesgo asociado de muerte súbita (recomendación consistente, calidad de la evidencia muy baja) y disminuye la hospitalización (recomendación consistente, calidad de la evidencia baja)110,111. En niños con fibrosis quística la oxigenoterapia mejora la asistencia escolar (recomendación consistente, calidad de la evidencia moderada), y produce una mejoría sintomática (recomendación consistente, calidad de la evidencia muy baja)111.
RecomendaciónLa oxigenoterapia nocturna debe recomendarse a pacientes con insuficiencia cardíaca congestiva con respiración de Cheyne-Stokes objetivada, preferiblemente asociada a servoventilación. La indicación de OCD en pacientes con SHP hay que considerarla en los que presenten insuficiencia respiratoria. La administración de oxígeno al 100% es un tratamiento de eficacia contrastada en los pacientes con cefaleas en racimos. La utilización paliativa de oxigenoterapia en pacientes con cáncer y disnea ha demostrado ser menos eficaz que la administración de opiáceos.
Fuentes de oxígenoSistemas estáticos (fig. 2)BombonasLos cilindros de aluminio han sustituido a los cilindros de acero para su uso en el hogar almacenando el gas comprimido (200bars), y existen bombonas de diferentes tamaños que son útiles en pacientes con poca movilidad. Actualmente la OCD se administra preferentemente utilizando 2tipos de sistemas estáticos: concentradores de oxígeno o depósitos de oxígeno líquido.
Concentradores de oxígenoSon dispositivos conectados a la red eléctrica. El peso es de 13-26kg y emplean la tecnología de separación del nitrógeno del aire ambiente, siendo capaces de entregar 3-4l/min de oxígeno con una pureza del 95%, aunque existen modelos de concentradores que proporcionan hasta 10l/min. Son útiles en pacientes que precisen bajos flujos y realicen salidas esporádicas. Presentan un coste inferior al de las bombonas ya que precisan un menor número de desplazamientos de la empresa suministradora. Para facilitar el movimiento en el entorno familiar los pacientes pueden conectar su sistema estacionario con un tubo de hasta 15m, siendo esto aplicable a cualquier fuente estática112.
Oxígeno líquidoEl oxígeno en estado líquido puede ser almacenado, transportado y traspasado a otros dispositivos de manera más eficiente que los sistemas de gas. Con una relación de expansión de 860:1,1l, el oxígeno líquido se expandirá a 860l de oxígeno gaseoso, pudiendo proporcionar hasta 15l/min de oxígeno de flujo continuo con una pureza de 99%. El componente principal es un unidad base (denominada «nodriza»), que es un contenedor especialmente diseñado que almacena oxígeno en estado líquido a –180°C y que se acompaña de una mochila para los desplazamientos. Se recomienda en pacientes que precisen oxígeno fuera del domicilio y flujos altos en reposo (>3l/min). Sin embargo, como el contenido de oxígeno se agota, la nodriza requiere recarga periódica por el proveedor de cuidados domiciliarios. (tabla 5).
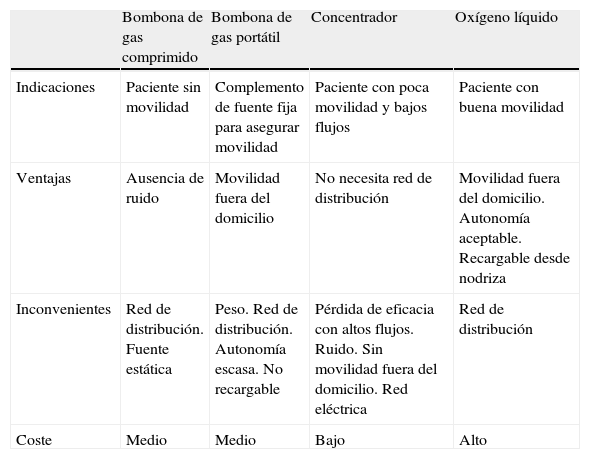
Características principales de las fuentes de oxígeno
| Bombona de gas comprimido | Bombona de gas portátil | Concentrador | Oxígeno líquido | |
| Indicaciones | Paciente sin movilidad | Complemento de fuente fija para asegurar movilidad | Paciente con poca movilidad y bajos flujos | Paciente con buena movilidad |
| Ventajas | Ausencia de ruido | Movilidad fuera del domicilio | No necesita red de distribución | Movilidad fuera del domicilio. Autonomía aceptable. Recargable desde nodriza |
| Inconvenientes | Red de distribución. Fuente estática | Peso. Red de distribución. Autonomía escasa. No recargable | Pérdida de eficacia con altos flujos. Ruido. Sin movilidad fuera del domicilio. Red eléctrica | Red de distribución |
| Coste | Medio | Medio | Bajo | Alto |
Cuando los pacientes deben dejar su domicilio por unas horas, la OCD no debería ser interrumpida. Así, como parte de su prescripción, los pacientes disponen de sistemas portátiles de suministro de oxígeno113,114.
Un método clásico es el uso de cilindros de oxígeno gaseoso de tamaño pequeño tipo mochila (tamaño M-6) que, si fuera necesario, pueden transportarse en un carro. Sin embargo, existe la limitación debido a su pequeña capacidad; así, un paciente con una prescripción de OCD de 2l/min agota un cilindro M-6 (164l de oxígeno gaseoso) en poco más de una hora. Cilindros de mayor tamaño hacen que sean poco manejables y extremadamente difíciles de transportar.
La segunda opción es acoplar a la ya mencionada nodriza de oxígeno líquido una mochila portátil que se rellena desde la nodriza; se utiliza en pacientes activos con objetivada caída de la saturación de la oxihemoglobina (SpO2) en el esfuerzo y que quieran utilizarlo fuera de su domicilio115–117. El tiempo de uso dependerá del flujo empleado. Es útil en pacientes para desplazamientos cortos y necesidad de flujos altos en esfuerzo de más de 3l/min.
Concentrador con transfer a cilindro. Es una adaptación del concentrador tradicional. Se trata de un módulo que transfiere O2 a un cilindro portátil, y requiere varias horas para su carga y recarga diaria. Es útil en pacientes con salidas esporádicas, aunque es poco habitual en nuestro medio.
Concentrador portátil de oxígeno. Supone la ventaja de poder adaptarse a cualquier toma de red eléctrica o a la batería de un automóvil. Han dado lugar a la tecnología denominada «non delivery·delivery less», ya que no necesitan de proveedor para ser mantenidos aunque requieren revisiones cada 3meses. Los concentradores portátiles deben pesar no más de 4kg, aunque algunos de flujo continuo pesan 9kg y producen un 90%±3% de oxígeno, proporcionando por lo menos 2l de oxígeno durante un mínimo de 4h. Es útil en pacientes que realicen desplazamientos largos y tengan actividades frecuentes fuera del domicilio117.
Con tecnología de conservación de oxígeno (fig. 3)Válvula a demanda. Los denominados «sistemas dosis de pulso», «flujo a demanda», «sistemas de suministro de oxígeno a demanda» y/o «dispositivos de conservación de oxígeno» suministran oxígeno de manera intermitente, a diferencia de la terapia de flujo continuo. En lugar de flujo continuo, la tecnología de conservación de oxígeno (TCO) a demanda ofrece un volumen preajustado, o bolo de oxígeno, que se mide en mililitros por respiración. El bolo se entrega cuando el paciente realiza un esfuerzo inspiratorio (o demanda). El bolo se aplica durante el primer 60% de la inspiración y, por tanto, no se está desperdiciando durante el resto de cada ciclo de respiración con mayor duración de la fuente de suministro. Es importante señalar que no son equivalentes la configuración numérica de un medidor de flujo continuo que se expresa en litros/min, mientras que la configuración numérica, diferente según el modelo, de un TCO indica los tamaños relativos de los bolos entregados. Se pueden utilizar 2sistemas: oxígeno líquido y concentrador. Los primeros suministran entre 1,5 y 5pulsos (pulsos de ±15ml), recargándose de la nodriza correspondiente; asimismo, existen algunos modelos capaces de funcionar tanto a flujo continuo como a pulsos. Con los concentradores portátiles de oxígeno los pulsos varían según modelos (1 a 6pulsos), con pulsos diferentes y con la ventaja de ser fácilmente recargables y de ser utilizados en el domicilio y en desplazamientos. Existe algún modelo que puede ser utilizado tanto en flujos continuo como a demanda. Son útiles en pacientes capaces de disparar la válvula y que se constata que mantienen saturaciones correctas durante los desplazamientos118.
Los dispositivos a demanda son sensibles a variables como la frecuencia respiratoria del paciente, que puede condicionar las cifras de SpO2 obtenidas, por lo que deben existir alarmas que deben saltar cuando la SpO2 baja del 85%. La prescripción de todos los sistemas portátiles necesita evaluar al paciente durante el ejercicio para un correcto ajuste de la dosis necesaria119.
Sistemas de liberación al pacienteCatéter transtraquealEl catéter transtraqueal proporciona oxígeno directamente en la tráquea a través de un pequeño catéter de 1,6-2mm de diámetro que se introduce por vía percutánea a la altura del segundo-tercer anillo traqueal; produce un ahorro de oxígeno del 50% en reposo y del 30% en ejercicio. Estaría indicado en pacientes que utilizan fuentes portátiles para la deambulación. Sus inconvenientes radican en que se trata de un método invasivo, necesita un entrenamiento y una educación en su cuidado, y es preciso recambiarlo cada 60-90días en ámbito hospitalario50. Su utilización actual es escasa120.
Mascarilla tipo VenturiLa fracción inspirada de O2 (FiO2) se regula mediante la apertura de las ventanas laterales de la máscara «efecto Venturi»; suministra una FiO2 fija, constante e independiente del patrón respiratorio del paciente. En domicilio solo se utiliza en pacientes con hipercapnia para aplicarlo durante la noche.
Cánulas nasalesEs el sistema utilizado habitualmente en domicilio. Consiste en 2tubos pequeños, flexibles, de 0,5 a 1cm, que se acoplan a las fosas nasales y se ajustan detrás de los pabellones auditivos. La FiO2 es totalmente variable dependiendo del volumen corriente del paciente. Dado que se admite que las cánulas nasales convencionales son un sistema ineficiente —solo el 15-20% del oxígeno administrado participa en el intercambio gaseoso—, se han concebido sistemas de ahorro para utilizar menos oxígeno y de manera más eficiente, con un aumento de la autonomía hasta 3veces más que con oxígeno continuo utilizando las gafas nasales convencionales.
ReservoriosUtilizan fuentes continuas, proporcionan un bolo enriquecido de oxígeno al comienzo de la inspiración y acumulan en la espiración una cantidad de ±20ml. Son útiles en pacientes que precisen flujos altos que no puedan ser suministrados por las fuentes habituales o que necesiten conseguir una misma SpO2 con menos flujos121 (tabla 6).
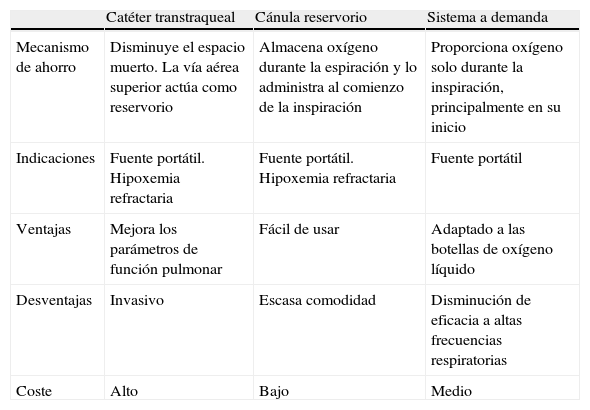
Características principales de los sistemas de ahorro o liberación de oxígeno
| Catéter transtraqueal | Cánula reservorio | Sistema a demanda | |
| Mecanismo de ahorro | Disminuye el espacio muerto. La vía aérea superior actúa como reservorio | Almacena oxígeno durante la espiración y lo administra al comienzo de la inspiración | Proporciona oxígeno solo durante la inspiración, principalmente en su inicio |
| Indicaciones | Fuente portátil. Hipoxemia refractaria | Fuente portátil. Hipoxemia refractaria | Fuente portátil |
| Ventajas | Mejora los parámetros de función pulmonar | Fácil de usar | Adaptado a las botellas de oxígeno líquido |
| Desventajas | Invasivo | Escasa comodidad | Disminución de eficacia a altas frecuencias respiratorias |
| Coste | Alto | Bajo | Medio |
Se recomienda lavar con agua y jabón cada mañana la parte en contacto con el paciente de los sistemas de liberación, ya sean gafas nasales, cánulas reservorio o mascarillas. Los tubos y alargaderas se deben lavar una vez a la semana, y se recomienda el cambio de las gafas nasales y de las mascarillas cada 15días. Para las cánulas reservorio el recambio recomendado por el fabricante es cada 3semanas.
Con respecto a las fuentes, el oxígeno no es combustible, pero activa la combustión de las materias inflamables. Por ello hay que tener en cuenta las recomendaciones generales que facilitan las empresas suministradoras117.
Recomendaciones específicas según la fuente de oxígenoBombonaEvitar que caiga. No engrasar ni lubricar las válvulas que sirven para el suministro. Abrir el caudalímetro suavemente.
ConcentradorEl concentrador se ha de colocar a 15cm de la pared o de un mueble para facilitar la circulación de aire: no taparlo nunca. Hay que esperar entre 5 y 10min desde la puesta en marcha hasta su utilización, tiempo que tarda en proporcionar la concentración de oxígeno adecuada. Desconectar el concentrador cuando no se utiliza. Se puede poner en otra habitación o sobre una alfombra para amortiguar el ruido. Hay que moverlo en posición vertical, incluso para transportarlo. El concentrador portátil debe estar siempre conectado (en domicilio) a la corriente eléctrica para mantener cargada la batería. Se recomienda llevar el conector a la corriente en las salidas del domicilio, por si es necesario. Hay que lavar el filtro de entrada de aire cada semana.
Oxígeno líquidoEs extremadamente frío, por lo que no deben tocarse las partes heladas. Para cargar la mochila se recomienda hacerlo en una habitación bien ventilada y que el suelo sea firme. No alejarse del depósito mientras se recarga. Si hay fugas al separar la mochila del tanque, se debe volver a conectar la mochila, y si esto es imposible, hay que ventilar el local, no tocar las fugas, no fumar ni provocar llamas o chispas. En caso de fuga, se recomienda alejarse de las proyecciones, y si entrara en contacto con los ojos, se deben lavar con abundante agua durante más de 15min. Si entrara en contacto con la piel, se recomienda no frotar, quitar la ropa si fuera necesario, descongelar las partes afectadas con calor moderado y, en ambos casos, avisar al médico122.
Prescripción de la oxigenoterapia continua domiciliariaAjuste del flujo de oxígenoA pesar de que se debería ajustar el flujo de oxígeno para conseguir una adecuada corrección de la SpO2, lo cierto es que existe una gran disparidad en la forma de hacerlo. Wijkstra et al.123, mediante encuestas, observaron que menos del 40% de neumólogos ajustaban adecuadamente el flujo en las distintas situaciones: reposo, sueño y esfuerzo.
En reposoEl flujo de oxígeno debería ajustarse cuando el paciente no fuma, estando en fase estable, despierto, en reposo y tras un tratamiento farmacológico optimizado. Además, se debe comprobar la adecuada corrección de los gases arteriales, utilizando la misma fuente que llevará en su domicilio124. Para ello se recomienda ajustar el flujo con un pulsioxímetro hasta alcanzar una SpO2≥90%, y en este punto extraer gases arteriales para asegurar una adecuada corrección de la hipoxemia sin producir hipercapnia (recomendación consistente, calidad de evidencia alta). En los pacientes con insuficiencia respiratoria normocápnica podría hacerse el ajuste solo con el pulsioxímetro.
Durante el sueñoSe considera desaturación nocturna la presencia de una SpO2 media <90% y/o un porcentaje de tiempo con SpO2<90%(CT90)>30%125.
Hay varios métodos para ajustar el flujo de oxígeno durante el sueño:
a) Mantener el mismo flujo de reposo. Diversos estudios126–128 muestran que con el flujo de oxígeno ajustado durante el día existe una inadecuada corrección de la SpO2 durante el sueño en un importante número de pacientes, entre el 16 y el 48%. Descartar la presencia de un síndrome de apneas-hipopneas del sueño (SAHS) y realizar el ajuste en fase estable de la enfermedad pueden determinar que se consiga una mejor corrección de la SpO2126.
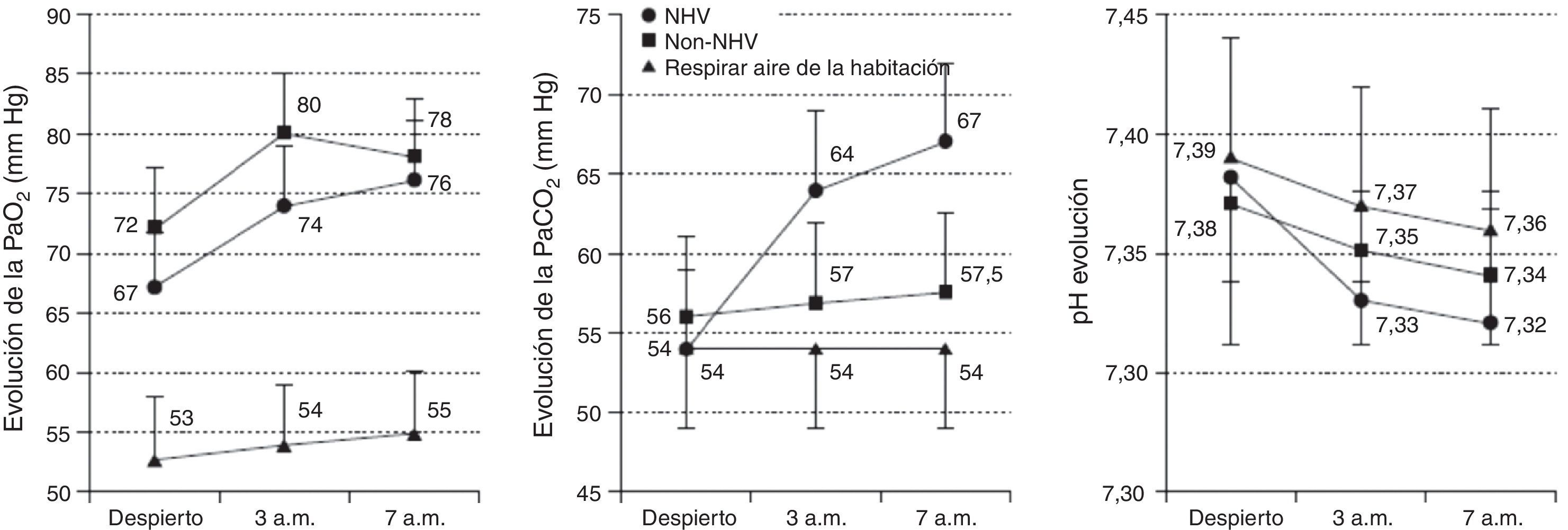
b) Incrementar el flujo de oxígeno en reposo en 1 o 2l·min−1 para evitar la caída de la SpO2 nocturna (recomendación consistente, calidad de la evidencia moderada). Así lo recomiendan algunas guías internacionales129, afirmando que no existe riesgo de provocar hipercapnia secundaria. Sin embargo, es bien conocido que la administración de oxígeno puede potencialmente generar hipercapnia. Este fenómeno está mediado por distintos mecanismos tales como la hipoventilación, las alteraciones de ventilación-perfusión o el efecto Haldane. Además, el sueño por sí mismo produce una serie de fenómenos como una disminución en el metabolismo basal, un incremento en la resistencia de las vías aéreas, una hipotonía de la bomba muscular respiratoria y una disminución en la sensibilidad del centro respiratorio. En pacientes con EPOC se añade, además, una mayor hipoventilación debida a una reducción en el volumen corriente, la asociación frecuente de un SAHS y/o la reducción del aclaramiento mucociliar. Por lo tanto, la oxigenoterapia nocturna induce hipercapnia en pacientes con EPOC con mayor frecuencia de lo esperado. De hecho, hay 2estudios127,130 que detectan entre el 43 y el 59% de pacientes con hipercapnia nocturna con el flujo de oxígeno ajustado durante el día. Los factores predictores de esta mala respuesta al oxígeno son un índice más elevado de masa corporal y una PaO2 más baja durante la administración diurna de oxígeno131 (fig. 4).
Evolución de la PaO2, la PaCO2 y el pH en pacientes con EPOC y OCD.
Breathing room air: respirando aire ambiente; EPOC: enfermedad pulmonar obstructiva crónica; NHV: hipoventilación nocturna; OCD: oxigenoterapia continua domiciliaria; PaCO2: Presión arterial de dióxido de carbono; PaO2: Presión arterial de oxígeno.
De Tarrega et al.131.
Parece obvio que si incrementamos el flujo de oxígeno en 1 o 2l·min−1 el fenómeno de hipoventilación puede empeorar, tal como se ha demostrado en un estudio donde se objetivaba un incremento significativo de la PaCO2 y la presencia de acidosis respiratoria en un considerable número de pacientes tras incrementar 1l el flujo en comparación con el ajustado de día (34,2% vs 23,7%)132.
c) Ajustar el flujo de oxígeno según una monitorización continua de la SpO2durante el sueño para mantener una SpO2≥90%. Las situaciones detalladas previamente refuerzan la necesidad de evaluar individualmente a los pacientes con EPOC e insuficiencia respiratoria crónica hipercápnica para ajustar el flujo de oxígeno durante el sueño. Lo adecuado sería establecer el flujo durante el sueño con un pulsioxímetro para intentar mantener una SpO2≥90%, y en el caso de que el paciente tenga hipercapnia sería importante realizar gases matinales para confirmar que el flujo prescrito no eleva la PaCO2 (recomendación débil, calidad de la evidencia baja).
Durante el ejercicioEn general, se considera desaturación al esfuerzo la presencia de una SpO2 media ≤88% durante una prueba de esfuerzo, como la PM6M, y se recomienda ajustar el flujo de oxígeno durante la misma prueba hasta alcanzar una SpO2 media ≥90%124 (recomendación consistente, calidad de evidencia alta). Sin embargo, con mucha frecuencia no se hace adecuadamente123; de hecho, algunos países europeos sugieren utilizar el mismo flujo de oxígeno que el indicado en reposo o añadir un litro a este sin realizar ninguna prueba que evalúe cuál es el flujo necesario para cada paciente.
La prueba de esfuerzo más utilizada para detectar la caída del SpO2, así como para ajustar el flujo de oxígeno al esfuerzo, es la PM6M, aunque se han utilizado otras, como la de esfuerzo submáximo con cicloergómetro o cinta sin fin133. Se ha demostrado una buena correlación entre la SpO2 durante la PM6M y la obtenida durante las actividades de la vida diaria, así como del flujo de oxígeno necesario para la corrección de dicha desaturación entre ambas situaciones134.
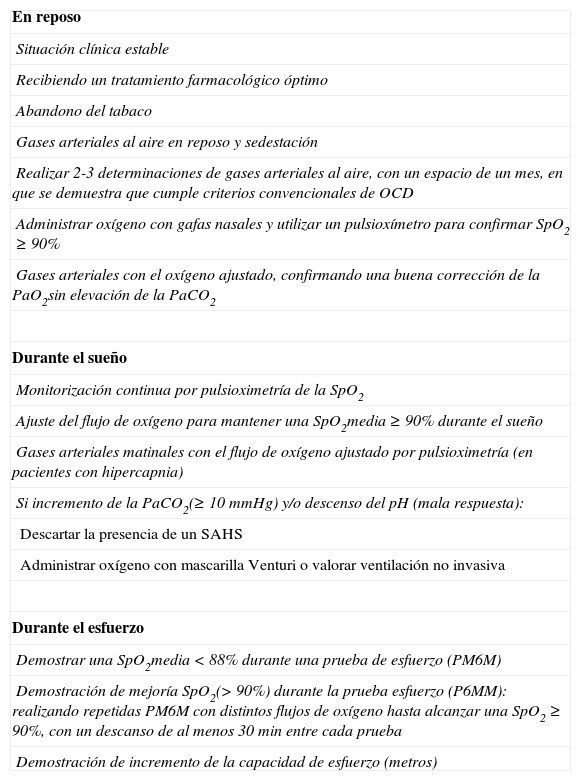
En la tabla 7 se exponen algunas recomendaciones para hacer un correcto ajuste del flujo de oxígeno en reposo, durante el sueño y durante el esfuerzo.
Recomendaciones de ajuste del flujo de oxígeno en reposo, durante el sueño y durante el esfuerzo
| En reposo |
| Situación clínica estable |
| Recibiendo un tratamiento farmacológico óptimo |
| Abandono del tabaco |
| Gases arteriales al aire en reposo y sedestación |
| Realizar 2-3 determinaciones de gases arteriales al aire, con un espacio de un mes, en que se demuestra que cumple criterios convencionales de OCD |
| Administrar oxígeno con gafas nasales y utilizar un pulsioxímetro para confirmar SpO2≥90% |
| Gases arteriales con el oxígeno ajustado, confirmando una buena corrección de la PaO2sin elevación de la PaCO2 |
| Durante el sueño |
| Monitorización continua por pulsioximetría de la SpO2 |
| Ajuste del flujo de oxígeno para mantener una SpO2media≥90% durante el sueño |
| Gases arteriales matinales con el flujo de oxígeno ajustado por pulsioximetría (en pacientes con hipercapnia) |
| Si incremento de la PaCO2(≥10mmHg) y/o descenso del pH (mala respuesta): |
| Descartar la presencia de un SAHS |
| Administrar oxígeno con mascarilla Venturi o valorar ventilación no invasiva |
| Durante el esfuerzo |
| Demostrar una SpO2media<88% durante una prueba de esfuerzo (PM6M) |
| Demostración de mejoría SpO2(>90%) durante la prueba esfuerzo (P6MM): realizando repetidas PM6M con distintos flujos de oxígeno hasta alcanzar una SpO2≥90%, con un descanso de al menos 30min entre cada prueba |
| Demostración de incremento de la capacidad de esfuerzo (metros) |
OCD: oxigenoterapia continua domiciliaria; PaCO2: presión arterial de dióxido de carbónico; PaO2: presión arterial de oxígeno; PM6M: prueba de 6min de marcha; SAHS: síndrome de apnea-hipopnea del sueño; SpO2: saturación de oxihemoglobina.
De O’Donohue124.
En general, se recomienda el uso de oxígeno más de 15h al día, incluyendo la noche (recomendación consistente, calidad de evidencia alta). Sin embargo, si nos fijamos cuidadosamente en los resultados del NOTT7 y del MRC6, observaremos que los pacientes que realizaban el tratamiento 24h tenían mayor supervivencia, si bien es cierto que la media de uso fue de aproximadamente 18h/día. Es razonable pensar que cuantas más horas se realice el tratamiento, mayores beneficios se podrán alcanzar, sobre todo si se usa durante el ejercicio, que es cuando mayor caída de la SpO2 se produce. Un dato interesante que se extrae del estudio de Eaton et al.52 es la demostración de que el único factor predictor de respuesta a la OCD en términos de calidad de vida relacionada con la salud es el número de horas de tratamiento. Este hallazgo apoya el hecho de que las horas de tratamiento tienen impacto en los beneficios.
Actualmente, con los dispositivos portátiles, el uso de oxígeno durante todo el día no provoca limitación para desarrollar las actividades de la vida diaria. Un inconveniente importante es la dificultad de aceptación por parte de los pacientes de utilizar el oxígeno fuera del domicilio.
Elección de la fuente de oxígenoLa elección de la fuente de oxígeno estará en relación con el perfil del paciente, su capacidad y deseo de movilidad y, sobre todo, la adecuada corrección de la SpO2 tanto en reposo como durante el sueño o el esfuerzo.
Según el perfil de movilidad del paciente podemos aconsejar112:
- 1.
Pacientes sin o escasa movilidad. Fuentes de oxígeno fijas, predominantemente el concentrador estático, teniendo en cuenta que facilitan la movilidad dentro del domicilio con una alargadera que puede ser de hasta 15m. Es aconsejable facilitar una botella de oxígeno portátil para los desplazamientos ocasionales fuera del domicilio. También se puede prescribir un concentrador con recargador de botella portátil de oxígeno.
- 2.
Pacientes con movilidad, pero salidas cortas. Oxígeno portátil, ya sea concentrador portátil o líquido, teniendo en cuenta que la duración del concentrador portátil no es de más de 1-3h, dependiendo del modelo y la de la mochila de oxígeno líquido, y de 2-6h, dependiendo de si dispone de un sistema de válvula ahorradora y, sobre todo, del flujo necesario durante el esfuerzo.
- 3.
Pacientes con mayor movilidad, estancia en centros de día, actividad laboral, más de una vivienda y viajes. Concentrador portátil, puesto que permite conectarlo a la electricidad o al encendedor del vehículo. En el caso del viaje en avión, es el único sistema aceptado. En viajes largos en barco se puede plantear tanto el concentrador portátil como el oxígeno líquido. En ambos casos es importante informarse con la agencia de viajes de las posibilidades y de la aceptación de la fuente. Añadir una batería externa permite más autonomía, pero incrementa el peso del sistema.
Debemos añadir 2 premisas indispensables:
- 1.
El uso de concentrador portátil debe estar restringido a los pacientes que precisan flujos bajos de oxígeno (<3l/min o 6pulsos/min, puesto que es el máximo que pueden ofrecer, siempre dependiendo del modelo), y siempre debe comprobarse su eficacia con una prueba de esfuerzo (consiguiendo una SpO2≥90%).
- 2.
En el caso de que el sistema acople válvula a demanda, tanto para oxígeno líquido como concentrador portátil, debe comprobarse siempre su eficacia con una prueba de esfuerzo y no se debe prescribir en pacientes que son portadores de CPAP u otro tipo de ventilación mecánica.
El gasto derivado de la oxigenoterapia es complejo de deducir. Es algo más complicado que valorar el coste estipulado en los conciertos vigentes con las diferentes administraciones sanitarias, sea en modalidad de coste por tratamiento y día, coste per cápita o estimaciones de coste alternativas. A este gasto base habrá que sumarle el coste de tecnologías adicionales e innovación tecnológica, y a su vez habrá que restar los beneficios derivados de esta modalidad de tratamiento. En esta ecuación es fundamental considerar que las indicaciones sean correctas, el cumplimiento de la prescripción óptimo y la adherencia terapéutica completa. Solo así tendremos la certeza de que el gasto invertido en la oxigenoterapia domiciliaria será útil.
Gracias al informe realizado por Fenin y Price Waterhousecooper en 2011, disponemos de algunos datos sobre la eficiencia y los beneficios de la oxigenoterapia domiciliaria en España135. En este informe, el análisis coste-utilidad del tratamiento de la EPOC mediante oxigenoterapia muestra que el tratamiento anual de un paciente con EPOC en estadioiv (por obstrucción espirométrica) supone un ahorro medio de 1.372euros(€), además de mejorar la calidad de vida del paciente en 0,15años ajustados por calidad de vida por paciente y año. Otro dato a resaltar en este informe es que el coste que genera un paciente con EPOC en estadioiii representa aproximadamente el 70% del coste de un paciente con EPOC en estadioiv. Con estos datos, se estima que el coste ponderado de un paciente medio tratado en estadioiii-iv sería de 3.178€, mientras que un paciente medio no tratado supondría un coste de 4.079€. De forma global, se estima que en España en el año 2010 se trataron con oxigenoterapia 79.000pacientes con EPOC, representando un coste de 100millones de euros, y que hubo 42.000pacientes no tratados con esta terapia pero que sí debieron haberla recibido, provocando un coste asociado de 172millones de euros.
No disponemos de datos de coste-eficiencia de los equipos de oxigenoterapia específicos, como los concentradores portátiles o el oxígeno líquido.
RecomendaciónEl flujo de oxígeno debería ajustarse utilizando la misma fuente que llevará el paciente en su domicilio. Se recomienda ajustar el flujo con un pulsioxímetro hasta alcanzar una SpO2≥90%, y en este punto extraer gases arteriales para asegurar una adecuada corrección de la hipoxemia sin producir hipercapnia. En los pacientes con insuficiencia respiratoria normocápnica podría hacerse el ajuste solo con el pulsioxímetro. Durante el sueño se debería ajustar el flujo de oxígeno según una monitorización continua de la SpO2 durante el sueño para mantener una SpO2≥90%. Durante el ejercicio se recomienda ajustar el flujo de oxígeno durante la PM6M hasta alcanzar una SpO2 media ≥90%. La elección de la fuente de oxígeno se debe adaptar al perfil del paciente.
Efectos secundarios y riesgos de la oxigenoterapia continua domiciliariaComo cualquier fármaco, la oxigenoterapia tiene sus efectos secundarios y riesgos136,137, aunque en general es un tratamiento seguro si se siguen las indicaciones elementales. Los principales efectos nocivos suelen derivar del mal uso de los equipos.
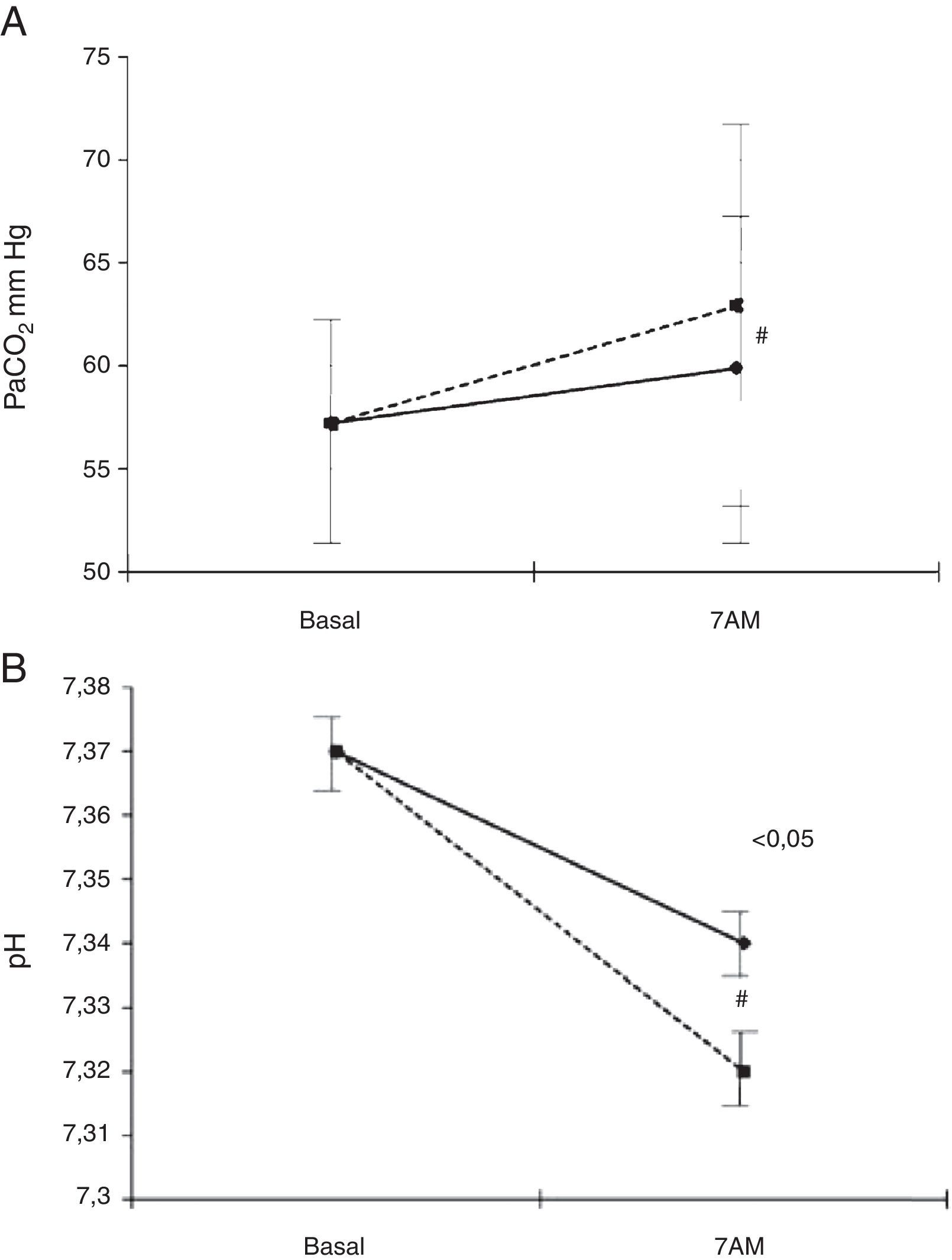
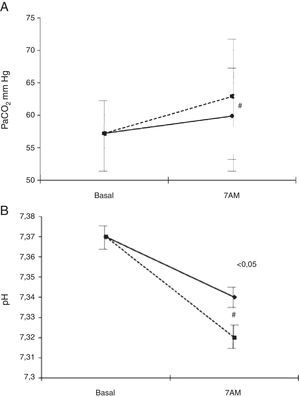
El efecto secundario que más afecta al manejo clínico de los pacientes que precisan OCD es el desarrollo de hipercapnia. El empeoramiento de las relaciones V/Q secundario a la inhibición de la vasoconstricción hipóxica y a la inhibición del estímulo hipóxico son los mecanismos principales que la condicionan. Este fenómeno es especialmente importante durante el sueño127,129 y puede empeorar con el incremento del flujo de oxígeno necesario para corregir la hipoxemia nocturna que aconsejan las diferentes guías, como se ha demostrado recientemente en pacientes con EPOC en fase estable e insuficiencia respiratoria crónica hipercápnica132 (fig. 5).
Evolución de la PaCO2 (A) y el pH (B) durante el sueño con el flujo ajustado en vigilia (línea continua) y tras incrementarlo en 1l/min durante el sueño (línea de puntos).
De Samolski et al.132.
La repercusión clínica de la presencia de hipercapnia nocturna secundaria a la oxigenoterapia no se conoce. Sin embargo, la presencia de hipercapnia diurna se ha considerado como factor de mal pronóstico en la evolución de pacientes con EPOC que precisan OCD138–140. La hipercapnia puede acentuar la disfunción muscular, disminuir la contractilidad del diafragma y favorecer el desarrollo de fatiga muscular141,142. Puede, además, influir en la contractilidad cardíaca, favoreciendo la presencia de arritmias, y producir lesiones estructurales a nivel del miocardio143–145. Otros efectos conocidos de la hipercapnia es la disminución de las resistencias vasculares cerebrales con aumento de la presión intracraneal, potenciando la hipoxia tisular cerebral.
En el caso de coexistencia del SAHS y EPOC, la oxigenoterapia puede prolongar la duración de los episodios obstructivos, incluso cuando se administra a flujos bajos146,147. Como consecuencia de estos fenómenos, la calidad de sueño de estos pacientes podría verse afectada148.
Otro efecto secundario de la oxigenoterapia es la toxicidad pulmonar. El oxígeno puede producir daño pulmonar directo al provocar atelectasias por absorción, al reducirse la concentración intraalveolar de nitrógeno, y daño pulmonar difuso (agudo y crónico) por la liberación de radicales libres. Dichas complicaciones son propias de la administración prolongada de oxígeno a altas concentraciones. Este tipo de alteraciones son dependientes de las dosis y se relacionan tanto con la presión parcial de oxígeno como con el tiempo de exposición. Solo en los casos de daño pulmonar crónico (con proliferación capilar, fibrosis intersticial, hiperplasia epitelial y hemorragia) las lesiones observadas son irreversibles. A pesar de que en la OCD se utilizan flujos bajos de O2 y exposiciones a FiO2<0,5 que se pueden tolerar durante semanas, se han descrito casos de pacientes con OCD que han presentado cambios histológicos relacionados con toxicidad por oxígeno149.
Finalmente, otros efectos adversos que pueden influir en el cumplimiento del tratamiento son la congestión y la irritación de mucosa nasal y epistaxis, el eccema de contacto por el material con el que se realizan las cánulas nasales y los efectos psicológicos y sociales.
También existe el riesgo de los incendios y las explosiones, que son mucho más frecuentes cuando el enfermo continúa fumando. El oxígeno líquido puede producir quemaduras con la manipulación de la fuente de administración o si existen fugas en el sistema.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.