En los últimos años existe un debate en relación con la exactitud diagnóstica de la tomografía axial computarizada (TAC) para identificar metástasis pulmonares y la necesidad de la palpación pulmonar para determinar el número de nódulos metastásicos. El objetivo del estudio fue determinar en qué pacientes era más eficaz la TAC para detectar todas las metástasis.
MétodosSe estudiaron todos los pacientes operados de metástasis pulmonar con intención curativa a través de toracotomía entre 1998 y 2012. Todos los casos fueron revisados preoperatoriamente por 2radiólogos expertos en pulmón. Para el análisis estadístico se utilizó el programa Systat versión 13.
ResultadosCiento ochenta y tres pacientes (63,6% varones) con una edad media de 61,7años a los que se les realizaron 217intervenciones. La TAC acertó en 185casos (85,3%). Discordancias observadas: 26pacientes (11,9%) con más metástasis resecadas que las observadas y 6casos (2,8%) con menos metástasis. Agrupando a los pacientes de origen colorrectal con una o 2metástasis y metástasis única de cualquier origen, la probabilidad de resecar nódulos extras fue del 9,5%. En el resto la probabilidad fue del 27,8%, observándose diferencias estadísticamente significativas (p=0,001). La edad media de los pacientes en los que no aparecieron nódulos no observados fue de 62,9años, frente a 56,5años de media en los pacientes que se escapaba alguna metástasis (p=0,001).
ConclusionesSe consideró grupo con baja probabilidad de resecar más metástasis que las observadas a los pacientes mayores de 60años con una o 2metástasis de origen colorrectal o una de otro origen.
In recent years, there has been debate regarding the diagnostic accuracy of computed tomography (CT) in the identification of lung metastases and the need for lung palpation to determine the number of metastatic nodules. The aim of this study was to determine in which patients the CT scan was more effective in detecting all metastases.
MethodsWe studied all patients who underwent curative thoracotomy for pulmonary metastasis between 1998 and 2012. All cases were reviewed by two expert pulmonary radiologists before surgery. Statistical analyses were performed using Systat version 13.
ResultsThe study included 183patients (63.6% male) with a mean age of 61.7 years who underwent 217interventions. The CT scan was correct in 185cases (85.3%). Discrepancies observed: 26patients (11.9%) with more metastases resected than observed and 6cases (2.8%) with fewer metastases. In patients with one or two metastases of colorectal origin or a single metastasis of any other origin, the probability of finding extra nodules was 9.5%. In the remaining patients, the probability was 27.8%, with statistically significant differences (P=.001). The mean age of the patients in whom no unobserved nodules were detected was 62.9 years compared to 56.5 years on average in patients who were free from any metastases (P=.001).
ConclusionsPatients older than 60years, with one or two metastases of colorectal origin or a single metastasis from any other origin were considered to be the group with low probability of having more metastases resected than observed.
La resección de las metástasis pulmonares de neoplasias primarias extrapulmonares se ha convertido en los últimos años en una parte esencial de la actividad de los servicios de cirugía torácica1. La evidencia procedente de series de casos permite afirmar que la exéresis completa en pacientes seleccionados proporciona una mayor supervivencia que los tratamientos no quirúrgicos1. El objetivo del tratamiento de las metástasis pulmonares es la extirpación completa de la metástasis con la mínima pérdida de parénquima pulmonar1,2. Antes de realizar la metastasectomía, la tomografía axial computarizada (TAC) torácica se considera la prueba de elección para determinar la extensión de la lesión intratorácica3. En los últimos años existe un debate en relación con la exactitud diagnóstica de la misma y la necesidad de la palpación pulmonar para determinar el número de nódulos metastásicos presentes en el pulmón4,5. Fiel reflejo de lo controvertido del tema es que en el libro Difficult decisions in thoracic surgery: An evidence based aproach se dedican 2 capítulos a la metastasectomía pulmonar6,7, y los autores concluyen que:
- -
En relación con la necesidad de palpación bipulmonar6, la ausencia de datos que demuestran la mejoría de supervivencia después de palpación de nódulos no detectados contralaterales justifica un acceso unilateral para nódulos detectados unilateralmente6.
- -
Comparando el abordaje por videotoracoscopia (VATS) frente a la toracotomía7: a)la toracotomía permite identificar nódulos adicionales en el 20% de los casos; b)la resección incompleta se considera un fracaso terapéutico, pero la resección incompleta no es sinónimo de presencia de lesión no detectable radiológicamente post-VATS; c)no hay evidencia científica que apoye que la toracotomía aporta mejoría clínica frente a la VATS en términos de supervivencia, y d)la afirmación de que la toracotomía aporta más ventaja que la VATS solo está apoyada por opinión de experto. La literatura disponible sugiere equivalencia, y los 2 accesos parecen apropiados para la resección de metástasis solitaria pulmonar.
En estos momentos, determinar la mejor forma de acceso está siendo objeto de debate. Frente a trabajos en los que se detectan hasta un 20% de metástasis no identificadas por la TAC, que escaparían a la TAC y la VATS8, tenemos un producción científica creciente en la que se observa una supervivencia y una supervivencia libre de enfermedad equiparable5,9,10 en los pacientes operados por VATS frente a los operados por toracotomía. Gossot et al.9 para pacientes con metástasis de osteosarcomas y Nakajima5 y Nakaset al.11 de origen colorrectal, muestran una supervivencia y una supervivencia libre de enfermedad equiparables en pacientes operados por VATS frente a los operados por toracotomía. En los últimos años la mejoría en las pruebas de imagen están produciendo una mejora en la precisión de la TAC, como podemos observar en el artículo publicado en 2008 por Kang et al.12, en el que la exactitud de la TAC llegaba al 96% en metástasis de origen colorrectal.
MétodosSe estudiaron los pacientes operados de metástasis pulmonar con intención curativa entre el 1 de enero de 1998 y el 30 de junio 2012. Durante este periodo se llevaron a cabo 229intervenciones, de las cuales 12 se realizaron mediante VATS, motivo por el cual fueron excluidas del estudio. En los pacientes incluidos se realizó una toracotomía y palpación unilateral para resecar todos los nódulos palpados. Se consideraron criterios para realizar la cirugía: tumor primario controlado (o con posibilidad de controlarlo), ausencia de metástasis extrapulmonares (con excepción de metástasis hepáticas resecables), el paciente se encontraba suficientemente sano para tolerar la cirugía (con buenas pruebas de función respiratoria) y con metástasis técnicamente resecables.
Intervención quirúrgicaTodos los pacientes fueron intervenidos por el Servicio de Cirugía Torácica del Hospital Universitario Donostia bajo anestesia general, ventilación unipulmonar y toracotomía posterolateral. Como parte del estudio preoperatorio, a todos los pacientes se les realizaron pruebas de función respiratoria (espirometría y difusión), fibrobroncoscopia y TAC. A partir de 2006 también se realizó PET-TAC en todos los pacientes. El procedimiento seguido para la intervención fue siempre el mismo: a)exploración de la pleura parietal y visceral; b)liberación de adherencias pleuropulmonares (si existían); c)identificación del nódulo/nódulos pulmonares, y d)cuando el nódulo era periférico: biopsia intraoperatoria con resección atípica. Si la biopsia intraoperatoria confirmaba la metástasis, no se resecaba más pulmón. Si el patólogo no podía determinar si la naturaleza de la lesión era metastásica o un tumor primario pulmonar, se procedía a lobectomía con linfadenectomía. En los casos en que el tumor era central y no permitía la biopsia intraoperatoria, se procedía a la lobectomía directamente. En los pacientes con metástasis y sospecha de afectación de adenopatías mediastínicas se realizó linfadenectomía.
Estudio preoperatorioTodos los casos fueron revisados preoperatoriamente por 2 radiólogos expertos en pulmón. Se realizó TAC helicoidal de una corona no multicorte (Siemens) con cortes de 5mm a los pacientes operados antes de noviembre de 2002 y TAC helicoidal de 2 coronas no multicorte (Siemens Somaton Volume Access) con cortes de 5mm y con contraste a los pacientes operados a partir de noviembre de 2002. Todos los pacientes fueron operados en los 40días posteriores a la realización de la TAC.
Análisis estadísticoEl objetivo fue comparar el número de metástasis identificados por TAC con el número de metástasis resecados por paciente (confirmados mediante anatomía patológica) tras palpación manual, por lo que los nódulos benignos palpados y resecados durante la intervención no fueron tomados en cuenta. Para el análisis estadístico se utilizó el programa Systat versión 13 y se describieron las variables cuantitativas mediante intervalo, mediana y media, y las variables cualitativas mediante frecuencias absolutas y relativas en porcentaje. Se midieron las diferencias entre ambos grupos mediante exacto de Fisher o chicuadrado para variables categóricas y Mann-Whitney para las variables cuantitativas.
El estudio cuenta con la aceptación del Comité de Ética de Investigación Clínica, según consta en Acta (n.o 02/2012), y con el consentimiento informado de los pacientes.
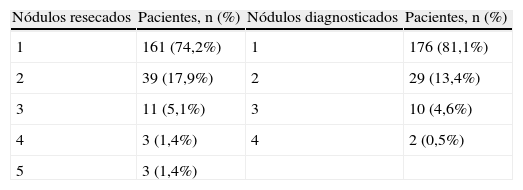
ResultadosSe consideraron para el estudio 183pacientes (63,6% varones) a los que se les realizaron 217intervenciones. La edad media fue de 61,7años (mediana, 63; rango, 24-82). Comparando los nódulos detectados en la TAC con los resecados en la cirugía, existió acierto en 185casos (85,3%). Entre las discordancias observadas: 26pacientes (11,9%) con más metástasis resecadas que las observadas y 6casos (2,8%) con menos metástasis que las observadas. En la tabla 1 se resumen las principales variables descriptivas del estudio.
Principales variables descriptivas del estudio
| Nódulos resecados | Pacientes, n (%) | Nódulos diagnosticados | Pacientes, n (%) |
| 1 | 161 (74,2%) | 1 | 176 (81,1%) |
| 2 | 39 (17,9%) | 2 | 29 (13,4%) |
| 3 | 11 (5,1%) | 3 | 10 (4,6%) |
| 4 | 3 (1,4%) | 4 | 2 (0,5%) |
| 5 | 3 (1,4%) |
| Origen | Resección realizada | ||
| Colorrectal | 123 (56,7%) | Resección atípica | 128 (58,9%) |
| Sarcoma | 29 (13,4%) | Lobectomía | 71 (32,7%) |
| Riñón | 14 (6,5%) | Bilobectomía | 1 (0,5%) |
| Vejiga | 9 (4,1%) | Neumonectomía | 6 (2,8%) |
| Mama | 7 (3,2%) | Lobectomía+atípica | 7 (3,2%) |
| Otro | 35 (16,1%) | Otra | 4 (1,8%) |
En total se resecaron 299metástasis y se analizó el tamaño de estas. Los diagnosticados por TAC como media tuvieron un tamaño de 2,4cm (mediana, 2,0cm; rango, 0,4-8cm), y los no observados, una media de 0,6cm (mediana, 0,5cm; rango, 0,2-1cm). Comparando las 2 medias se observó que existen diferencias estadísticamente significativas (p<0,001). Los tumores menores de 1cm se infradiagnosticaron en el 19,4% de los casos, el 12,8% en los tumores entre 1 y 2cm y el 8,4% en mayores de 2cm. Las diferencias no resultaron estadísticamente significativas (p=0,213), aunque se observó la tendencia de que a menor diámetro, más probabilidad de que no se detectara alguna metástasis.
Análisis según número de metástasis observadas en tomografía axial computarizadaEn 176casos se vio un solo nódulo, de los cuales la valoración fue correcta en 158casos (89,8%); en 16pacientes (9,1%) se resecaron 2nódulos, y 3nódulos en 2pacientes (1,7%).
En 29pacientes se vieron 2nódulos, con un acierto del 72,4% (20pacientes); en 3pacientes (10,3%) solo había un tumor metastásico, y en 5pacientes (17,2%) se detectaron más metástasis en la pieza que las observadas.
En 10pacientes se observaron 3nódulos; en 5pacientes la valoración fue correcta (50,0%); en 2casos (20,0%) se vieron menos, y en 3casos (30,0%) aparecieron más nódulos.
En 2ocasiones se vieron 4nódulos: en uno (50,0%) se resecaron 3 en la pieza, y en otro (50,0%), 4nódulos.
Comparando el acierto de la TAC cuando observa una metástasis (89,8%) frente al acierto cuando dice haber más (65,8%), existen diferencias estadísticamente significativas (p<0,001). Pero al comparar el número de pacientes en los que se escapó una metástasis, se observó que en los pacientes en los que la TAC decía que había una, en el 10,0% de los pacientes se resecaba alguna más de las observadas, frente al 19,0% (p=0,099) cuando en la TAC se observaba más de una, lo cual significa que cuando la TAC dice que hay una única metástasis tiene una kappa Cohen de 0,72, lo que representa un acuerdo sustancial entre los datos observados por TAC y resecados tras la cirugía.
Análisis según histologíaLa histología más frecuentemente hallada fue la de adenocarcinoma intestinal (111pacientes a los que se realizaron 123intervenciones). Se llevaron a cabo 23intervenciones en pacientes con tumores de origen urogenital y 29sarcomas. Se infradiagnosticaron metástasis en el 8,9% de los colorrectales, en el 13,8% de sarcomas, en el 21,7% de tumores urogenitales y en el 14,3% del resto de orígenes. Comparando los diferentes grupos, aunque hubo mayor tendencia a que se escaparan metástasis en el grupo de origen urogenital, no se observaron diferencias estadísticamente significativas (p=0,327).
Agrupando a los pacientes de origen colorrectal con una o 2 metástasis y metástasis única de cualquier origen, la probabilidad de resecar nódulos adicionales fue del 9,5%. Comparándolo con el resto, donde la probabilidad fue del 27,8%, se observaron diferencias estadísticamente significativas (p=0,001).
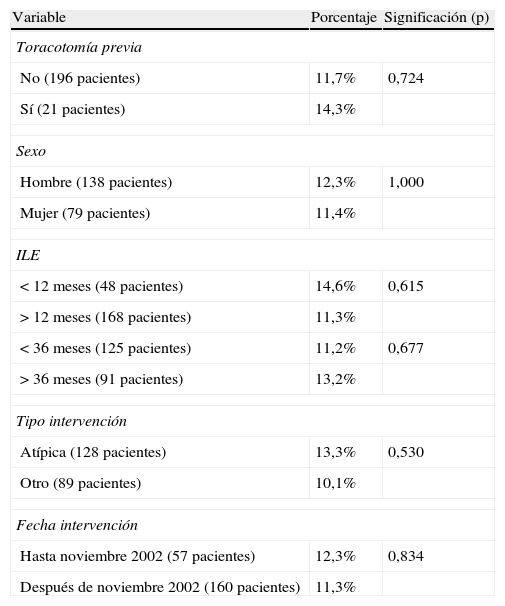
Otras variablesSe analizaron otras variables, como la edad, observando que la edad media de los pacientes en los que no aparecían nódulos no observados fue de 62,9años, frente a 56,5años de media en los pacientes que se escapaba alguna metástasis (p=0,001). En relación al intervalo libre de enfermedad, realización de toracotomía previa, sexo, fecha o tipo de intervención, no se observaron diferencias estadísticamente significativas (tabla 2).
Pacientes en los que se resecaron más metástasis que las observadas por TAC
| Variable | Porcentaje | Significación (p) |
| Toracotomía previa | ||
| No (196 pacientes) | 11,7% | 0,724 |
| Sí (21 pacientes) | 14,3% | |
| Sexo | ||
| Hombre (138 pacientes) | 12,3% | 1,000 |
| Mujer (79 pacientes) | 11,4% | |
| ILE | ||
| < 12 meses (48 pacientes) | 14,6% | 0,615 |
| > 12 meses (168 pacientes) | 11,3% | |
| < 36 meses (125 pacientes) | 11,2% | 0,677 |
| > 36 meses (91 pacientes) | 13,2% | |
| Tipo intervención | ||
| Atípica (128 pacientes) | 13,3% | 0,530 |
| Otro (89 pacientes) | 10,1% | |
| Fecha intervención | ||
| Hasta noviembre 2002 (57 pacientes) | 12,3% | 0,834 |
| Después de noviembre 2002 (160 pacientes) | 11,3% | |
ILE: intervalo libre de enfermedad.
Hasta noviembre de 2012 se utilizó TAC de una corona, y a partir de entonces, TAC de 2 coronas (ambos con cortes de 5mm).
Añadiendo la variable de la edad, los pacientes se pueden dividir en 2 grandes grupos. 1)Grupo con baja probabilidad de detectar metástasis extra: paciente mayor de 60años, con una o 2 metástasis de origen colorrectal o una de cualquier otro origen, donde solo en el 4,4% de los pacientes se escapó alguna metástasis. 2)Grupo con alta probabilidad de detectar metástasis extra: pacientes menores de 60años, con más de 2metástasis de origen colorrectal o más de una de cualquier otro origen (20,4% de pacientes con más metástasis resecadas que las observadas, p<0,001).
DiscusiónEl papel de la VATS para resecar metástasis pulmonares es controvertido7,13,14, ya que las ventajas de la VATS se enfrentan a su mayor inconveniente: la imposibilidad de palpar el pulmón. Entre las ventajas destacan: excelente visualización de la superficie pleural1, menor respuesta inmunológica frente al estrés quirúrgico15, disminución del dolor postoperatorio15, estancia hospitalaria más breve15 y postoperatorio con menos complicaciones que en la toracotomía10,16,17. Además, debido a que hasta el 50% de los pacientes operados por metástasis pulmonar presentarán nuevos nódulos pulmonares15, y puesto que la VATS produce menos adherencias pleuropulmonares, puede favorecer la reintervención en los pacientes con recidiva10,12,18. Por el contrario, la importancia de no poder palpar el pulmón radica en que podemos encontrar numerosas publicaciones en las que se detectan en torno a un 20% de metástasis no diagnosticadas previamente4,8,19-21.
En nuestra experiencia inicial con la VATS para metástasis pulmonar observamos supervivencia global y libre de enfermedad equiparable a la de los operados por toracotomía y el mismo índice de recurrencia pulmonar22. Estos resultados coinciden con el ensayo publicado por Nakas et al.11, quienes compararon a 25pacientes intervenidos por toracotomía con 27VATS y no observaron diferencias estadísticamente significativas en supervivencia, recurrencia y recurrencia en el mismo pulmón. Más tarde, Nakajima et al.5 reproduciría los mismos resultados con pacientes con metástasis de origen colorrectal y Gossot et al.9 para pacientes con metástasis sarcomatosas. Por todo ello, consideramos que la VATS puede ser una opción terapéutica en pacientes seleccionados23, y que para intentar minimizar el efecto negativo de la ausencia de palpación pulmonar sería interesante estudiar la posibilidad de agrupar a los pacientes por probabilidad de tener nódulos no detectables por TAC.
Según los resultados derivados del Registro Internacional de Metástasis Pulmonares24, el acierto de la TAC para detectar el número exacto de nódulos pulmonares fue del 61%. Con estos hallazgos, concluyeron que se precisa de la palpación bilateral manual para la estadificación final y poder resecar todas las metástasis.
En 2007, Parsons et al.19 publicaron los resultados observados tras intervenir a 60pacientes con metástasis unipulmonares por TAC; a todos los pacientes se les realizó palpación bilateral, encontrando un 23% de pacientes con metástasis en el hemitórax supuestamente sano, por lo que concluyeron, igual que el registro, que la palpación bilateral era obligatoria en la cirugía de las metástasis. Asimismo, Roth et al.25 compararon los resultados de los pacientes operados por esternotomía (que permite palpar ambos pulmones con una incisión única) con la toracotomía, donde se detectaron metástasis bilaterales no detectadas por TAC en los pacientes operados por esternotomía. Pero al analizar la supervivencia de ambos grupos no se vieron diferencias al comparar ambos grupos25. Más tarde, Younes et al.26, en la misma línea de investigación, determinaron que la mayoría de los pacientes con patología unipulmonar por TAC tenían patología unipulmonar, y que retrasar la toracotomía contralateral hasta que las lesiones se hacían visibles por TAC no afectaba a la superevivencia26. Por todo ello, Patel y DeCamp6 concluyen en su revisión que la ausencia de datos que demuestran la mejoría de supervivencia después de palpación de nódulos no detectados contralaterales justifica un acceso unilateral para nódulos detectados unilateralmente6.
En el año 2008 se publicó una encuesta realizada a los miembros de la Sociedad Europea de Cirugía Torácica27, en la que el 98% de los cirujanos encuestados contestó abordar un único hemitórax en los casos de afectación unipulmonar por TAC. De esa misma encuesta27 se desprende que para el 65% de los cirujanos la palpación es necesaria, es decir, que consideran inaceptable que se pudieran escapar hasta un 20% de metástasis si se realizara una cirugía mínimamente invasiva. Es por ello que resulta especialmente interesante delimitar el grupo de pacientes en los que más acierta la TAC, ya que serían candidatos ideales a la VATS.
En la mayoría de los estudios para determinar el acierto de la TAC se compararon los nódulos identificados por TAC con los resecados4,8,12,20,21, pudiendo ser estos últimos bien metastásicos o bien benignos (en torno al 30-40% de los nódulos extra resecados fueron benignos8,19,20). Para facilitar el análisis estadístico en nuestro estudio se analizaron solo las metástasis no detectadas por TAC, ya que la presencia de nódulos benignos no resecados no representa un empeoramiento en la supervivencia.
En nuestro estudio se resecaron metástasis no observadas en 26pacientes (11,9%). Parsons et al.19 encontraron que el 46% de los pacientes presentaban nódulos no detectados previamente. Analizando detenidamente las características de los pacientes incluidos en su serie, cabe destacar que la mayoría de los pacientes operados tenían un origen sarcomatoso. Chun et al.17, en cambio, tras revisar 120pacientes con tumor de origen colorrectal detectaron metástasis no identificadas en el 25% de pacientes. Cerfolio et al.28 y Kang et al.12 encontraron diferencias al comparar pacientes con metástasis de origen colorrectal con los sarcomatosos: los pacientes con sarcomas tenían más metástasis no detectadas, y en el grupo no sarcomatoso la TAC obtuvo un valor predictivo negativo del 96% y una sensibilidad del 97%12. Del mismo modo, en el trabajo de Chun et al.17 la sensibilidad de la TAC en pacientes con metástasis única de origen colorrectal fue del 95%.
Para intentar mejorar el diagnóstico preoperatorio se ha analizado el valor de la PET. La misma puede aportar información sobre infiltración de adenopatías mediastínicas3 y para detectar patología extrapulmonar29, pero no ayuda en la detección de nódulos pulmonares extra, ya que la sensibilidad de la PET para detectar nódulos menores de 10mm es del 30%29.
Según los resultados obtenidos en nuestro estudio, en el grupo con baja probabilidad de detectar metástasis extra (paciente mayor de 60años con una o 2metástasis de origen colorrectal o una de cualquier otro origen), solo en el 4,4% de los pacientes se escapó alguna metástasis. Estos serían los candidatos ideales a abordar mediante cirugía mínimamente invasiva, dado que se beneficiarían de sus ventajas, disminuyendo al máximo el posible efecto deletéreo que tendría la falta de resección de todas las metástasis. Por el contrario, como grupo con alta probabilidad de detectar metástasis extra estarían los pacientes menores de 60años con más de 2metástasis de origen colorrectal o más de una de cualquier otro origen (20,4% de pacientes con más metástasis resecadas que las observadas). Para plantear la intervención en este grupo, ambos —cirujano y paciente— deben discutir los pros y los contras de cada abordaje, conociendo las ventajas y las limitaciones de cada técnica.
ConclusionesSe considera grupo con baja probabilidad de resecar más metástasis que las observadas a los pacientes mayores de 60años con una o 2metástasis de origen colorrectal o una de cualquier otro origen.
El grupo con baja probabilidad de resecar más metástasis que las observadas son los candidatos ideales a operar mediante cirugía videotoracoscópica. En el resto de pacientes habría que valorar más detenidamente la probabilidad de que se escape una metástasis y los beneficios de la VATS frente a la toracotomía.
Limitaciones del estudioLa principal limitación del estudio radica en que se trata de un estudio retrospectivo, por lo que las conclusiones que se derivan de él deben considerarse como un punto de inicio para futuros estudios prospectivos.
Contribución de los autoresJZ: diseño, redacción del primer borrador y del manuscrito final; BA: revisión bibliográfica y colaboración en la redacción del primer borrador; JI: recogida de datos, revisión del manuscrito; MM: estudio de imagen preoperatorio, revisión del manuscrito; FB: estudio de imagen preoperatorio; MM: recogida de datos; CL: estudio anatomopatológico; JE: análisis estadístico, revisión del manuscrito.
FinanciaciónEste trabajo no ha recibido financiación de ningún tipo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.