La bronquitis plástica (BP) es una enfermedad infrecuente caracterizada por la formación de moldes bronquiales que ocluyen parcial o totalmente la luz bronquial1,2. Se describe como una complicación de enfermedades respiratorias, anomalías linfáticas, infecciones y sobre todo después de la cirugía de cardiopatías congénitas, especialmente en el postoperatorio de intervención tipo Fontan1,2, siendo frecuente su confusión con broncoaspiraciones2. Presentamos una serie de casos de pacientes diagnosticados de bronquitis plástica.
Desde 2001 hasta 2016 se diagnosticaron 13 pacientes afectos de bronquitis plástica, realizándose un total de 18 broncoscopias. Todos los pacientes fueron diagnosticados mediante broncoscopia flexible (BF).
La edad media de los pacientes fue de 31 meses (mínimo: un mes, máximo: 8 años), siendo 7 de ellos varones y 6 mujeres. La afección más frecuente subyacente fueron las sibilancias recurrentes y el asma, presente en 10 pacientes. Los otros 3 pacientes correspondieron a una tosferina maligna, una leucosis linfoide y una cardiopatía congénita compleja con ventrículo derecho de doble salida y múltiples intervenciones quirúrgicas, entre ellas una cirugía tipo Fontan.
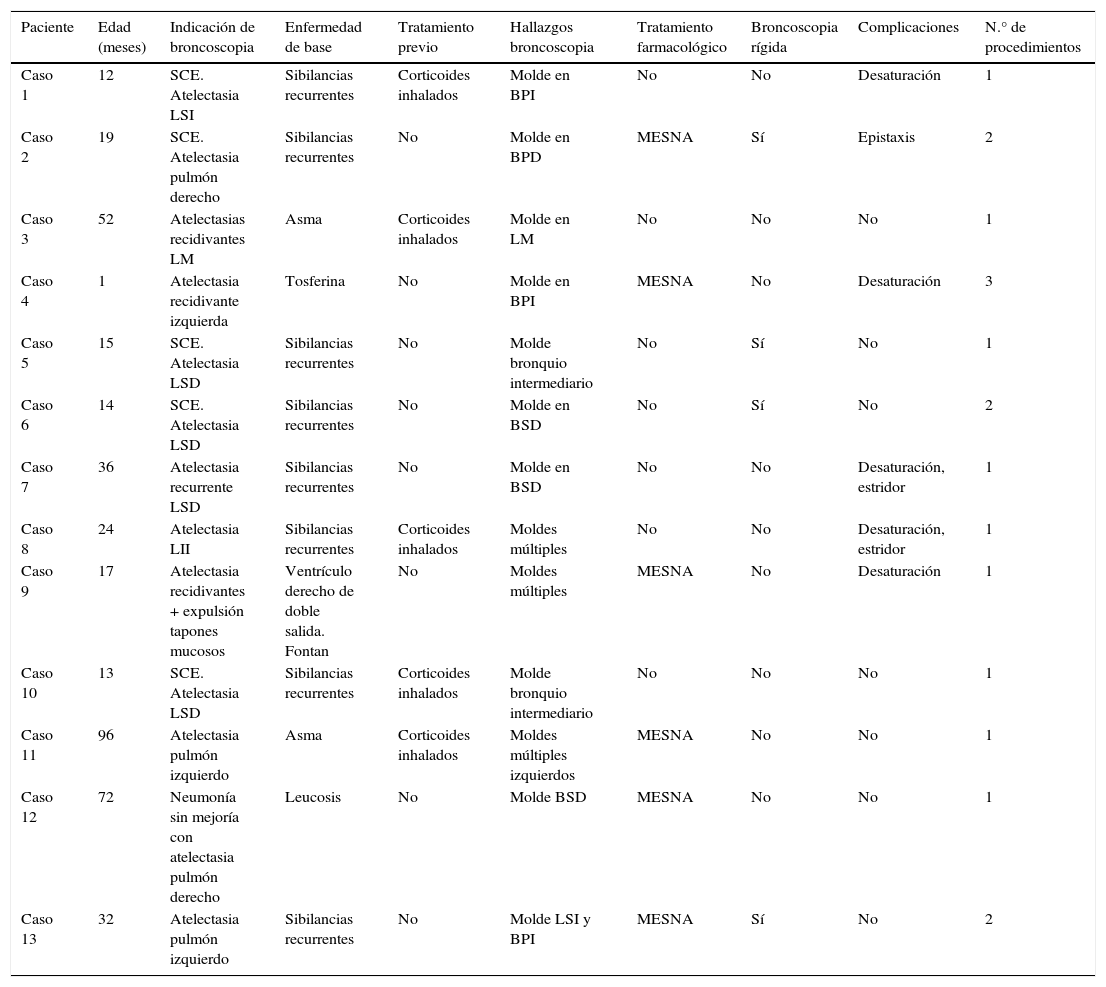
Los síntomas de presentación incluyeron: fiebre, dificultad respiratoria y broncorrea. Los hallazgos de la BF se detallan en la tabla 1.
Características clínicas y hallazgos broncoscópicos de los pacientes
| Paciente | Edad (meses) | Indicación de broncoscopia | Enfermedad de base | Tratamiento previo | Hallazgos broncoscopia | Tratamiento farmacológico | Broncoscopia rígida | Complicaciones | N.° de procedimientos |
|---|---|---|---|---|---|---|---|---|---|
| Caso 1 | 12 | SCE. Atelectasia LSI | Sibilancias recurrentes | Corticoides inhalados | Molde en BPI | No | No | Desaturación | 1 |
| Caso 2 | 19 | SCE. Atelectasia pulmón derecho | Sibilancias recurrentes | No | Molde en BPD | MESNA | Sí | Epistaxis | 2 |
| Caso 3 | 52 | Atelectasias recidivantes LM | Asma | Corticoides inhalados | Molde en LM | No | No | No | 1 |
| Caso 4 | 1 | Atelectasia recidivante izquierda | Tosferina | No | Molde en BPI | MESNA | No | Desaturación | 3 |
| Caso 5 | 15 | SCE. Atelectasia LSD | Sibilancias recurrentes | No | Molde bronquio intermediario | No | Sí | No | 1 |
| Caso 6 | 14 | SCE. Atelectasia LSD | Sibilancias recurrentes | No | Molde en BSD | No | Sí | No | 2 |
| Caso 7 | 36 | Atelectasia recurrente LSD | Sibilancias recurrentes | No | Molde en BSD | No | No | Desaturación, estridor | 1 |
| Caso 8 | 24 | Atelectasia LII | Sibilancias recurrentes | Corticoides inhalados | Moldes múltiples | No | No | Desaturación, estridor | 1 |
| Caso 9 | 17 | Atelectasia recidivantes + expulsión tapones mucosos | Ventrículo derecho de doble salida. Fontan | No | Moldes múltiples | MESNA | No | Desaturación | 1 |
| Caso 10 | 13 | SCE. Atelectasia LSD | Sibilancias recurrentes | Corticoides inhalados | Molde bronquio intermediario | No | No | No | 1 |
| Caso 11 | 96 | Atelectasia pulmón izquierdo | Asma | Corticoides inhalados | Moldes múltiples izquierdos | MESNA | No | No | 1 |
| Caso 12 | 72 | Neumonía sin mejoría con atelectasia pulmón derecho | Leucosis | No | Molde BSD | MESNA | No | No | 1 |
| Caso 13 | 32 | Atelectasia pulmón izquierdo | Sibilancias recurrentes | No | Molde LSI y BPI | MESNA | Sí | No | 2 |
BPD: bronquio principal derecho; BPI: bronquio principal izquierdo; BSD: bronquio superior derecho; LID: lóbulo inferior derecho; LII: lóbulo inferior izquierdo; LM: lóbulo medio; LSD: lóbulo superior derecho; LSI: lóbulo superior izquierdo; MESNA: 2-sulfaniletansulfonato; SCE: Sospecha de cuerpo extraño.
En cuanto al tratamiento, en todos los pacientes se extrajeron los moldes bronquiales. Cuatro de los 13 pacientes requirieron broncoscopia rígida (BR) para extracción completa del molde. Cuatro pacientes precisaron BF seriadas por sintomatología persistente. No hubo incidencias destacables durante el procedimiento, salvo, las desaturaciones autolimitadas. Se realizó estudio histológico del material obtenido del paciente cardiópata con hallazgos de material fibrinoso con escasa celularidad.
Respecto a la evolución, 11/13 pacientes se recuperaron en la totalidad y 2 de ellos fallecieron. Los fallecimientos correspondieron al paciente con cardiopatía congénita y a la paciente afecta de leucosis. El paciente intervenido de la cardiopatía congénita presentó una recurrencia de la BP transcurrido un mes, falleciendo en su centro de referencia por este motivo, mientras que la paciente afecta de leucosis falleció por su enfermedad de base.
La BP es un proceso infrecuente3, consistente en una obstrucción por moldes de la vía aérea predominantemente asociado a cardiopatías congénitas subyacentes o enfermedades pulmonares. Seear et al. clasificaron la BP en: tipo 1, moldes constituidos por células inflamatorias —frecuentes en enfermedades pulmonares— y tipo 2, moldes hipocelulares con mucina —frecuentes en cardiopatías4—. Aunque la etiología no está totalmente aclarada, parece ser que la formación de los moldes se debe a la estasis linfática en el pulmón. La pérdida de linfa al árbol bronquial tiene como consecuencia la obstrucción de la vía respiratoria y la pérdida de células linfoides e inmunoglobulinas, lo que implica mayor susceptibilidad a infecciones1,3. Madsen et al. proponen un modelo en el que los procesos inflamatorios que se activan en los cuadros de asma implicarían una disregulación en la formación del moco que junto con la disminución del aclaramiento mucociliar y la infiltración de la vía aérea por neutrófilos y eosinófilos explicaría la fisiopatología de la BP5. En las pruebas de imagen es frecuente encontrar atelectasias, lo que, plantea diagnóstico diferencial con broncoaspiración de cuerpo extraño.
En cuanto al tratamiento, consiste en lavado broncoalveolar y aspiración BF. En algunos casos se precisa el uso del BR para la aspiración y la extracción del material con las pinzas6.
Existen otras opciones de tratamiento como el recientemente descrito por Gibb et al. consistente en la administración del agente fibrinolítico activador tisular del plasminógeno (t-PA)7 vía BF, en el que nosotros no tenemos experiencia. Sin embargo, la mayoría de los estudios indican el uso inhalado del t-PA para la disrupción del molde bronquial6,8. Otras terapias incluyen: fibrinolíticos aerosolizados como la urokinasa o mucolíticos inhalados como la acetilcisteína y la dornasa alfa8–12. Los mucolíticos parecen ser más útiles en los moldes tipo 1, que tienen un contenido mayor en mucina4,11,12. En los pacientes afectos de cardiopatías congénitas es importante conseguir un buen gasto cardíaco, mientras que en las afecciones pulmonares que conllevan hiperreactividad bronquial, el uso de corticoides inhalados y sistémicos son una de las bases del tratamiento12.
En cuanto al pronóstico, generalmente es bueno1, salvo los casos asociados a cardiopatías congénitas, donde pueden alcanzar una mortalidad del 29%13 y una tasa de episodios aparentemente letales de hasta el 41% de los pacientes13.
En conclusión, aunque la BP es un proceso poco común, es necesario considerar esta enfermedad en las atelectasias recurrentes y ante la sospecha de cuerpo extraño intrabronquial. Los pacientes con cardiopatías subyacentes son los que tienen más riesgo de muerte, mientras que aquellos afectos de procesos inflamatorios cursan con cuadros de menor gravedad.
A todos los integrantes de la Sección de Neumología del Hospital Materno-Infantil de Málaga.